El campo de la farmacología moderna ha encontrado en las nanopartículas para la liberación controlada de analgésicos una solución innovadora para el manejo del dolor. Estas estructuras diminutas permiten la administración precisa y prolongada de fármacos, mejorando la eficacia terapéutica y reduciendo efectos secundarios. Al encapsular los principios activos, las nanopartículas optimizan su biodistribución y liberación en el organismo. Esta tecnología no solo incrementa la comodidad del paciente, sino que también abre nuevas posibilidades en el tratamiento de enfermedades crónicas. Su desarrollo representa un avance significativo en la medicina personalizada y la terapia del dolor.
Aplicaciones de las Nanopartículas para la liberación controlada de analgésicos
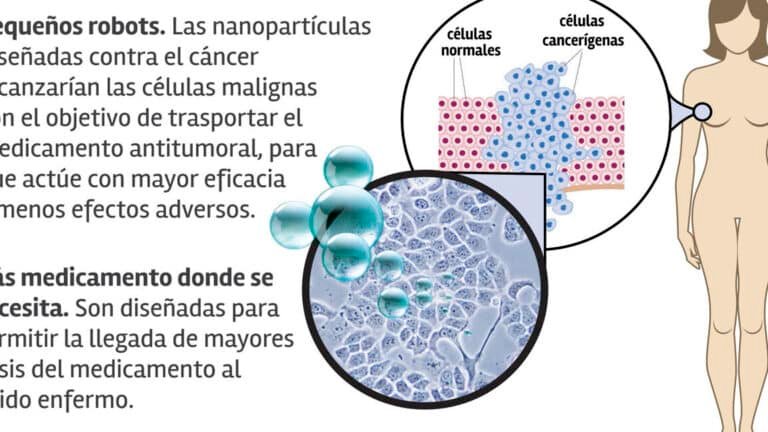
Las nanopartículas para la liberación controlada de analgésicos representan un avance significativo en la farmacología moderna. Estos sistemas permiten una administración más precisa y prolongada de fármacos, reduciendo efectos secundarios y mejorando la eficacia terapéutica. Mediante el uso de materiales biocompatibles, las nanopartículas pueden encapsular analgésicos y liberarlos de manera gradual en el organismo, optimizando su acción en el tratamiento del dolor crónico o agudo.
Ventajas de las Nanopartículas en la administración de analgésicos
La utilización de nanopartículas para la liberación controlada de analgésicos ofrece múltiples beneficios, como una mayor biodisponibilidad del fármaco, reducción de la frecuencia de dosificación y minimización de picos de concentración en sangre. Además, estas nanopartículas pueden dirigirse específicamente a tejidos afectados, disminuyendo el impacto en órganos sanos.
Tipos de materiales utilizados en la síntesis de nanopartículas
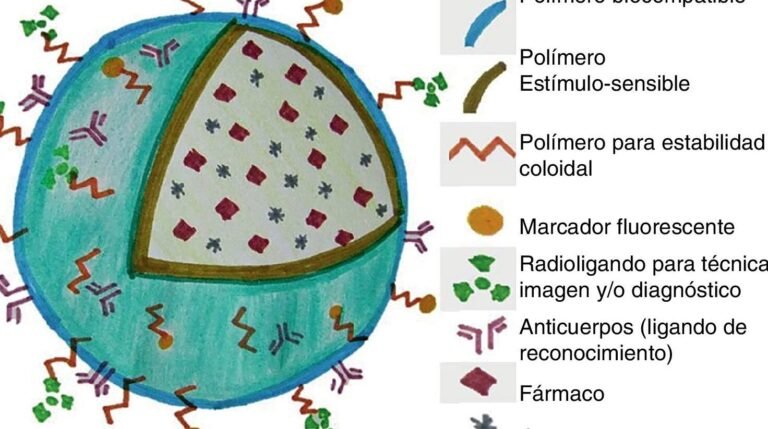
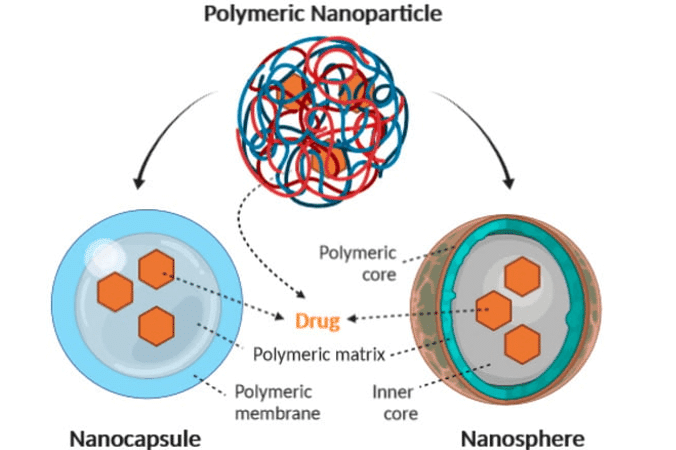
Los materiales más empleados en la fabricación de nanopartículas para la liberación controlada de analgésicos incluyen polímeros biodegradables (como PLGA), liposomas y dendrímeros. Cada material presenta características únicas en términos de biocompatibilidad, capacidad de carga y tiempo de liberación, lo que permite adaptar el sistema a diferentes necesidades clínicas.
Mecanismos de liberación controlada en nanopartículas
Los mecanismos de liberación en las nanopartículas para la liberación controlada de analgésicos pueden ser difusión controlada, erosión de la matriz o respuestas a estímulos externos (como pH o temperatura). Estos sistemas garantizan una dosificación sostenida y evitan fluctuaciones peligrosas en los niveles del fármaco en el organismo.
Desafíos en la implementación clínica de nanopartículas
A pesar de su potencial, las nanopartículas para la liberación controlada de analgésicos enfrentan retos como la escalabilidad en su producción, estabilidad a largo plazo y regulaciones sanitarias. La estandarización de protocolos y estudios de toxicidad a largo plazo son esenciales para su adopción masiva.
Casos de éxito y aplicaciones actuales
Actualmente, varias formulaciones basadas en nanopartículas para la liberación controlada de analgésicos han sido aprobadas para uso clínico, como sistemas de liberación prolongada de opioides o antiinflamatorios no esteroideos (AINEs). Estas innovaciones demuestran mejoras significativas en la calidad de vida de pacientes con dolor crónico.
| Tipo de Nanopartícula | Material | Analgésico encapsulado | Tiempo de liberación |
| Polimérica | PLGA | Morfina | Hasta 72 horas |
| Liposómica | Fosfolípidos | Lidocaína | 24-48 horas |
| Dendrímeros | PAMAM | Ketorolaco | 12-36 horas |
Preguntas Frecuentes
¿Qué son las nanopartículas para la liberación controlada de analgésicos?
Las nanopartículas son estructuras diminutas, generalmente entre 1 y 100 nanómetros, diseñadas para transportar y liberar analgésicos de manera controlada en el organismo. Esta tecnología permite una distribución precisa del fármaco, mejorando su eficacia y reduciendo efectos secundarios.
¿Cómo funcionan las nanopartículas en la administración de analgésicos?
Estas nanopartículas actúan como vehículos transportadores que liberan el analgésico de forma gradual en el sitio específico de acción. Su liberación controlada se debe a su composición y tamaño, lo que permite mantener niveles terapéuticos óptimos por más tiempo.
¿Cuáles son las ventajas de usar nanopartículas para analgésicos?
Entre las principales ventajas destacan la reducción de dosis, la minimización de efectos adversos y una mayor eficacia terapéutica. Además, permiten dirigir el fármaco al área afectada, evitando su degradación prematura en el organismo.
¿Qué tipos de analgésicos pueden administrarse con nanopartículas?
Las nanopartículas son versátiles y pueden encapsular tanto analgésicos opioides (como morfina) como no opioides (como el ibuprofeno). También son útiles para fármacos de alta potencia que requieren una administración precisa.