se ha convertido en un tema crítico a medida que los avances científicos abren nuevas posibilidades terapéuticas. Esta disciplina, que combina nanotecnología y medicina, promete tratamientos revolucionarios, pero también plantea desafíos en materia de seguridad y eficacia. Dado su carácter transfronterizo, es esencial establecer marcos normativos armonizados que garanticen la protección de los pacientes y la calidad de los productos. Organismos internacionales trabajan para definir estándares que equilibren innovación y control, asegurando que la nanomedicina se desarrolle de manera ética y responsable. es, por tanto, un pilar fundamental para su futuro sostenible.
La regulación internacional de la seguridad en nanomedicina: Avances y desafíos
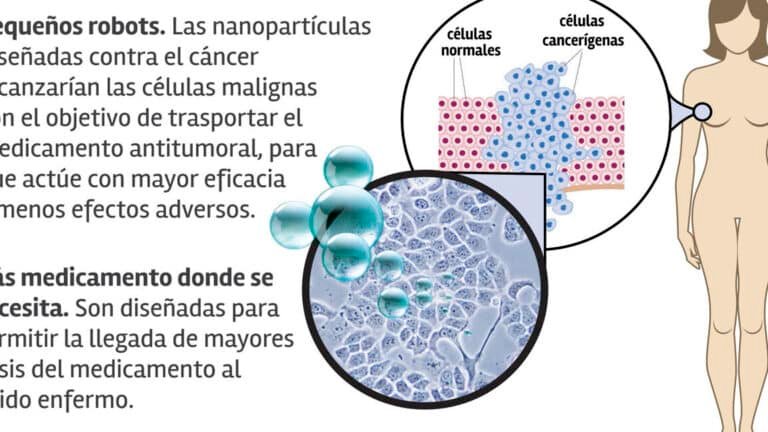
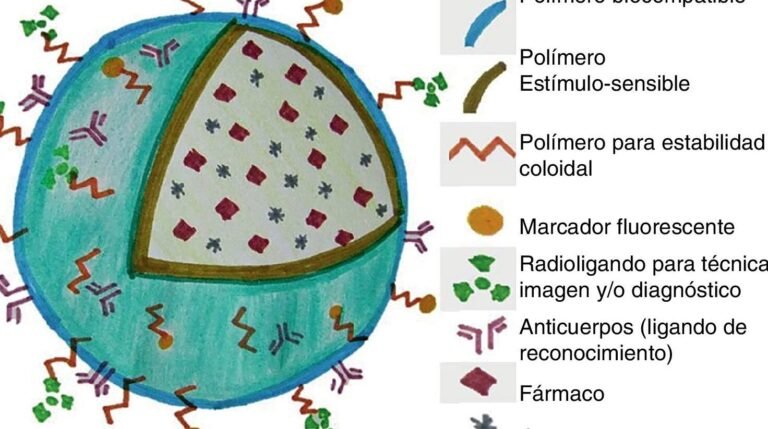
La regulación internacional de la seguridad en nanomedicina es un tema crítico en el ámbito de la salud global, dado el rápido desarrollo de tecnologías nanoescalares aplicadas a diagnósticos, tratamientos y sistemas de liberación controlada de fármacos. Este marco normativo busca garantizar que los productos basados en nanomedicina sean seguros, eficaces y éticos, mientras se fomenta la innovación científica. Países y organizaciones internacionales trabajan en armonizar estándares, aunque persisten desafíos debido a la naturaleza interdisciplinaria y la falta de consenso en metodologías de evaluación.
1. Fundamentos legales de la regulación internacional de la seguridad en nanomedicina
Los fundamentos legales se basan en tratados internacionales, directrices de la OMS y agencias como la FDA o la EMA. Estas entidades establecen requisitos para la aprobación de nanomedicamentos, enfatizando la evaluación de riesgos asociados a propiedades únicas de los nanomateriales, como su biodistribución o potencial toxicidad. Sin embargo, la falta de una definición universal de nanomaterial complica la estandarización.
2. Roles de las organizaciones internacionales en la supervisión
Organizaciones como la OECD y la ICN (International Council on Nanotechnology) impulsan cooperación técnica para desarrollar protocolos de pruebas. Sus esfuerzos se centran en armonizar marcos regulatorios regionales, evitando duplicidades y facilitando el acceso a mercados globales con garantías de seguridad.
3. Desafíos en la evaluación de riesgos de nanomedicinas
La heterogeneidad de nanopartículas y su interacción dinámica con sistemas biológicos dificultan la creación de modelos predictivos. Se requiere avanzar en técnicas de caracterización físico-química y estudios a largo plazo para cubrir vacíos en la regulación internacional de la seguridad en nanomedicina.
4. Comparativa de marcos regulatorios por región
| Región | Agencia Reguladora | Enfoque Principal |
| Estados Unidos | FDA | Evaluación caso por caso bajo normas existentes |
| Unión Europea | EMA | Adaptación de guías específicas para nanomateriales |
| Asia-Pacífico | PMDA (Japón) | Enfoque en innovación con requisitos adicionales |
5. Futuras direcciones para fortalecer la normativa
Se prevé la creación de bancos de datos globales sobre nanopartículas, junto con la integración de inteligencia artificial para predecir efectos adversos. La colaboración público-privada será clave para actualizar la regulación internacional de la seguridad en nanomedicina sin frenar el progreso científico.
Preguntas Frecuentes
¿Qué organismos internacionales regulan la seguridad en nanomedicina?
La seguridad en nanomedicina es supervisada por organismos como la Organización Mundial de la Salud (OMS), la Administración de Alimentos y Medicamentos (FDA) de EE.UU. y la Agencia Europea de Medicamentos (EMA). Estas entidades establecen directrices y estándares para garantizar el uso seguro de las nanopartículas en aplicaciones médicas.
¿Cuáles son los principales riesgos asociados a la nanomedicina?
Los riesgos incluyen toxicidad de nanopartículas, posibles efectos secundarios no deseados y desafíos en la biodegradabilidad. La falta de estudios a largo plazo sobre su impacto en el cuerpo humano también es una preocupación clave para los reguladores.
¿Existen normativas específicas para la aprobación de nanomedicamentos?
Sí, algunas agencias han desarrollado marcos regulatorios específicos que requieren ensayos clínicos rigurosos y evaluaciones de seguridad y eficacia. Por ejemplo, la FDA y la EMA exigen datos adicionales sobre el comportamiento de las nanopartículas en el organismo antes de su aprobación.
¿Cómo se coordina la regulación de la nanomedicina entre diferentes países?
La coordinación se logra mediante acuerdos internacionales y la armonización de estándares, como los propuestos por la Organización para la Cooperación y el Desarrollo Económicos (OCDE) o la International Council for Harmonisation (ICH). Sin embargo, persisten diferencias regionales en los requisitos de aprobación.