El síndrome de intestino corto (SIC) representa un desafío clínico significativo, caracterizado por la pérdida de capacidad funcional del intestino debido a resecciones quirúrgicas o malformaciones congénitas. Ante la limitada eficacia de los tratamientos convencionales, la emerge como una prometedora alternativa. Esta disciplina combina principios de ingeniería, biología celular y medicina regenerativa para desarrollar sustitutos intestinales funcionales que restauran la absorción de nutrientes. Los avances en biomateriales, cultivo de células epiteliales y técnicas de biofabricación abren nuevas perspectivas terapéuticas, ofreciendo esperanza a pacientes con SIC. Este artículo explora los últimos progresos y desafíos en este innovador campo.
Bioingeniería de tejido intestinal para el síndrome de intestino corto: Avances y aplicaciones clínicas
La Bioingeniería de tejido intestinal para el síndrome de intestino corto representa una innovadora estrategia terapéutica dirigida a pacientes con pérdida significativa de longitud intestinal. Este enfoque combina principios de ingeniería de tejidos, biomateriales y biología celular para desarrollar estructuras funcionales que mejoren la absorción de nutrientes y la calidad de vida.
1. Fundamentos científicos de la bioingeniería de tejido intestinal
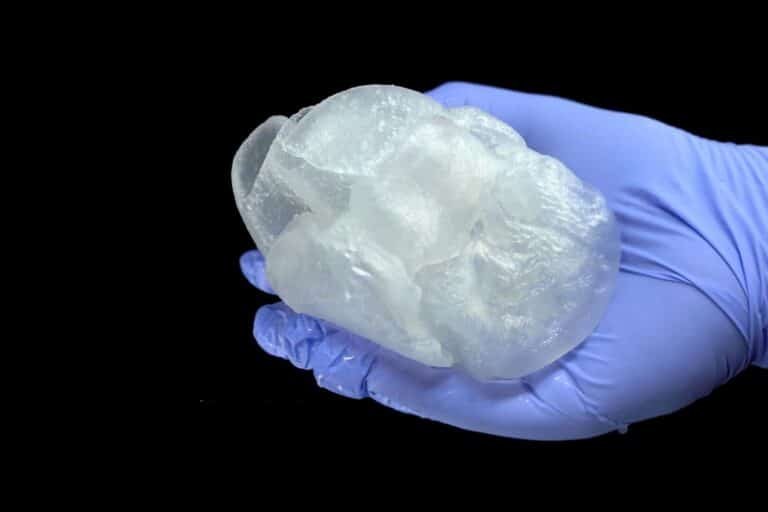
La Bioingeniería de tejido intestinal se basa en el uso de células madre, scaffolds biodegradables y factores de crecimiento para recrear la arquitectura y función del intestino. Estudios recientes demuestran que la combinación de células epiteliales intestinales con matrices 3D puede generar vellosidades funcionales, claves para la absorción nutricional en pacientes con síndrome de intestino corto.
2. Técnicas de fabricación en la ingeniería de tejidos intestinales
Los métodos avanzados incluyen biodiseño computacional, bioimpresión 3D y sistemas de bioreactores. La técnica de descelularización-recelularización ha mostrado resultados prometedores, utilizando matrices intestinales nativas repobladas con células del paciente para mantener características fisiológicas.
3. Desafíos en la vascularización del tejido bioingenierizado
Uno de los principales obstáculos es lograr una vascularización adecuada en los constructos de tejido intestinal. Investigaciones actuales exploran el uso de factores angiogénicos y microcanales en los scaffolds para promover la formación de redes capilares funcionales.
4. Resultados clínicos y estudios preclínicos relevantes
En modelos animales, los injertos de tejido intestinal bioingenierizado han demostrado capacidad para integrarse con el intestino nativo y desarrollar funciones absortivas. Los ensayos clínicos iniciales se centran en injertos de pequeño tamaño para evaluar seguridad y biocompatibilidad.
5. Perspectivas futuras y direcciones de investigación
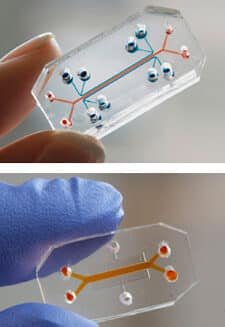
Las líneas de investigación emergentes incluyen el desarrollo de órganos bioartificiales completos y la combinación con tecnologías de microfluídica para crear sistemas intestinales más sofisticados. La personalización mediante células del paciente podría reducir riesgos de rechazo inmunológico.
| Tecnología | Ventajas | Desafíos |
|---|---|---|
| Bioimpresión 3D | Precisión anatómica, personalización | Escalabilidad, coste elevado |
| Scaffolds biodegradables | Compatibilidad, soporte estructural | Degradación controlada |
| Células madre organoides | Capacidad de diferenciación | Maduración funcional |
| Sistemas de bioreactores | Condiciones fisiológicas controladas | Complejidad técnica |
Preguntas Frecuentes
¿Qué es la bioingeniería de tejido intestinal para el síndrome de intestino corto?
La bioingeniería de tejido intestinal es un enfoque innovador que busca desarrollar tejidos intestinales funcionales en el laboratorio para tratar el síndrome de intestino corto (SIC). Esta técnica utiliza células madre y soportes biológicos para crear estructuras similares al intestino, capaces de mejorar la absorción de nutrientes en pacientes afectados.
¿Cómo funciona el proceso de bioingeniería de tejido intestinal?
El proceso implica aislar células progenitoras intestinales, cultivarlas en una matriz 3D y estimular su crecimiento para formar estructuras similares a las vellosidades intestinales. Estas estructuras se integran luego en el paciente para restaurar parcialmente la función digestiva y mejorar su calidad de vida.
¿Cuáles son los beneficios potenciales de esta tecnología?
Los principales beneficios incluyen la reducción de la dependencia de la nutrición parenteral, el aumento de la absorción de nutrientes y una posible mejora en la calidad de vida del paciente. Además, esta técnica podría disminuir complicaciones asociadas al SIC, como infecciones y problemas hepáticos.
¿Qué desafíos enfrenta la bioingeniería de tejido intestinal?
Entre los desafíos clave están la vascularización del tejido implantado, garantizar su funcionalidad a largo plazo y superar posibles rechazos inmunológicos. Además, se requiere más investigación para optimizar los protocolos y garantizar la seguridad en humanos.