En la vanguardia de la investigación oncológica, cómo la bioingeniería crea modelos de tumores personalizados se ha convertido en un tema clave para el desarrollo de terapias más precisas. Esta disciplina combina técnicas avanzadas de ingeniería y biología para replicar las características únicas de los tumores en entornos controlados, permitiendo estudiar su comportamiento y respuesta a tratamientos de manera individualizada. Estos modelos, diseñados a partir de células del propio paciente, ofrecen insights sin precedentes para la medicina personalizada, reduciendo la dependencia de ensayos tradicionales. Con ello, la bioingeniería no solo acelera el descubrimiento de fármacos, sino que también mejora las perspectivas de éxito en tratamientos contra el cáncer.
Avances en la creación de modelos de tumores personalizados mediante bioingeniería
La bioingeniería está transformando la investigación oncológica al permitir el desarrollo de modelos de tumores personalizados, que replican con precisión las características genéticas y microambientales de los tumores en pacientes individuales. Estos modelos facilitan la evaluación de terapias dirigidas y reducen la dependencia de ensayos en animales. A continuación, se detallan aspectos clave de este proceso innovador.
1. Técnicas de biofabricación de tejidos tumorales
La bioingeniería emplea técnicas como la impresión 3D de biomateriales y el cultivo de células tumorales en matrices tridimensionales para recrear la arquitectura del tumor original. Estos métodos permiten incorporar vascularización y componentes del microambiente tumoral, clave para estudiar la resistencia a fármacos y metástasis.
2. Integración de datos genómicos del paciente
Al secuenciar el ADN del tumor del paciente, los bioingenieros modifican líneas celulares o organoides para reflejar mutaciones específicas. Esto posibilita probar drogas in vitro con mayor precisión, un componente esencial en Cómo la bioingeniería crea modelos de tumores personalizados.
3. Uso de organoides y cultivos 3D
Los organoides derivados de biopsias conservan la heterogeneidad celular del tumor original. Estas estructuras autoorganizadas se cultivan en condiciones controladas, permitiendo analizar interacciones célula-célula y respuesta a inmunoterapias.
4. Aplicaciones en medicina de precisión
Estos modelos personalizados ayudan a identificar combinaciones terapéuticas óptimas antes del tratamiento clínico. Se han utilizado con éxito en cánceres de páncreas y glioblastoma, donde las opciones terapéuticas son limitadas.
5. Desafíos y futuras direcciones
Persisten retos como la estandarización de protocolos y la escalabilidad. Sin embargo, la combinación con inteligencia artificial para predecir comportamientos tumorales marca el futuro de esta disciplina.
| Tecnología | Aplicación | Ventaja |
|---|---|---|
| Organoides tumorales | Pruebas de sensibilidad a fármacos | Mantiene heterogeneidad original |
| Impresión 3D de hidrogeles | Replicación de microambiente tumoral | Control preciso de parámetros físicos |
| Secuenciación de células individuales | Identificación de subpoblaciones cancerosas | Detecta resistencias clonales |
Preguntas Frecuentes
¿Qué es un modelo de tumor personalizado en bioingeniería?
Un modelo de tumor personalizado es una representación creada en laboratorio a partir de células del paciente, que imita las características genéticas y biológicas de su tumor. La bioingeniería utiliza técnicas como cultivos 3D y biopsias líquidas para replicar la estructura y comportamiento del tumor, permitiendo estudios personalizados y pruebas de tratamientos específicos.
¿Qué técnicas utiliza la bioingeniería para crear estos modelos?
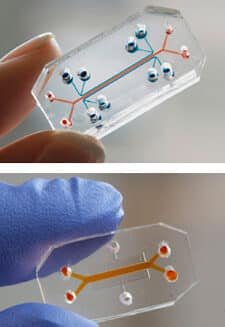
La bioingeniería emplea técnicas avanzadas como organoides tumorales, impresión 3D de tejidos y sistemas microfisiológicos (chips de órganos). Estas herramientas permiten recrear el microambiente tumoral, incluyendo vasos sanguíneos y células inmunitarias, para analizar cómo responde el tumor a terapias específicas.
¿Por qué son importantes los modelos personalizados para el tratamiento del cáncer?
Estos modelos permiten probar terapias dirigidas en un entorno controlado antes de aplicarlas al paciente, reduciendo riesgos y aumentando la eficacia. Al replicar la heterogeneidad del tumor, ayudan a identificar resistencias a fármacos y a diseñar estrategias de medicina de precisión adaptadas a cada caso.
¿Cuáles son los desafíos en la creación de modelos de tumores personalizados?
Los principales retos incluyen la obtención de muestras representativas, la reproducibilidad del modelo y la integración de la complejidad biológica del tumor original. Además, el alto costo y el tiempo requerido para desarrollar estos sistemas limitan aún su implementación masiva en entornos clínicos.