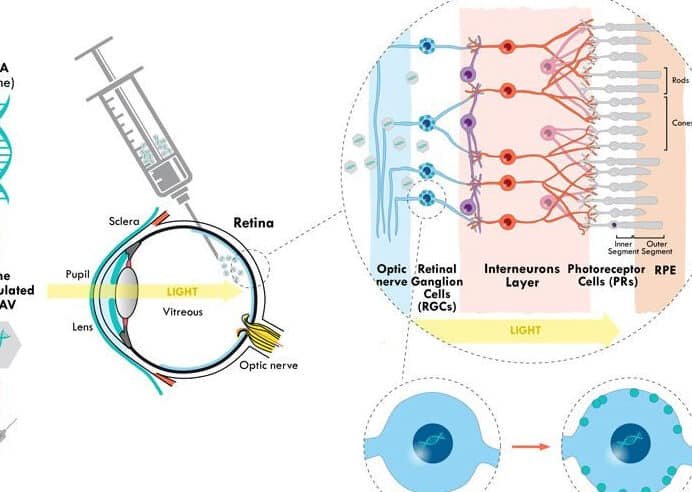
representa un avance revolucionario en el campo de la edición genética. Esta tecnología permite modificar con precisión el ADN defectuoso responsable de esta enfermedad hereditaria, ofreciendo esperanza a millones de pacientes en todo el mundo. La anemia de células falciformes, causada por una mutación en el gen de la hemoglobina, provoca graves complicaciones de salud. Gracias a CRISPR, los científicos pueden corregir esta mutación en células madre hematopoyéticas, restableciendo la producción de glóbulos rojos sanos. Este enfoque innovador no solo mejora la calidad de vida, sino que también abre nuevas puertas para el tratamiento de otras enfermedades genéticas.
El uso de CRISPR para corregir la anemia de células falciformes: Una revolución en la terapia génica
La tecnología CRISPR ha emergido como una herramienta revolucionaria en la edición génica, ofreciendo un potencial sin precedentes para tratar enfermedades genéticas como la anemia de células falciformes. Esta condición, causada por una mutación en el gen HBB, provoca la producción de hemoglobina defectuosa, lo que lleva a glóbulos rojos deformes y complicaciones clínicas severas. La aplicación de CRISPR permite corregir esta mutación directamente en las células madre hematopoyéticas, abriendo un horizonte terapéutico prometedor.
1. ¿Qué es la anemia de células falciformes y cómo afecta al organismo?
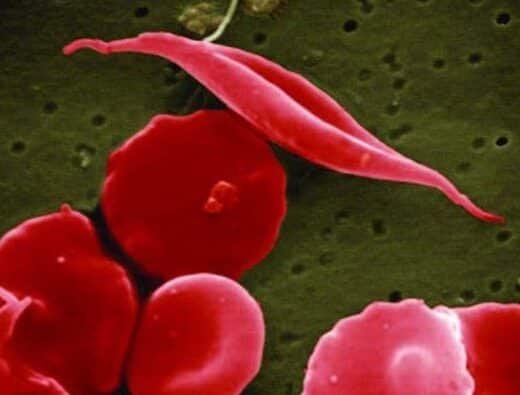
La anemia de células falciformes es un trastorno hereditario caracterizado por la producción de glóbulos rojos con forma de hoz. Estas células tienen una vida más corta y obstruyen los vasos sanguíneos, causando dolor intenso, daño orgánico e incrementando el riesgo de infecciones. La mutación en el gen HBB altera la estructura de la hemoglobina, reemplazando el aminoácido ácido glutámico por valina. El uso de CRISPR busca revertir esta alteración genética.
2. Mecanismo de acción de CRISPR en la corrección génica
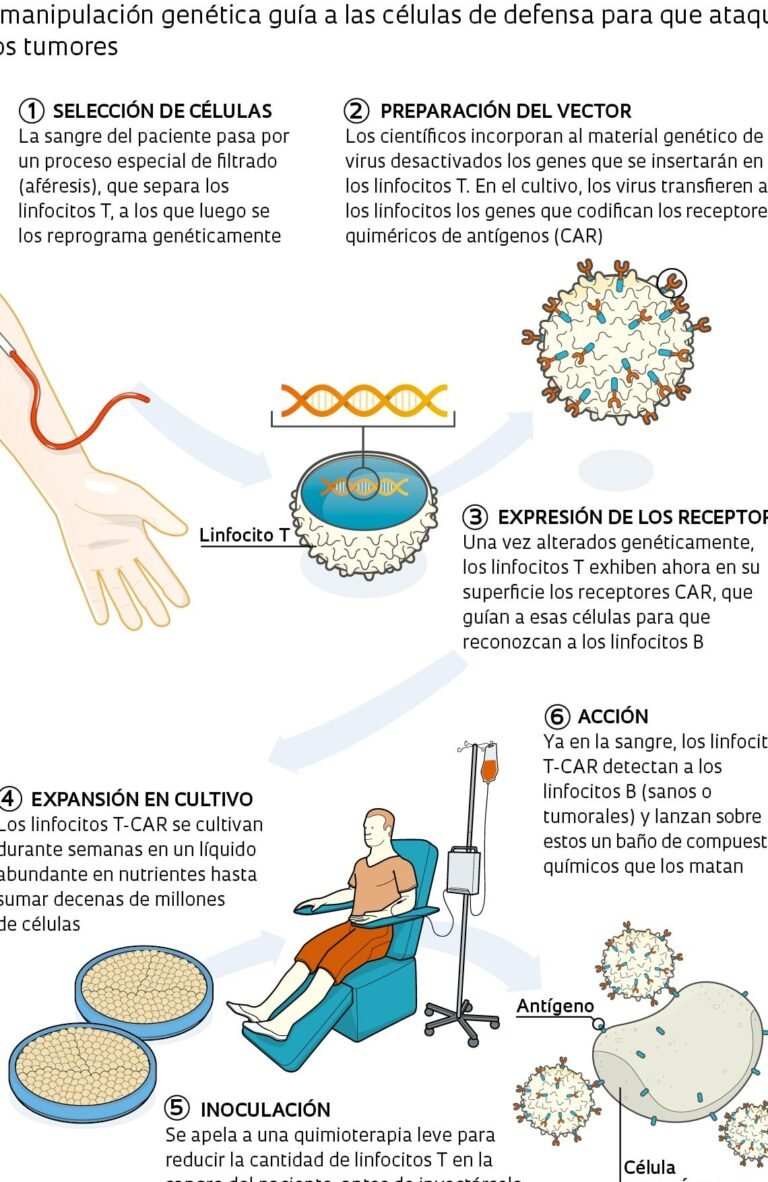
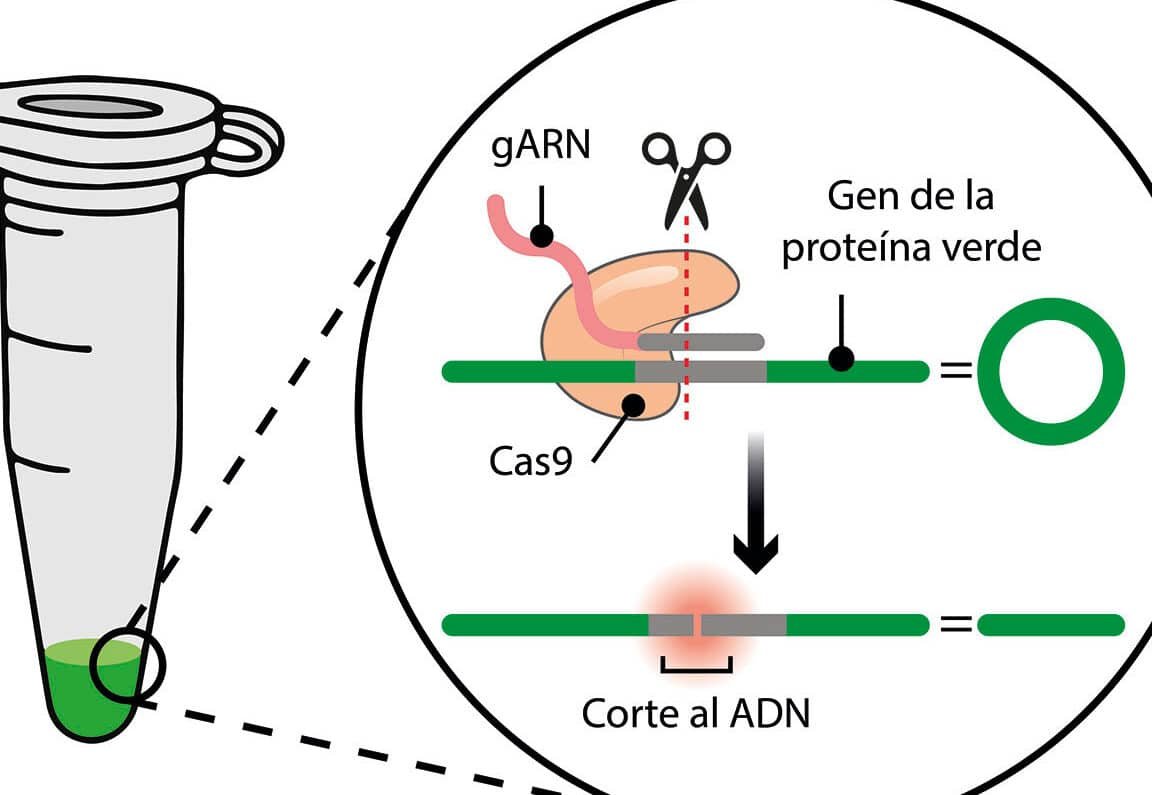
La técnica CRISPR-Cas9 actúa como unas tijeras moleculares que cortan el ADN en la ubicación exacta de la mutación. Mediante un ARN guía, el sistema se dirige al gen HBB y repara la secuencia defectuosa utilizando la maquinaria celular o una plantilla de ADN saludable. En el contexto de la anemia de células falciformes, esto restaura la producción de hemoglobina normal, eliminando los síntomas.
3. Avances clínicos y ensayos en humanos
Ensayos recientes, como el estudio CLIMB-SCD, han demostrado que el uso de CRISPR en pacientes con anemia de células falciformes puede lograr resultados sustanciales. Participantes tratados mostraron niveles elevados de hemoglobina fetal funcional, reduciendo significativamente las crisis de dolor. Estos avances respaldan la seguridad y eficacia de la terapia en entornos controlados.
4. Desafíos y consideraciones éticas
A pesar del potencial, el uso de CRISPR enfrenta retos, como posibles efectos off-target (cortes no deseados en el ADN) y dilemas éticos en la modificación de la línea germinal. Regulaciones estrictas y protocolos de monitoreo son esenciales para garantizar que la corrección de la anemia de células falciformes sea segura, accesible y equitativa.
5. Comparación entre CRISPR y otras terapias existentes
La siguiente tabla resume las diferencias clave entre el uso de CRISPR y tratamientos convencionales para la anemia de células falciformes:
| Terapia | Mecanismo | Ventajas | Limitaciones |
| CRISPR | Edición génica del HBB | Corrección permanente, potencialmente curativa | Coste elevado, requerimientos técnicos complejos |
| Transplante de médula ósea | Reemplazo de células madre defectuosas | Eficacia probada en casos compatibles | Rechazo inmunológico, escasez de donantes |
| Fármacos (hidroxiurea) | Estimulación de hemoglobina fetal | No invasivo, ampliamente disponible | Efectos secundarios, tratamiento sintomático |
Preguntas Frecuentes
¿Cómo funciona la tecnología CRISPR en el tratamiento de la anemia de células falciformes?
La tecnología CRISPR permite editar genes específicos asociados a la anemia de células falciformes, corrigiendo la mutación en el gen HBB que causa la producción de hemoglobina defectuosa. Utilizando una enzima llamada Cas9, se corta el ADN en el lugar preciso y se repara o reemplaza la secuencia dañada, restaurando la producción de hemoglobina normal.
¿Es seguro el uso de CRISPR para corregir esta enfermedad?
Aunque los estudios clínicos han mostrado resultados prometedores, el uso de CRISPR aún enfrenta desafíos de seguridad, como posibles efectos fuera del objetivo (off-target) o respuestas inmunes no deseadas. Los investigadores trabajan para garantizar que la técnica sea precisa y minimice riesgos antes de su aplicación generalizada.
¿En qué etapa se encuentra la investigación de CRISPR para la anemia de células falciformes?
Actualmente, la investigación se encuentra en fases clínicas avanzadas, con ensayos en humanos que evalúan la eficacia y seguridad de la terapia. Algunos resultados preliminares han demostrado una reducción significativa de los síntomas, aunque aún se requiere más estudio para su aprobación definitiva.
¿Cuáles son los posibles beneficios a largo plazo de esta terapia génica?
Los beneficios incluyen la curación potencial de la enfermedad, eliminando la necesidad de transfusiones sanguíneas frecuentes y reduciendo complicaciones como el dolor crónico. A largo plazo, la terapia génica con CRISPR podría ofrecer una solución duradera y mejorar significativamente la calidad de vida de los pacientes.