La farmacogenómica en cardiología: prevenir reacciones adversas se ha consolidado como una herramienta esencial para optimizar el tratamiento de pacientes con enfermedades cardiovasculares. Esta disciplina analiza cómo las variaciones genéticas individuales influyen en la respuesta a los fármacos, permitiendo personalizar terapias y reducir riesgos. En cardiología, donde medicamentos como anticoagulantes o antiarrítmicos presentan márgenes terapéuticos estrechos, su aplicación puede evitar efectos secundarios graves e incluso mortalidad. Al integrar datos genéticos en la práctica clínica, la farmacogenómica en cardiología: prevenir reacciones adversas no solo mejora la eficacia de los tratamientos, sino que también impulsa un enfoque más seguro y preciso en el manejo de los pacientes.
Farmacogenómica en cardiología: Avances para minimizar reacciones adversas a medicamentos
La Farmacogenómica en cardiología: Prevenir reacciones adversas es un campo emergente que busca personalizar tratamientos basados en la variabilidad genética de los pacientes. Esta disciplina permite identificar predisposiciones a efectos secundarios graves y optimizar la selección de fármacos cardiovasculares, mejorando la seguridad y eficacia terapéutica. Su aplicación es clave en fármacos como anticoagulantes, antiarrítmicos y betabloqueadores, donde las diferencias genéticas influyen significativamente en la respuesta al tratamiento.
1. ¿Qué es la farmacogenómica y por qué es relevante en cardiología?
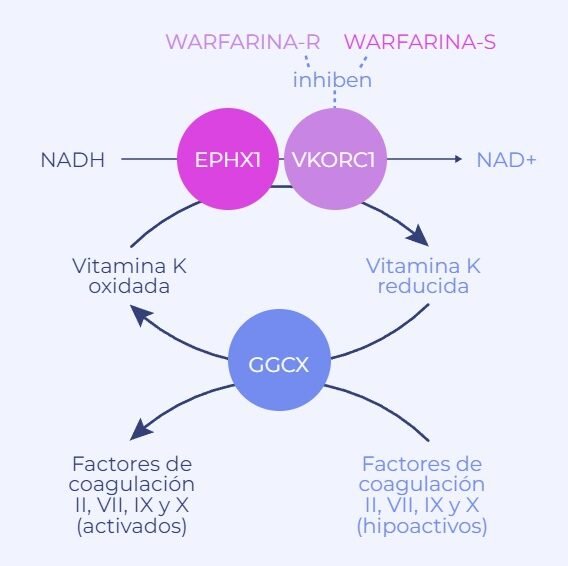
La farmacogenómica estudia cómo las variaciones genéticas afectan la respuesta a los fármacos. En cardiología, permite predecir reacciones adversas o falta de eficacia en medicamentos críticos como la warfarina o el clopidogrel. Por ejemplo, variantes en los genes CYP2C9 y VKORC1 determinan la dosis requerida de anticoagulantes, evitando sangrados o trombosis.
2. Principales fármacos cardiovasculares con implicaciones farmacogenómicas
Entre los medicamentos con mayor evidencia en Farmacogenómica en cardiología: Prevenir reacciones adversas destacan: – Clopidogrel: El gen CYP2C19 define su metabolización en pacientes con stent coronario. – Estatinas: Polimorfismos en SLCO1B1 aumentan el riesgo de miopatía. – Betabloqueadores: Variantes en ADRB1 influyen en la respuesta a metoprolol.
3. Beneficios de implementar la farmacogenómica en la práctica clínica
La integración de pruebas genéticas reduce hospitalizaciones por reacciones adversas en un 30% según estudios recientes. Además, optimiza costos al evitar terapias inefectivas y mejora la adherencia al tratamiento mediante esquemas personalizados, clave en enfermedades crónicas como la insuficiencia cardíaca.
4. Desafíos actuales y limitaciones de la farmacogenómica
Aunque prometedora, su adopción enfrenta barreras como: – Acceso limitado a pruebas genéticas en sistemas públicos de salud. – Falta de guías estandarizadas para la interpretación de resultados. – Necesidad de educar a profesionales sobre su aplicación clínica.
5. Casos de éxito: Ejemplos reales en cardiología
En instituciones líderes, la Farmacogenómica en cardiología: Prevenir reacciones adversas ha demostrado resultados tangibles. Un estudio en la Clínica Mayo redujo un 50% los eventos hemorrágicos en usuarios de warfarina al ajustar dosis según perfiles genéticos, validando su utilidad en la práctica rutinaria.
| Fármaco | Gen asociado | Reacción adversa prevenida |
| Warfarina | CYP2C9 , VKORC1 | Hemorragias o trombosis |
| Clopidogrel | CYP2C19 | Eventos isquémicos recurrentes |
| Simvastatina | SLCO1B1 | Miopatía severa |
Guía detallada sobre farmacogenómica en cardiología: Prevenir reacciones adversas
¿Cuál es el papel de la farmacogenómica en la predicción de reacciones adversas a medicamentos (RAM) en pacientes cardiovasculares?
La farmacogenómica en cardiología: prevenir reacciones adversas juega un papel crucial al analizar variaciones genéticas en pacientes cardiovasculares para predecir y evitar reacciones adversas a medicamentos (RAM). Esta disciplina permite identificar polimorfismos en genes como CYP2C19 o VKORC1, que influyen en el metabolismo de fármacos como los antiagregantes plaquetarios o anticoagulantes, optimizando así la selección y dosificación de tratamientos. Al integrar datos genómicos en la práctica clínica, se reduce el riesgo de eventos adversos graves, como hemorragias o resistencia a medicamentos, mejorando la seguridad y eficacia terapéutica en pacientes con condiciones cardíacas.
Variantes genéticas y metabolismo de fármacos cardiovasculares
La farmacogenómica en cardiología: prevenir reacciones adversas se centra en estudiar cómo variantes en genes como CYP2D6 o SLCO1B1 afectan la metabolización de fármacos como las estatinas o los betabloqueantes. Por ejemplo, pacientes con polimorfismos en CYP2C19 pueden presentar menor eficacia con clopidogrel, aumentando el riesgo de trombosis. Identificar estos marcadores genéticos permite ajustar dosis o elegir alternativas terapéuticas, minimizando las RAM.
Aplicación clínica de la farmacogenómica en anticoagulantes
En el uso de anticoagulantes como la warfarina, la farmacogenómica analiza genes como VKORC1 y CYP2C9 para predecir respuestas individuales. Pacientes con ciertas variantes requieren dosis significativamente menores para evitar sangrados. La siguiente tabla resume genes clave y su impacto:
| Gen | Fármaco | Efecto en RAM |
|---|---|---|
| VKORC1 | Warfarina | Mayor riesgo de hemorragia |
| CYP2C9 | Warfarina | Metabolismo lento, acumulación tóxica |
Impacto en la personalización de tratamientos antiagregantes
La farmacogenómica en cardiología: prevenir reacciones adversas es esencial en tratamientos con antiagregantes como clopidogrel o ticagrelor. Variantes en CYP2C19 pueden inactivar el clopidogrel, reduciendo su efecto antiplaquetario y aumentando el riesgo de infartos. La detección temprana de estos perfiles genéticos permite optar por alternativas como prasugrel, mejorando los resultados clínicos y evitando eventos cardiovasculares mayores.
¿Cómo pueden los fármacos basados en farmacogenómica prevenir la remodelación cardíaca en pacientes con enfermedades cardiovasculares?
Los fármacos basados en farmacogenómica pueden prevenir la remodelación cardíaca en pacientes con enfermedades cardiovasculares al personalizar el tratamiento según el perfil genético del individuo, optimizando la elección y dosificación de medicamentos para bloquear vías moleculares específicas implicadas en la progresión de la disfunción cardíaca. Esta aproximación permite identificar variantes genéticas asociadas con respuestas terapéuticas diferenciales, reduciendo así efectos adversos y mejorando la eficacia de fármacos como los betabloqueantes o los inhibidores de la enzima convertidora de angiotensina (IECA). La Farmacogenómica en cardiología: Prevenir reacciones adversas es clave para evitar terapias ineficaces o dañinas, promoviendo un manejo más preciso de la enfermedad.
Mecanismos moleculares de la farmacogenómica en la remodelación cardíaca
La farmacogenómica analiza cómo las variantes genéticas afectan la respuesta a fármacos que influyen en la remodelación cardíaca, como los que modulan el sistema renina-angiotensina-aldosterona (SRAA) o la vía de las catecolaminas. Por ejemplo, polimorfismos en el gen _ACE_ pueden determinar la eficacia de los IECA, mientras que mutaciones en el gen _ADRB1_ afectan la respuesta a betabloqueantes. Estos datos genéticos permiten seleccionar terapias que inhiban de manera óptima la fibrosis miocárdica y la hipertrofia ventricular, minimizando efectos no deseados.
Aplicación clínica de la farmacogenómica en enfermedades cardiovasculares
En la práctica clínica, la farmacogenómica se utiliza para guiar decisiones terapéuticas en condiciones como la insuficiencia cardíaca o la hipertensión arterial. Una estrategia común incluye pruebas genéticas para genes como _CYP2D6_ o _VKORC1_, que metabolizan fármacos cardiovasculares. La siguiente tabla resume ejemplos clave:
| Gen | Fármaco asociado | Implicación clínica |
|---|---|---|
| _CYP2D6_ | Metoprolol | Metabolizadores lentos requieren ajuste de dosis |
| _VKORC1_ | Warfarina | Variantes genéticas afectan la dosis terapéutica |
Beneficios de la farmacogenómica en la prevención de reacciones adversas
La implementación de la farmacogenómica reduce significativamente el riesgo de reacciones adversas al evitar combinaciones terapéuticas inapropiadas o dosis subóptimas. Por ejemplo, pacientes con variantes en _SLCO1B1_ pueden presentar toxicidad muscular con estatinas, mientras que aquellos con alteraciones en _CYP2C19_ podrían no beneficiarse de clopidogrel. Esta personalización mejora la seguridad y adherencia al tratamiento, especialmente en poblaciones con polimorfismos de alto riesgo.
¿De qué manera la farmacogenómica contribuye a reducir la incidencia de reacciones adversas a medicamentos en tratamientos cardiológicos?
La farmacogenómica en cardiología: prevenir reacciones adversas permite personalizar tratamientos al analizar variaciones genéticas que influyen en la respuesta a fármacos, optimizando la elección y dosificación de medicamentos para evitar efectos no deseados. Al identificar polimorfismos en genes como CYP2C19 o VKORC1, se pueden ajustar terapias con anticoagulantes o antiagregantes plaquetarios, reduciendo riesgos de hemorragias o trombosis. Esta aproximación mejora la seguridad y eficacia en pacientes cardiópatas, minimizando reacciones adversas y mejorando resultados clínicos.
Identificación de variantes genéticas en pacientes cardiológicos
La farmacogenómica en cardiología: prevenir reacciones adversas se basa en detectar mutaciones en genes clave como CYP2C19, asociado al metabolismo del clopidogrel, o SLCO1B1, relacionado con estatinas. Estos hallazgos permiten predecir respuestas anómalas y ajustar terapias, evitando efectos como mialgias o resistencia al tratamiento. Por ejemplo, pacientes con variantes CYP2C19 de metabolización lenta requieren alternativas como prasugrel para evitar fracasos terapéuticos.
Optimización de dosis basada en perfiles genéticos
La farmacogenómica permite calcular dosis precisas de fármacos como la warfarina, cuya eficacia depende del gen VKORC1. Una tabla ilustra cómo variantes genéticas influyen en la dosificación:
| Gen | Variante | Impacto en dosificación |
|---|---|---|
| VKORC1 | GG | Dosis altas requeridas |
| CYP2C9 | 2/3 | Dosis reducidas (20-30%) |
Reducción de interacciones farmacológicas en polimedicación
En pacientes cardiológicos polimedicados, la farmacogenómica analiza interacciones entre fármacos y enzimas metabólicas, como inhibidores del CYP3A4 que afectan a simvastatina. Esto evita efectos adversos como rabdomiólisis o toxicidad acumulativa, priorizando combinaciones seguras según el perfil genético individual.
¿Qué fármacos, respaldados por estudios farmacogenómicos, han demostrado mejorar la contractilidad cardíaca con menor riesgo de efectos adversos?
Estudios farmacogenómicos han identificado fármacos como los inhibidores de la fosfodiesterasa-3 (PDE-3) (por ejemplo, milrinona), los betabloqueantes selectivos (como metoprolol y carvedilol) y los moduladores de los canales de calcio (por ejemplo, levosimendán) que mejoran la contractilidad cardíaca con un menor riesgo de efectos adversos, al optimizar su dosificación según variantes genéticas como los polimorfismos en los genes CYP2D6 y ADRB1, lo que subraya la importancia de la Farmacogenómica en cardiología: Prevenir reacciones adversas mediante terapias personalizadas.
Inhibidores de la fosfodiesterasa-3 (PDE-3) y su perfil farmacogenómico
Los inhibidores de PDE-3, como la milrinona, han demostrado eficacia en mejorar la contractilidad cardíaca en pacientes con insuficiencia cardíaca aguda, especialmente en aquellos con variantes genéticas en PDE3A que afectan su metabolismo. La Farmacogenómica en cardiología: Prevenir reacciones adversas permite ajustar dosis para reducir el riesgo de arritmias, un efecto adverso común en sujetos con polimorfismos en KCNE2.
Betabloqueantes selectivos y su interacción con CYP2D6
El metoprolol y el carvedilol, betabloqueantes ampliamente utilizados, presentan una respuesta variable según el genotipo CYP2D6. Los metabolizadores lentos pueden experimentar mayores concentraciones plasmáticas, aumentando el riesgo de bradicardia, mientras que los ultrarápidos pueden requerir dosis más altas. La Farmacogenómica en cardiología: Prevenir reacciones adversas ayuda a personalizar tratamientos, mejorando la seguridad y eficacia.
Levosimendán y su mecanismo genómico en la contractilidad
El levosimendán, un modulador de los canales de calcio, ha mostrado beneficios en pacientes con variantes en RYR2 y SLC6A4, asociadas a una mejor respuesta inotrópica y menor incidencia de hipotensión. Estudios farmacogenómicos destacan su papel en terapias dirigidas, reforzando la Farmacogenómica en cardiología: Prevenir reacciones adversas mediante la identificación de subpoblaciones con mayor beneficio terapéutico.
| Fármaco | Genes involucrados | Efecto en contractilidad | Riesgo reducido de |
|---|---|---|---|
| Milrinona | PDE3A, KCNE2 | Aumenta el cAMP cardíaco | Arritmias ventriculares |
| Metoprolol | CYP2D6, ADRB1 | Mejora la función sistólica | Bradicardia excesiva |
| Levosimendán | RYR2, SLC6A4 | Sensibiliza a la troponina C | Hipotensión |
Preguntas Frecuentes
¿Qué es la farmacogenómica en cardiología y cómo ayuda a prevenir reacciones adversas?
La farmacogenómica en cardiología estudia cómo las variaciones genéticas individuales afectan la respuesta a fármacos cardiovasculares, permitiendo personalizar tratamientos para reducir reacciones adversas y mejorar la eficacia terapéutica.
¿Cuáles son los medicamentos cardiovasculares más comunes que requieren análisis farmacogenómico?
Fármacos como la warfarina, clopidogrel y estatinas (p. ej., simvastatina) suelen analizarse, ya que sus efectos varían según polimorfismos en genes como CYP2C9, CYP2C19 o SLCO1B1, evitando toxicidad o fallo terapéutico.
¿Cómo se realiza un test farmacogenómico para pacientes cardiológicos?
Se obtiene una muestra de ADN (sangre o saliva) para analizar genes clave relacionados con el metabolismo de fármacos. Los resultados guían al médico en la selección de dosis o medicamentos alternativos, optimizando la seguridad del paciente.
¿Qué beneficios tiene implementar la farmacogenómica en tratamientos cardiovasculares?
Reduce el riesgo de eventos adversos (hemorragias, toxicidad muscular), minimiza la prescripción por ensayo-error y acelera la eficacia del tratamiento, lo que se traduce en menores costos hospitalarios y mejor calidad de vida del paciente.