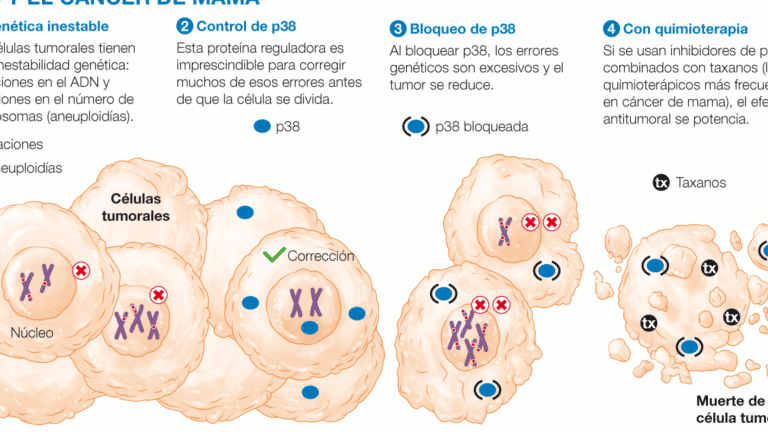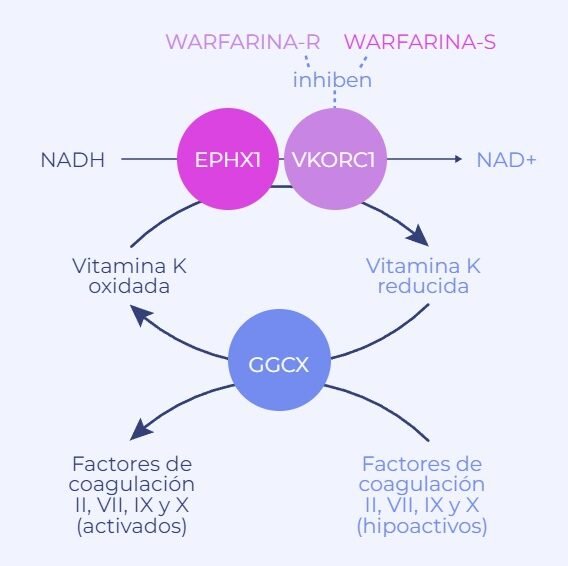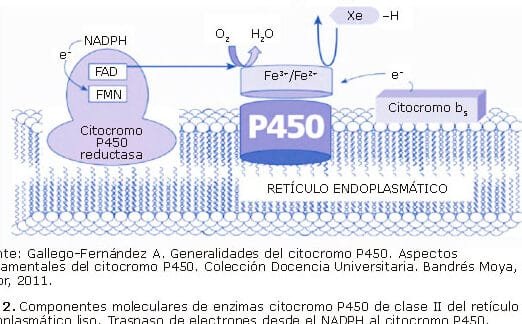
La representa un avance crucial en la medicina personalizada, ofreciendo nuevas esperanzas para pacientes con diagnósticos complejos. Las enfermedades raras, muchas de origen genético, presentan desafíos únicos en su tratamiento debido a la escasez de terapias específicas. Los medicamentos huérfanos, diseñados para estas afecciones, pueden optimizarse mediante la farmacogenómica, que estudia cómo la variabilidad genética individual influye en la respuesta a los fármacos. Esta disciplina no solo mejora la eficacia y seguridad de los tratamientos, sino que también reduce los efectos adversos, marcando un hito en el abordaje de patologías poco frecuentes con soluciones terapéuticas más precisas y efectivas.
Farmacogenómica en enfermedades raras y medicamentos huérfanos: Avances y desafíos
La Farmacogenómica en enfermedades raras y medicamentos huérfanos es un campo emergente que busca optimizar el tratamiento de pacientes con afecciones poco frecuentes. Esta disciplina estudia cómo las variaciones genéticas individuales afectan la respuesta a medicamentos huérfanos, diseñados específicamente para enfermedades raras. Su implementación puede reducir efectos adversos, mejorar la eficacia terapéutica y acelerar el desarrollo de tratamientos personalizados. Sin embargo, su aplicación enfrenta desafíos como la limitada disponibilidad de datos genómicos en poblaciones pequeñas.
1. ¿Qué es la Farmacogenómica aplicada a enfermedades raras?
La Farmacogenómica en enfermedades raras y medicamentos huérfanos analiza cómo el perfil genético de un paciente influye en su respuesta a tratamientos para condiciones poco comunes. Estas enfermedades, al afectar a menos de 1 por cada 2,000 personas, presentan desafíos únicos donde la farmacogenómica permite identificar subgrupos de pacientes que podrían beneficiarse de terapias específicas, reduciendo el enfoque de prueba y error en estos casos complejos.
2. Beneficios de la Farmacogenómica en el desarrollo de medicamentos huérfanos
La implementación de Farmacogenómica en enfermedades raras y medicamentos huérfanos puede agilizar los procesos de desarrollo y aprobación de estos tratamientos. Al identificar marcadores genéticos predictivos de respuesta, se reducen los tiempos y costos de investigación clínica, especialmente valioso dada la escasez de pacientes disponibles para ensayos. Además, permite establecer dosis más precisas y anticipar posibles reacciones adversas.
3. Desafíos éticos y regulatorios en este campo
La aplicación de Farmacogenómica en enfermedades raras y medicamentos huérfanos plantea cuestiones éticas significativas, incluyendo el manejo de datos genéticos sensibles en poblaciones vulnerables. Regulaciones diferenciadas para medicamentos huérfanos pueden dificultar la estandarización de pruebas farmacogenómicas. Además, existe el reto de garantizar equidad en el acceso a estas tecnologías costosas para condiciones con limitado interés comercial.
4. Casos de éxito en terapias personalizadas
Varios ejemplos demuestran el potencial de la Farmacogenómica en enfermedades raras y medicamentos huérfanos. El tratamiento de la atrofia muscular espinal con nusinersen o las terapias para la amiloidosis hereditaria por transtiretina muestran cómo los análisis genómicos permiten identificar pacientes con mayor probabilidad de respuesta. Estos avances están transformando el pronóstico de condiciones antes consideradas intratables.
5. Futuras direcciones de investigación en este campo
La evolución de la Farmacogenómica en enfermedades raras y medicamentos huérfanos requerirá mayor colaboración internacional para compartir datos genómicos limitados. Se explora la integración de inteligencia artificial para analizar patrones en pequeñas cohortes. Además, se investiga cómo extender estos enfoques a enfermedades ultra-raras (afectando <1 por millón), donde la escasez de casos dificulta aún más el desarrollo de evidencia.
| Aspecto clave | Impacto | Ejemplo |
| Reducción de efectos adversos | Mejora la seguridad en poblaciones sensibles | Dosificación de ivacaftor en fibrosis quística |
| Identificación de respondedores | Optimiza recursos terapéuticos limitados | Terapias enzimáticas para enfermedades lisosomales |
| Acortamiento de ensayos clínicos | Agiliza disponibilidad de tratamientos | Desarrollo de eteplirsen para distrofia muscular |
| Modelos predictivos | Facilita diseño de nuevas moléculas | Medicamentos para porfirias agudas |
Preguntas Frecuentes
¿Qué es la farmacogenómica y cómo se aplica en enfermedades raras?
La farmacogenómica estudia cómo los genes influyen en la respuesta a los fármacos. En enfermedades raras, esta disciplina permite personalizar tratamientos según el perfil genético del paciente, mejorando la eficacia y reduciendo efectos adversos.
¿Qué son los medicamentos huérfanos y cómo se relacionan con la farmacogenómica?
Los medicamentos huérfanos están diseñados para tratar enfermedades raras con prevalencia limitada. La farmacogenómica optimiza su uso al identificar marcadores genéticos que predicen respuesta terapéutica, asegurando tratamientos más precisos.
¿Cómo ayuda la farmacogenómica a reducir los efectos secundarios en pacientes con enfermedades raras?
Al analizar variantes genéticas, la farmacogenómica anticipa reacciones adversas a fármacos en enfermedades raras, permitiendo ajustar dosis o seleccionar alternativas terapéuticas más seguras para el paciente.
¿Qué desafíos presenta la implementación de la farmacogenómica en medicamentos huérfanos?
Los principales retos incluyen la escasa población para estudios clínicos, altos costos de desarrollo y la necesidad de más investigación en biomarcadores genéticos específicos para estas enfermedades.