representa un campo emergente en la medicina personalizada, transformando nuestra comprensión de la eficacia y seguridad de los tratamientos. Los mecanismos epigenéticos, como la metilación del ADN y las modificaciones de histonas, influyen en la expresión génica y, por ende, en la forma en que los pacientes metabolizan y responden a los medicamentos. Esta variabilidad epigenética puede explicar diferencias interindividuales en la efectividad terapéutica o la aparición de efectos adversos. Al integrar estos conocimientos, se abre la puerta a terapias más precisas, optimizando dosis y reduciendo riesgos. Así, la epigenética se consolida como un pilar clave en el futuro de la farmacología.
El impacto de la epigenética en la respuesta a fármacos: Una perspectiva científica
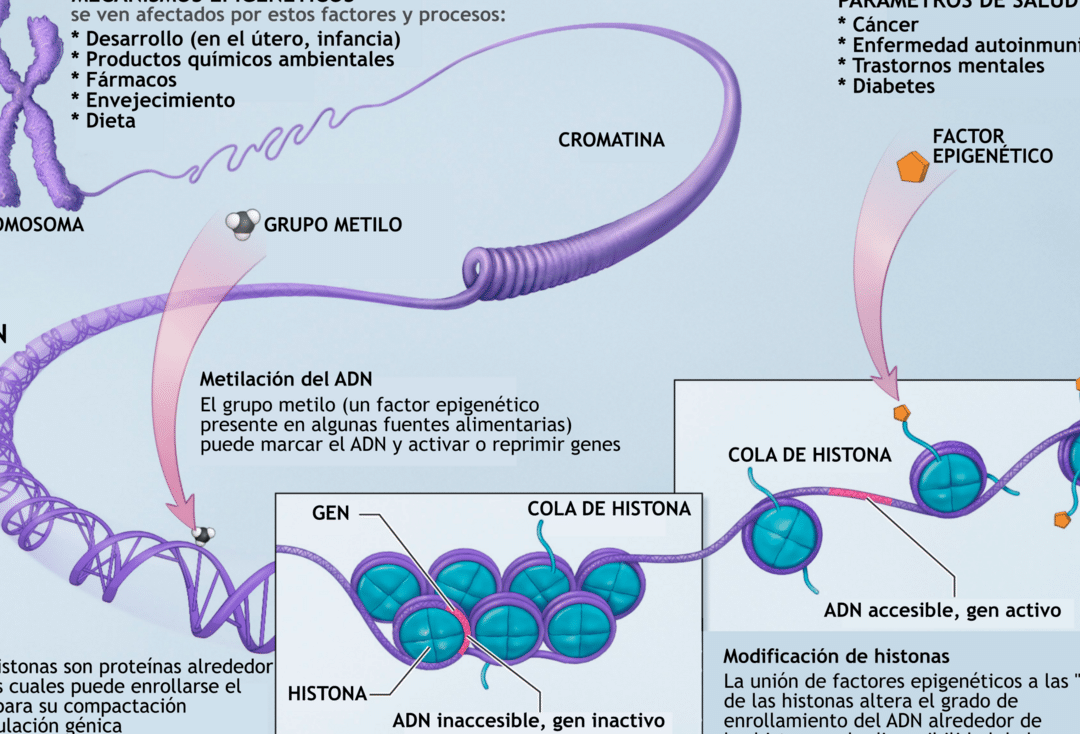
La epigenética ha surgido como un campo crucial en la farmacología moderna, ya que estudia las modificaciones hereditarias en la expresión génica sin alterar la secuencia del ADN. Estas modificaciones, como la metilación del ADN o las modificaciones de histonas, influyen directamente en cómo los pacientes responden a los tratamientos farmacológicos. El impacto de la epigenética en la respuesta a fármacos puede determinar la eficacia, toxicidad o resistencia a medicamentos, siendo esencial para el desarrollo de terapias personalizadas.
1. Mecanismos epigenéticos que modifican la eficacia de los fármacos
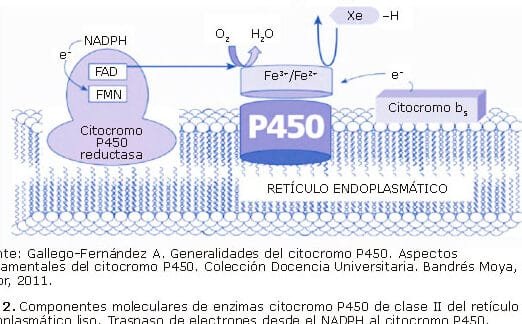
Los mecanismos epigenéticos, como la metilación del ADN o la acetilación de histonas, pueden alterar la expresión de genes involucrados en el metabolismo de fármacos. Por ejemplo, la hipermetilación de promotores génicos en enzimas como CYP450 puede reducir su actividad, afectando la degradación de ciertos medicamentos. El impacto de la epigenética en la respuesta a fármacos destaca la necesidad de considerar estos factores en el diseño de tratamientos.
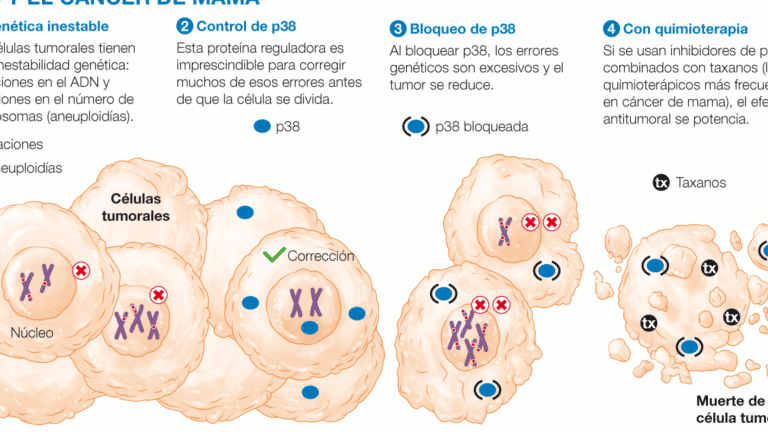
2. Epigenética y resistencia a medicamentos en oncología
En el cáncer, las alteraciones epigenéticas pueden contribuir a la resistencia a quimioterapias. La metilación aberrante de genes supresores de tumores o la desregulación de miRNAs pueden reducir la sensibilidad a fármacos. Estudios recientes demuestran que el impacto de la epigenética en la respuesta a fármacos es clave para desarrollar estrategias de re-sensibilización en pacientes resistentes.
3. Influencia de la epigenética en farmacogenómica
La farmacogenómica estudia cómo las variaciones genéticas afectan la respuesta a medicamentos, pero la epigenética añade otra capa de complejidad. Factores como la dieta, el estrés o exposiciones ambientales pueden modificar marcadores epigenéticos, alterando la eficacia terapéutica. Esto refuerza el impacto de la epigenética en la respuesta a fármacos como un elemento dinámico y modificable.
4. Terapias epigenéticas y su sinergia con fármacos convencionales
Los inhibidores de DNMT (como azacitidina) o inhibidores de histona deacetilasas (como vorinostat) están siendo utilizados para revertir alteraciones epigenéticas en enfermedades. Su combinación con otros fármacos puede potenciar efectos terapéuticos, evidenciando el impacto de la epigenética en la respuesta a fármacos como una herramienta para terapias combinadas.
5. Biomarcadores epigenéticos en la medicina personalizada
La identificación de biomarcadores epigenéticos permite predecir la respuesta a tratamientos. Por ejemplo, patrones de metilación en genes como MGMT en glioblastomas predicen la eficacia de temozolomida. Este avance subraya el impacto de la epigenética en la respuesta a fármacos y su rol en la medicina de precisión.
| Mecanismo Epigenético | Ejemplo de Fármaco Afectado | Efecto en la Respuesta |
|---|---|---|
| Metilación del ADN | Temozolomida | Mayor eficacia si MGMT está metilado |
| Modificación de Histonas | Vorinostat | Inducción de apoptosis en linfomas |
| Regulación por miRNAs | Imatinib | Resistencia en leucemias |
Preguntas Frecuentes
¿Qué es la epigenética y cómo influye en la respuesta a los fármacos?
La epigenética estudia modificaciones químicas en el ADN y proteínas asociadas que alteran la expresión génica sin cambiar la secuencia genética. Estas modificaciones, como la metilación del ADN o las modificaciones de histonas, pueden afectar cómo los pacientes responden a ciertos fármacos, influyendo en su eficacia o toxicidad.
¿Qué tipos de cambios epigenéticos están vinculados a la farmacorresistencia?
La hipermetilación de genes supresores de tumores o la desregulación de microARNs son ejemplos clave de alteraciones epigenéticas asociadas a resistencia farmacológica. Estos cambios pueden reducir la sensibilidad a tratamientos en enfermedades como el cáncer, dificultando la acción de quimioterapéuticos.
¿Cómo se utiliza la epigenética para personalizar tratamientos médicos?
El análisis de biomarcadores epigenéticos permite identificar patrones únicos en pacientes, facilitando la medicina personalizada. Por ejemplo, detectar patrones de metilación anormal ayuda a seleccionar fármacos más efectivos y reducir efectos adversos, optimizando la terapia dirigida.
¿Pueden los hábitos del paciente modificar su epigenética y afectar la respuesta a los fármacos?
Factores como la dieta, el estrés o la exposición a toxinas ambientales pueden inducir cambios epigenéticos, modificando la respuesta a tratamientos. Por ello, intervenciones en el estilo de vida podrían complementar terapias para mejorar la eficacia de los fármacos.