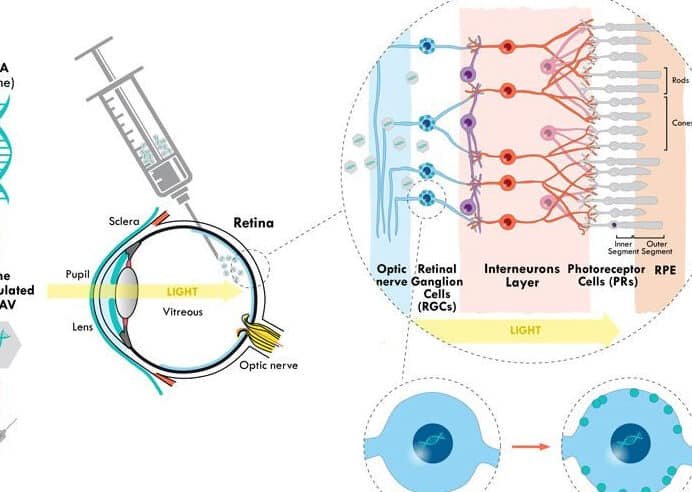
es un tema clave en el ámbito de la innovación médica y la salud pública. Estos tratamientos, que incluyen terapias génicas, celulares y de ingeniería tisular, representan una revolución en la medicina, pero también plantean desafíos normativos complejos. Mientras la Unión Europea cuenta con un marco regulatorio específico bajo el Reglamento (CE) nº 1394/2007, Estados Unidos aborda estas terapias principalmente a través de la FDA, con enfoques flexibles pero rigurosos. Este artículo analiza las diferencias y similitudes entre ambos sistemas, explorando cómo impactan en el desarrollo, aprobación y acceso a estas terapias transformadoras.
La regulación de las terapias avanzadas en Europa y EE.UU.: Un análisis comparativo
La regulación de las terapias avanzadas en Europa y EE.UU. es un tema clave en el desarrollo de medicamentos innovadores, como terapias génicas, celulares y de ingeniería tisular. Ambos mercados tienen marcos regulatorios distintos pero complementarios, diseñados para garantizar la seguridad y eficacia de estos tratamientos revolucionarios.
1. Marco regulatorio en la Unión Europea
En la UE, la regulación de las terapias avanzadas está bajo el Reglamento (EC) N° 1394/2007, que define los Medicamentos de Terapia Avanzada (ATMPs). La EMA (Agencia Europea de Medicamentos) supervisa su evaluación, con un enfoque en riesgos y beneficios. Existen programas como el PRIME para acelerar el desarrollo de terapias prometedoras.
2. Enfoque regulatorio en Estados Unidos
En EE.UU., la FDA (Administración de Alimentos y Medicamentos) regula estas terapias bajo las categorías de productos biológicos y terapias génicas. Se rige por el marco del 21 CFR Part 1271 para productos celulares y tisulares, con vías aceleradas como Breakthrough Therapy para facilitar su aprobación.
3. Procesos de aprobación comparados
Mientras la UE centraliza la aprobación de ATMPs mediante la EMA, EE.UU. utiliza un sistema mixto donde la FDA evalúa caso por caso. Ambos sistemas requieren ensayos clínicos rigurosos, pero difieren en plazos y requisitos post-comercialización.
4. Retos en la armonización global
Uno de los mayores desafíos en la regulación de las terapias avanzadas en Europa y EE.UU. es la falta de estandarización en criterios. Esto afecta especialmente a empresas que buscan aprobaciones simultáneas en ambos mercados, aumentando costos y tiempos de desarrollo.
5. Tendencias futuras y adaptaciones normativas
Ambas regiones están evolucionando sus marcos para terapias más complejas, como edición génica (CRISPR). La UE planea revisar su reglamento en 2024, mientras EE.UU. explora nuevas guías para terapias personalizadas, reflejando la rápida innovación en este campo.
| Aspecto | Unión Europea | EE.UU. |
|---|---|---|
| Organismo regulador | EMA | FDA |
| Marco legal principal | Reglamento (EC) 1394/2007 | 21 CFR Part 1271 |
| Vías aceleradas | PRIME, ATMP classification | Breakthrough Therapy, RMAT |
| Enfoque en ensayos clínicos | Centralizado por EMA | Descentralizado (por institución) |
| Aprobaciones anuales (promedio) | 2-3 ATMPs | 5-7 terapias avanzadas |
Preguntas Frecuentes
¿Qué son las terapias avanzadas reguladas en Europa y EE.UU.?
Las terapias avanzadas incluyen medicamentos innovadores como terapias génicas, celulares y de tejidos, regulados en Europa por el Reglamento (CE) Nº 1394/2007 y en EE.UU. por la FDA bajo categorías específicas como terapias génicas y celulares. Ambos marcos buscan garantizar su seguridad, eficacia y calidad.
¿Cuál es el proceso de aprobación para estas terapias en Europa y EE.UU.?
En Europa, la EMA evalúa las terapias avanzadas mediante un comité especializado (CAT), mientras que en EE.UU., la FDA utiliza vías aceleradas como la designación de terapia innovadora. Ambos procesos requieren ensayos clínicos rigurosos y revisión de datos preclínicos antes de su autorización.
¿Qué diferencias clave existen entre las regulaciones europeas y estadounidenses?
La principal diferencia radica en el enfoque: la UE tiene un Reglamento específico para terapias avanzadas, mientras que EE.UU. las integra en marcos existentes. Además, la EMA suele requerir más datos post-comercialización, mientras que la FDA tiende a priorizar vías aceleradas para productos prometedores.
¿Cómo se garantiza la seguridad de los pacientes en estas terapias?
Ambas regiones exigen evaluaciones exhaustivas de riesgo-beneficio, farmacovigilancia activa y, en algunos casos, planes de gestión de riesgos. En Europa, se aplica un seguimiento adicional debido a la naturaleza innovadora, mientras que en EE.UU., la monitorización post-aprobación es clave para terapias con designación acelerada.