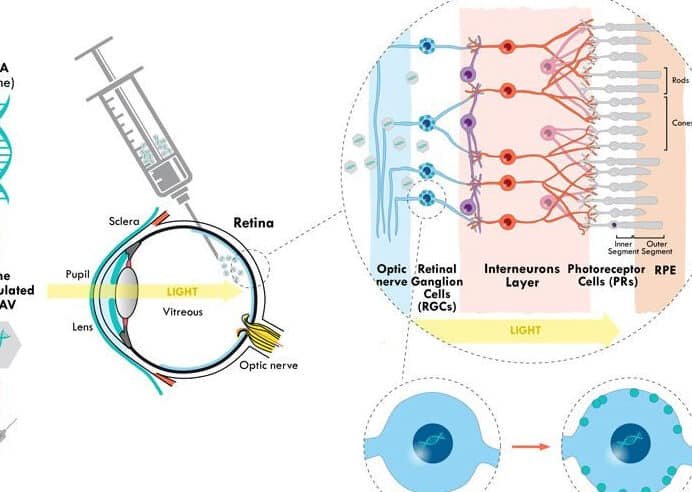
La representa una revolución en el campo de la genética y la biología molecular. A diferencia de las modificaciones directas en la secuencia del ADN, esta técnica permite regular la actividad de los genes alterando su entorno químico. Factores como la metilación del ADN o las modificaciones en las histonas actúan como interruptores moleculares, activando o silenciando genes sin alterar su código subyacente. Este enfoque abre nuevas puertas para entender enfermedades complejas y desarrollar terapias precisas, ofreciendo un potencial terapéutico sin los riesgos asociados a la manipulación genética tradicional.
Edición epigenética: Una revolución en la regulación génica
La Edición epigenética: Cambiar la expresión sin cambiar el ADN representa un avance crucial en la biología molecular al permitir modular la actividad de los genes sin alterar su secuencia genética. Esta técnica se centra en modificar marcas químicas, como metilaciones o acetilaciones, que influyen en cómo se lee el ADN. A diferencia de la edición genética tradicional (ej. CRISPR-Cas9), la epigenética ofrece un enfoque reversible y adaptable, con aplicaciones en medicina, agricultura e investigación biomédica.
¿Qué es la Edición epigenética?
La Edición epigenética se refiere a la modificación dirigida de marcas químicas en el ADN o histonas (proteínas asociadas al ADN) para activar o silenciar genes. Estas marcas incluyen metilación del ADN (añadir grupos metilo) o modificaciones en histonas (acetilación, fosforilación). A diferencia de mutaciones genéticas, estos cambios no afectan la secuencia de bases del ADN, pero alteran su accesibilidad para la maquinaria transcripcional. Un ejemplo es el uso de herramientas como CRISPR-dCas9 acoplado a enzimas epigenéticas (ej. DNMT3A para metilación).
Aplicaciones médicas de la Edición epigenética
En medicina, la Edición epigenética: Cambiar la expresión sin cambiar el ADN se investiga para tratar enfermedades crónicas y cáncer. Por ejemplo, en tumores, se pueden silenciar oncogenes o reactivar genes supresores mediante desmetilación. También se explora en enfermedades neurodegenerativas (Alzheimer) y autoinmunes. Su reversibilidad la hace atractiva para terapias precisas, reduciendo riesgos de efectos secundarios permanentes.
Diferencias entre edición genética y epigenética
Mientras la edición genética (como CRISPR tradicional) corta el ADN para insertar, eliminar o corregir secuencias, la Edición epigenética modifica su expresión sin alterar su estructura. La primera es permanente y puede generar mutaciones no deseadas; la segunda es reversible y ajustable. Por ejemplo, silenciar un gen con metilación puede revertirse con fármacos inhibidores de DNMT, mientras que una deleción génica es irreversible.
Técnicas clave en Edición epigenética
Las herramientas más usadas incluyen:
- CRISPR-dCas9: Versión inactiva de Cas9 fusionada con enzimas epigenéticas (ej. p300 para acetilación).
- Zinc Finger Proteins (ZFPs) y TALEs: Diseñados para dirigirse a secuencias específicas.
- Inhibidores de histona deacetilasas (HDAC): Para aumentar la expresión génica.
Retos y limitaciones actuales
Aunque prometedora, la Edición epigenética: Cambiar la expresión sin cambiar el ADN enfrenta desafíos como la especificidad (evitar efectos off-target), la estabilidad de las modificaciones y la entrega eficiente de herramientas a células target. Además, su reversibilidad, aunque ventajosa, requiere control preciso para evitar cambios no deseados en el perfil epigenético celular.
| Técnica | Objetivo | Ventaja |
|---|---|---|
| CRISPR-dCas9 + p300 | Acetilación de histonas | Activa genes promotores |
| CRISPR-dCas9 + DNMT3A | Metilación del ADN | Silencia genes específicos |
| TALEs-HDAC | Desacetilación de histonas | Reduce expresión génica |
Guía completa sobre Edición epigenética: Cambiar la expresión sin cambiar el ADN
¿Qué mecanismos epigenéticos permiten regular la expresión génica sin modificar la secuencia del ADN?
Los mecanismos epigenéticos que regulan la expresión génica sin alterar la secuencia del ADN incluyen la metilación del ADN, que silencia genes al agregar grupos metilo a las citosinas; las modificaciones de histonas, como acetilación o metilación, que afectan la compactación de la cromatina; y los ARN no codificantes, como los microARNs, que interfieren con la traducción o estabilidad del ARN mensajero. Estos procesos permiten una regulación dinámica de la actividad génica en respuesta a factores ambientales o del desarrollo, destacando el concepto de edición epigenética: cambiar la expresión sin cambiar el ADN.
Metilación del ADN y su papel en el silenciamiento génico
La metilación del ADN es un mecanismo clave en la regulación epigenética, donde la adición de grupos metilo a las citosinas en regiones promotoras suele silenciar genes. Este proceso es esencial en el desarrollo embrionario, la impronta genómica y la inhibición de elementos transponibles. La metilación anormal está asociada a enfermedades como el cáncer, donde genes supresores de tumores pueden ser hipermetilados. La edición epigenética: cambiar la expresión sin cambiar el ADN se logra mediante enzimas como las ADN metiltransferasas (DNMTs).
| Proceso | Función | Enzimas Involucradas |
|---|---|---|
| Metilación de Citosina | Silenciamiento génico | DNMT1, DNMT3A/B |
| Desmetilación | Activación génica | TET1/2/3 |
Modificaciones de histonas y su impacto en la cromatina
Las modificaciones postraduccionales de histonas, como la acetilación o metilación, alteran la estructura de la cromatina, facilitando o inhibiendo el acceso de la maquinaria transcripcional. La acetilación, mediada por histona acetiltransferasas (HATs), generalmente activa genes al relajar la cromatina, mientras que la desacetilación (por HDACs) promueve el silenciamiento. Estas modificaciones son reversibles y dinámicas, reflejando la plasticidad de la edición epigenética: cambiar la expresión sin cambiar el ADN.
ARN no codificantes en la regulación génica postranscripcional
Los ARN no codificantes, como microARNs (miRNAs) y ARN largos no codificantes (lncRNAs), regulan la expresión génica al unirse a ARN mensajeros (ARNm) para degradarlos o bloquear su traducción. Los miRNAs, por ejemplo, son cruciales en procesos como la diferenciación celular y la respuesta al estrés. Su desregulación se vincula a patologías neurodegenerativas y cáncer. Este nivel de control ejemplifica la edición epigenética: cambiar la expresión sin cambiar el ADN, ofreciendo blancos terapéuticos potenciales.
¿Existe evidencia de que las marcas epigenéticas puedan transmitirse a generaciones posteriores?
Sí, existe evidencia científica de que las marcas epigenéticas pueden transmitirse a generaciones posteriores, fenómeno conocido como herencia epigenética transgeneracional. Estudios en modelos animales, como roedores, han demostrado que cambios en la metilación del ADN o modificaciones en las histonas inducidos por factores ambientales, como la dieta o el estrés, pueden heredarse en la descendencia e influir en la expresión génica. En humanos, investigaciones observacionales sugieren que exposiciones traumáticas o nutricionales en generaciones anteriores pueden dejar huellas epigenéticas en generaciones futuras, aunque los mecanismos exactos siguen bajo investigación. La Edición epigenética: Cambiar la expresión sin cambiar el ADN ha ampliado el entendimiento de cómo estas marcas regulan genes sin alterar la secuencia genética subyacente.
Mecanismos de herencia epigenética transgeneracional
La herencia epigenética transgeneracional ocurre cuando las marcas químicas, como la metilación del ADN o las modificaciones de histonas, evaden el borrado durante la formación de gametos y la fertilización, transmitiéndose a la siguiente generación. Estos mecanismos son clave en la regulación de genes y pueden ser influenciados por factores ambientales, como toxinas o estrés nutricional. Aunque este proceso está bien documentado en organismos modelo, su confirmación en humanos requiere más investigación para entender su impacto a largo plazo.
Impacto ambiental en la epigenética heredable
Factores ambientales, como la exposición a químicos, una dieta desequilibrada o el estrés crónico, pueden inducir cambios epigenéticos que afectan a múltiples generaciones. Por ejemplo, estudios en roedores muestran que la exposición a pesticidas altera la metilación del ADN en espermatozoides, afectando la salud de la descendencia. En humanos, eventos históricos como hambrunas han dejado marcas epigenéticas detectables en generaciones posteriores, destacando cómo el ambiente moldea la expresión génica sin modificar el código genético.
Avances en la investigación de la herencia epigenética
Los avances tecnológicos, como la secuenciación de epigenomas completos, han permitido identificar patrones de herencia epigenética con mayor precisión. La Edición epigenética: Cambiar la expresión sin cambiar el ADN es una herramienta prometedora para estudiar estos fenómenos, permitiendo manipular marcas químicas específicas y observar sus efectos transgeneracionales. Sin embargo, persisten desafíos, como distinguir entre cambios epigenéticos heredados y aquellos inducidos postnatally.
| Factor ambiental | Efecto epigenético | Generaciones afectadas |
|---|---|---|
| Dieta alta en grasas | Alteración en metilación de genes metabólicos | Hasta 2 generaciones |
| Exposición a pesticidas | Cambios en histonas asociadas a desarrollo | 3 generaciones (en estudios con roedores) |
| Trauma psicológico | Metilación alterada en genes de respuesta al estrés | 2 generaciones (evidencia limitada en humanos) |
¿Qué procesos bioquímicos, como la metilación del ADN o las modificaciones de histonas, inducen cambios epigenéticos que regulan la expresión génica?
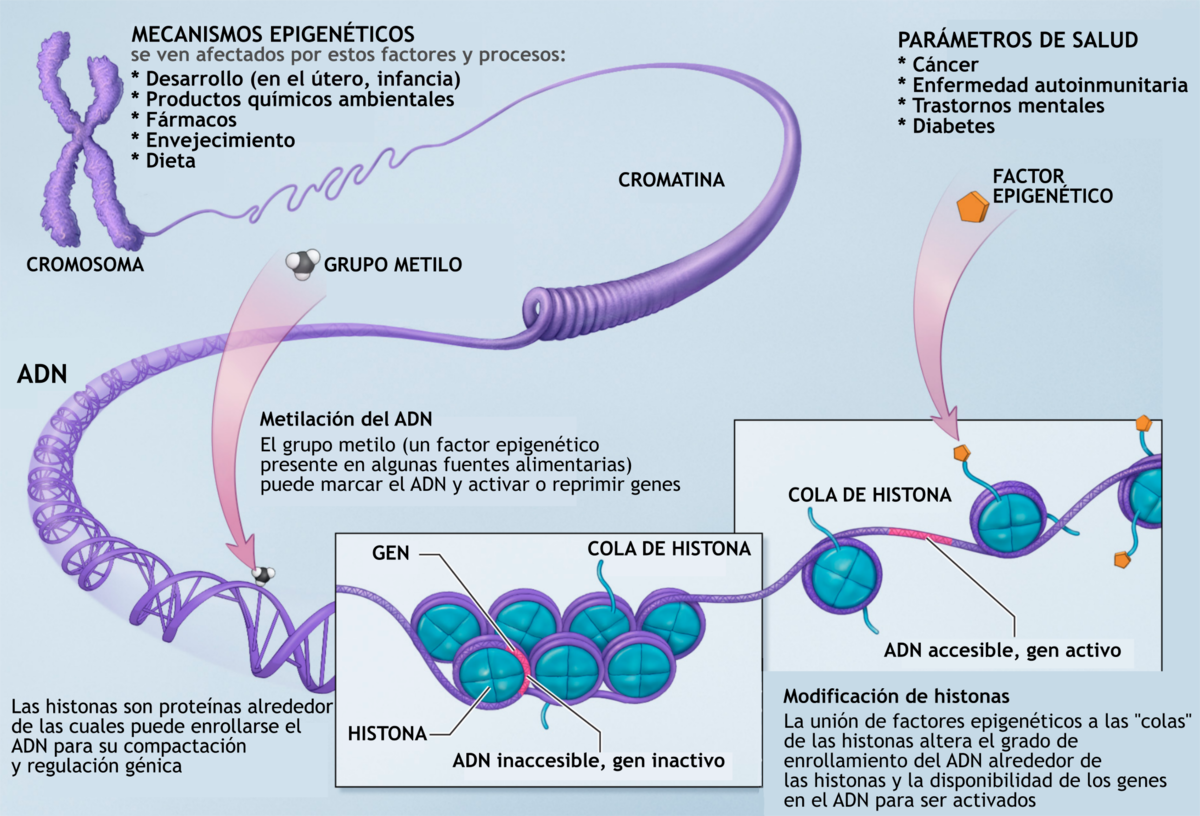
Los procesos bioquímicos que inducen cambios epigenéticos incluyen la metilación del ADN, donde grupos metilo se unen a citosinas en regiones promotoras, silenciando genes, y las modificaciones de histonas, como acetilación, metilación o fosforilación, que alteran la estructura de la cromatina para activar o reprimir la expresión génica. Además, los ARN no codificantes regulan la estabilidad y traducción del ARNm, mientras que los complejos remodeladores de cromatina reposicionan nucleosomas para facilitar o impedir el acceso de la maquinaria transcripcional. Estos mecanismos ejemplifican la edición epigenética: cambiar la expresión sin cambiar el ADN, permitiendo respuestas adaptativas a señales ambientales.
Metilación del ADN y su impacto en la expresión génica
La metilación del ADN es un proceso clave en la regulación epigenética, donde la adición de grupos metilo en las citosinas de las secuencias CpG en promotores suele reprimir la transcripción. Esta modificación atrae proteínas como las proteínas de unión a metil-CpG (MeCP2), que reclutan complejos represores para compactar la cromatina. En enfermedades como el cáncer, patrones aberrantes de metilación pueden silenciar genes supresores de tumores o activar oncogenes. La edición epigenética: cambiar la expresión sin cambiar el ADN es evidente aquí, ya que la metilación puede revertirse sin alterar la secuencia genómica.
| Proceso | Efecto | Ejemplo |
|---|---|---|
| Metilación de promotores | Silenciamiento génico | Genes supresores de tumores en cáncer |
| Hipometilación global | Inestabilidad genómica | Activación de retrotransposones |
Modificaciones de histonas y regulación de la cromatina
Las modificaciones de histonas, como la acetilación (activadora) o metilación (activadora/represora), alteran la accesibilidad del ADN. La acetilación neutraliza las cargas positivas de las histonas, reduciendo su afinidad por el ADN y facilitando la transcripción. En contraste, la metilación de lisinas como H3K27me3 (por el complejo PRC2) promueve el silenciamiento génico. Estos cambios dinámicos ilustran cómo la edición epigenética: cambiar la expresión sin cambiar el ADN influye en procesos como el desarrollo embrionario o la memoria celular.
ARN no codificantes y su rol en la regulación epigenética
Los ARN no codificantes, como microARNs (miARNs) y ARNs largos no codificantes (lncARNs), modulan la expresión génica post-transcripcionalmente o guiando complejos epigenéticos a loci específicos. Por ejemplo, los lncARNs pueden reclutar la proteína Polycomb para silenciar genes, mientras que los miARNs degradan ARNm diana. Este nivel de regulación refuerza el concepto de edición epigenética: cambiar la expresión sin cambiar el ADN, destacando su papel en enfermedades neurodegenerativas y cáncer.
¿Cómo influyen factores ambientales, como la dieta o el estrés, en la modulación epigenética de la expresión génica?
Los factores ambientales, como la dieta o el estrés, ejercen una influencia directa en la modulación epigenética de la expresión génica mediante mecanismos como la metilación del ADN, modificaciones en las histonas y la acción de ARN no codificantes. Por ejemplo, una dieta rica en nutrientes como folato o metionina puede alterar los patrones de metilación, mientras que el estrés crónico activa vías como el eje hipotálamo-hipófisis-adrenal, modificando la expresión de genes relacionados con la respuesta inflamatoria o neuronal. Estas modificaciones no alteran la secuencia del ADN, pero sí su accesibilidad y función, destacando el concepto de Edición epigenética: Cambiar la expresión sin cambiar el ADN, lo que permite una adaptación rápida al entorno sin mutaciones genéticas.
Impacto de la dieta en la modulación epigenética
La dieta es uno de los factores ambientales más estudiados en la modulación epigenética, ya que componentes como vitaminas B, ácidos grasos omega-3 y polifenoles influyen en mecanismos como la metilación del ADN y la acetilación de histonas. Por ejemplo, el folato, presente en vegetales verdes, actúa como donante de grupos metilo, esenciales para marcas epigenéticas que regulan genes implicados en el metabolismo o la proliferación celular. La Edición epigenética: Cambiar la expresión sin cambiar el ADN es evidente en estudios donde dietas altas en grasas saturadas alteran la expresión de genes asociados a la obesidad sin modificar su secuencia genética.
| Nutriente | Mecanismo Epigenético | Genes Afectados |
|---|---|---|
| Folato | Metilación del ADN | Genes de reparación celular |
| Resveratrol | Acetilación de histonas | Genes antienvejecimiento |
Efectos del estrés crónico en la epigenética
El estrés crónico desencadena cambios epigenéticos profundos, particularmente en genes relacionados con la respuesta inflamatoria y la plasticidad neuronal. La liberación prolongada de cortisol altera la metilación en promotores de genes como el _BDNF_, afectando la memoria y el estado de ánimo. Además, estudios demuestran que el estrés prenatal puede inducir marcas epigenéticas heredables, ilustrando cómo la Edición epigenética: Cambiar la expresión sin cambiar el ADN puede tener consecuencias transgeneracionales.
Interacción entre ambiente y epigenética en enfermedades
La interacción entre factores ambientales y modulación epigenética es clave en enfermedades como el cáncer, la diabetes o trastornos neurológicos. Por ejemplo, la exposición a toxinas ambientales como el humo del tabaco puede hipermetilar genes supresores de tumores, mientras que el ejercicio físico promueve modificaciones en histonas que activan genes metabólicos. Este enfoque resalta la Edición epigenética: Cambiar la expresión sin cambiar el ADN como un puente entre el entorno y la predisposición genética a patologías.
Preguntas Frecuentes
¿Qué es la edición epigenética y cómo funciona?
La edición epigenética es una técnica que permite modificar la expresión génica sin alterar la secuencia del ADN. Se enfoca en cambios químicos, como la metilación o modificaciones en las histonas, que actúan como interruptores para activar o silenciar genes específicos, influyendo en procesos biológicos como el desarrollo o enfermedades.
¿Cuál es la diferencia entre edición genética y epigenética?
Mientras la edición genética (como CRISPR) modifica directamente la secuencia del ADN, la edición epigenética altera su expresión mediante marcas químicas. Estas modificaciones son reversibles y no cambian el código genético subyacente, lo que reduce riesgos como mutaciones no deseadas.
¿Qué aplicaciones tiene la edición epigenética en medicina?
Esta tecnología promete tratar enfermedades complejas como el cáncer, trastornos neurológicos o metabólicos, al regular genes desequilibrados. También se investiga en terapias regenerativas y en revertir efectos de envejecimiento celular, ofreciendo opciones menos invasivas que las terapias génicas tradicionales.
¿Existen riesgos o limitaciones en la edición epigenética?
Aunque es menos invasiva, la edición epigenética puede tener efectos off-target, alterando genes no deseados. Además, las modificaciones pueden ser transitorias, requiriendo aplicaciones repetidas. Su uso clínico aún está en fase experimental, necesitando más estudios para garantizar seguridad y eficacia.