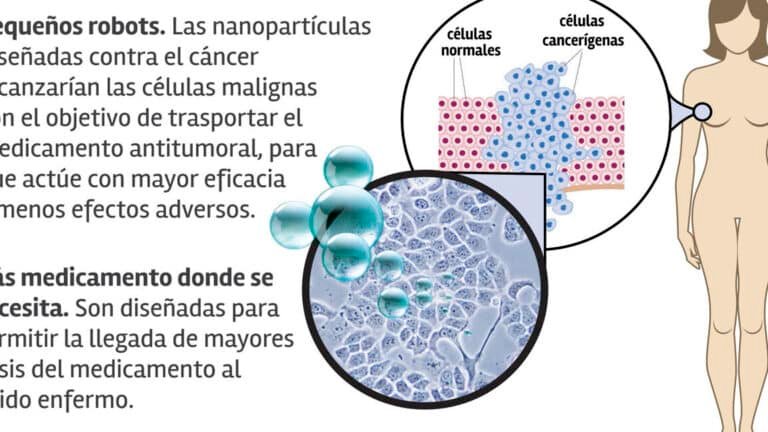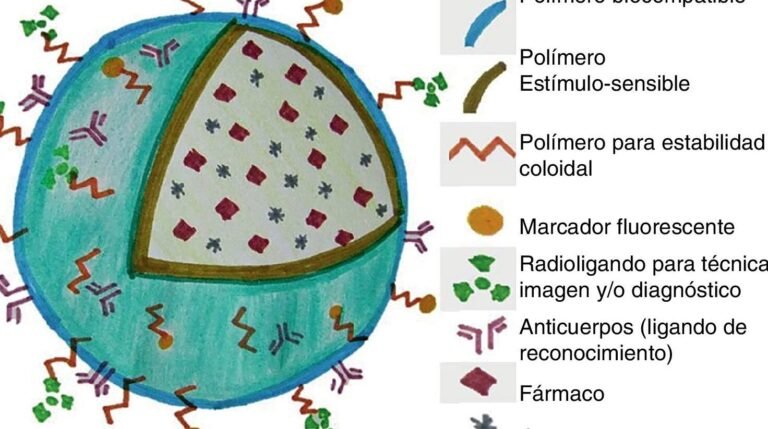
La representa un avance innovador en el tratamiento del cáncer, superando uno de los principales desafíos en la administración de medicamentos: la baja solubilidad. Muchos compuestos antitumorales presentan limitaciones en su biodisponibilidad debido a su pobre disolución en medios acuosos. Mediante el uso de nanosistemas, como liposomas, nanopartículas poliméricas o micelas, es posible encapsular estos fármacos, incrementando su solubilidad y estabilidad. Esta aproximación no solo optimiza la eficacia terapéutica, sino que también reduce efectos secundarios, abriendo nuevas posibilidades en oncología personalizada. La integración de la nanotecnología marca así un hito en el desarrollo de terapias más precisas y efectivas.
Aportes de la Nanotecnología para mejorar la solubilidad de fármacos oncológicos
La Nanotecnología para mejorar la solubilidad de fármacos oncológicos ha revolucionado el desarrollo de terapias contra el cáncer. Al manipular materiales a escala nanométrica, se logra incrementar la solubilidad y biodisponibilidad de compuestos antitumorales, optimizando su eficacia y reduciendo efectos secundarios. Esta tecnología permite diseñar sistemas de liberación controlada, como liposomas o nanopartículas poliméricas, que favorecen la estabilidad y penetración celular de fármacos poco solubles.
1. ¿Cómo incrementa la nanomedicina la solubilidad de los fármacos oncológicos?
La Nanotecnología para mejorar la solubilidad de fármacos oncológicos emplea vehículos nanométricos, como micelas o dendrímeros, que encapsulan principios activos hidrofóbicos. Estos sistemas modifican las propiedades fisicoquímicas del fármaco, aumentando su dispersión en medios acuosos y facilitando su absorción. Además, evitan la degradación prematura y mejoran la selectividad hacia células tumorales.
2. Nanomateriales más utilizados en la solubilización de medicamentos contra el cáncer
Entre los materiales destacan nanopartículas lipídicas, nanocristales y polímeros biocompatibles. Cada uno ofrece ventajas únicas: las lipídicas mejoran la permeabilidad, mientras que los nanocristales incrementan el área superficial. La elección depende del fármaco y la vía de administración.
3. Beneficios clínicos de aplicar nanotecnología en oncología
La implementación de Nanotecnología para mejorar la solubilidad de fármacos oncológicos reduce toxicidad sistémica, permite dosis menores y aumenta la concentración del fármaco en tejidos malignos. Esto se traduce en mayores tasas de respuesta terapéutica y menor resistencia a tratamientos.
4. Casos de éxito: fármacos oncológicos reformulados con nanotecnología
Ejemplos incluyen el paclitaxel nanoformulado (Abraxane®), que supera la baja solubilidad del principio activo original. Este avance demostró mayor eficacia en cáncer de mama y páncreas, validando el potencial de la nanotecnología en oncología.
5. Desafíos futuros y limitaciones técnicas
A pesar de los progresos, persisten retos como la escalabilidad industrial, la reproducibilidad de nanosistemas y estudios a largo plazo sobre biodistribución. La estandarización de protocolos es clave para consolidar esta tecnología.
| Nanomaterial | Ventaja principal | Ejemplo de fármaco |
| Liposomas | Alta biocompatibilidad | Doxorrubicina (Doxil®) |
| Nanopartículas poliméricas | Liberación controlada | Docetaxel (Nanotheryx®) |
| Micelas | Solubilización de hidrofóbicos | Paclitaxel (Genexol-PM®) |
Preguntas Frecuentes
¿Cómo mejora la nanotecnología la solubilidad de fármacos oncológicos?
La nanotecnología emplea sistemas como nanopartículas o liposomas para encapsular fármacos oncológicos, aumentando su solubilidad en medios acuosos. Esto optimiza su absorción y biodisponibilidad, mejorando la eficacia del tratamiento.
¿Qué ventajas ofrece la nanotecnología frente a métodos tradicionales?
Permite superar limitaciones como la baja solubilidad y la degradación prematura de los fármacos. Además, facilita la liberación controlada y el targeting selectivo hacia células cancerosas, reduciendo efectos secundarios.
¿Qué tipos de nanosistemas se utilizan en estos tratamientos?
Los más comunes son nanocápsulas, micelas poliméricas y nanoportadores lipídicos. Cada uno se diseña según las propiedades del fármaco para garantizar estabilidad y liberación controlada.
¿Existen desafíos en la aplicación clínica de estas nanotecnologías?
Sí, entre los principales están la escalabilidad de producción, la toxicidad potencial de algunos materiales y la necesidad de más ensayos clínicos para validar su seguridad y eficacia a largo plazo.