La representa un avance revolucionario en el tratamiento de enfermedades genéticas raras. Esta innovadora técnica consiste en la modificación de células del paciente fuera de su cuerpo, corrigiendo defectos genéticos antes de reinfundirlas. Dirigida especialmente a pacientes con inmunodeficiencia combinada severa (SCID), conocida como niños burbuja, la terapia ofrece una alternativa prometedora cuando no hay donante compatible para trasplante de médula ósea. Al insertar genes funcionales en las células hematopoyéticas, se restaura la capacidad inmunológica, reduciendo riesgos y mejorando la calidad de vida. Este enfoque marca un hito en la medicina personalizada.
Terapia génica ex vivo para la inmunodeficiencia combinada severa: Avances y aplicaciones
1. ¿Qué es la inmunodeficiencia combinada severa?
La inmunodeficiencia combinada severa (SCID) es un grupo de trastornos genéticos raros que afectan gravemente el sistema inmunológico, dejando a los pacientes vulnerables a infecciones potencialmente mortales. La Terapia génica ex vivo para la inmunodeficiencia combinada severa representa una alternativa innovadora al trasplante de médula ósea, especialmente cuando no hay donantes compatibles disponibles.
2. ¿En qué consiste la Terapia génica ex vivo?
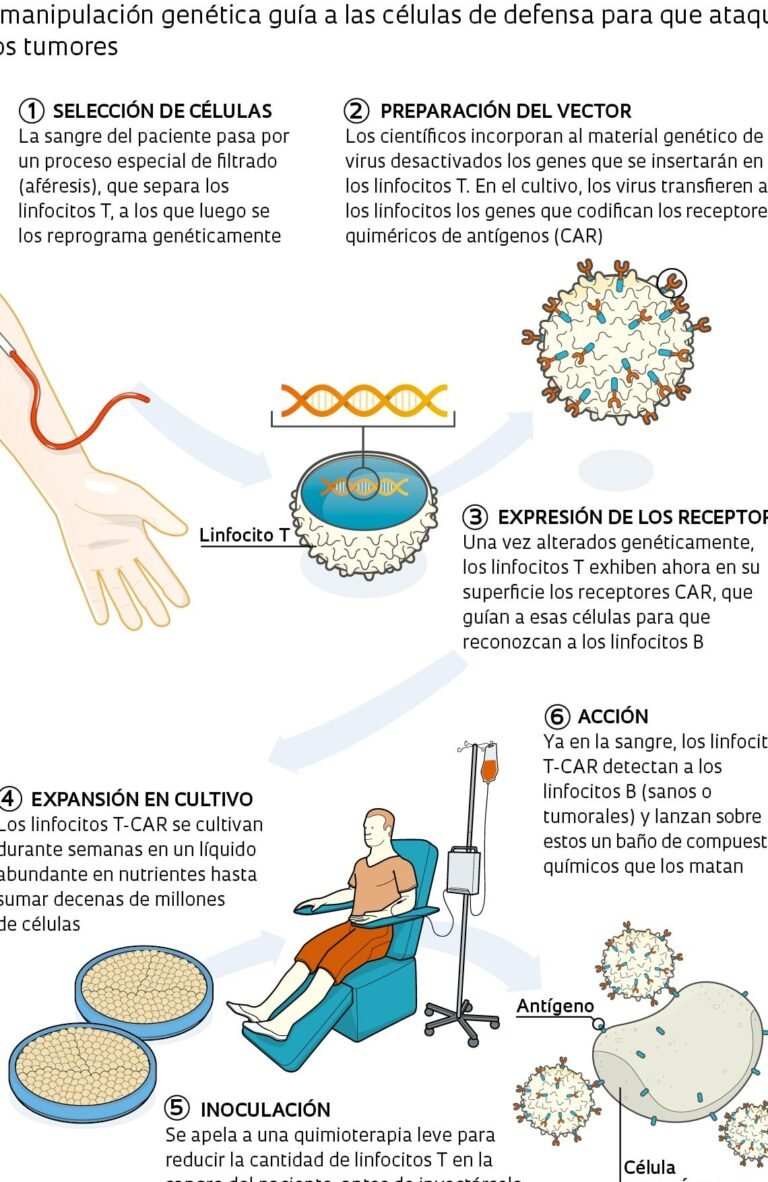
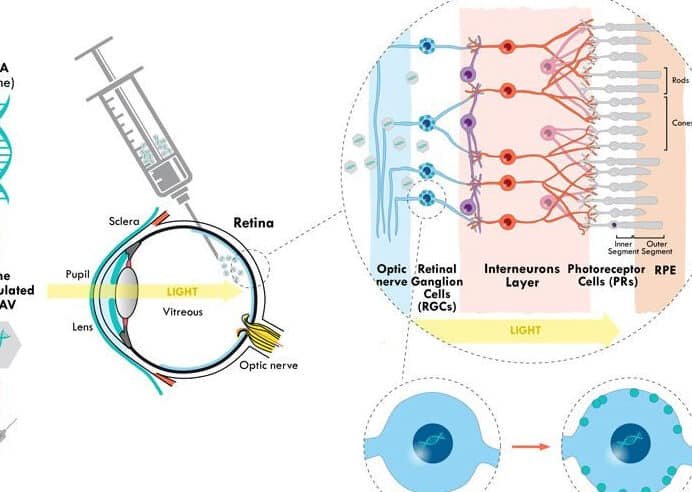
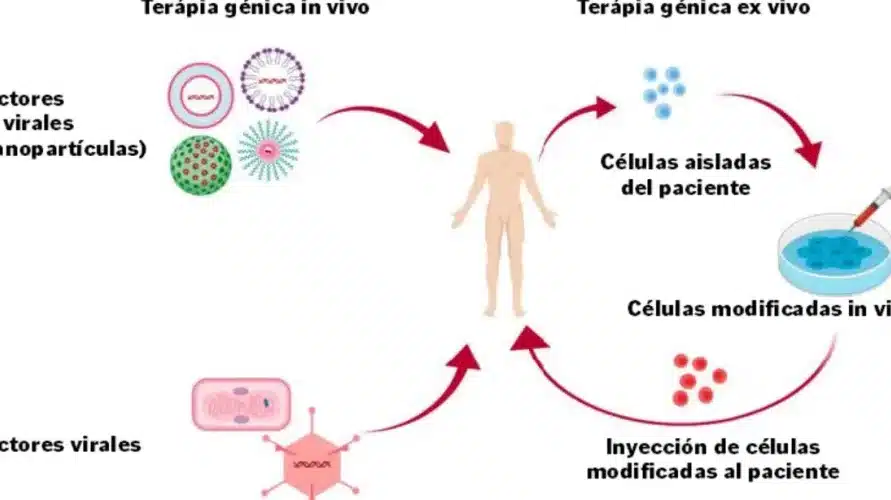
La Terapia génica ex vivo implica la extracción de células madre hematopoyéticas del paciente, su modificación genética en el laboratorio para corregir el defecto y su posterior reinfusión. Esta técnica evita los riesgos de rechazo asociados con los trasplantes convencionales y ha demostrado eficacia en ensayos clínicos para tratar la inmunodeficiencia combinada severa.
3. Beneficios de la Terapia génica ex vivo en SCID
Entre los principales beneficios destacan: – Personalización: Utiliza las propias células del paciente. – Reducción de complicaciones: Minimiza el riesgo de enfermedad injerto contra huésped. – Recuperación inmunológica: Restaura la función de linfocitos T y B en la mayoría de los casos.
4. Desafíos y limitaciones actuales
A pesar de su potencial, la Terapia génica ex vivo para la inmunodeficiencia combinada severa enfrenta desafíos como: – Altos costos de desarrollo y aplicación. – Posibilidad de mutagenesis insercional (activación accidental de oncogenes). – Disponibilidad limitada en centros médicos especializados.
5. Futuro de la Terapia génica ex vivo en SCID
La investigación se centra en mejorar vectores virales para mayor seguridad, ampliar el acceso a poblaciones subatendidas y combinar esta terapia con otras estrategias de edición genética, como CRISPR/Cas9.
| Aspecto clave | Detalle |
| Tipo de células modificadas | Células madre hematopoyéticas CD34+ |
| Vector utilizado | Virus lentiviral o retroviral |
| Tasa de éxito clínico | Superior al 80% en formas comunes de SCID |
| Duración del efecto | Resultados sostenidos por más de 10 años |
Preguntas Frecuentes
¿Qué es la terapia génica ex vivo para la inmunodeficiencia combinada severa (SCID)?
La terapia génica ex vivo para la inmunodeficiencia combinada severa (SCID) es un tratamiento innovador que consiste en extraer células madre hematopoyéticas del paciente, corregir el defecto genético en un laboratorio y luego reinsertarlas en el cuerpo para restaurar la función inmunológica.
¿Cuáles son los beneficios de la terapia génica ex vivo en pacientes con SCID?
Este abordaje ofrece ventajas como la reducción de riesgos asociados a trasplantes de donantes, la corrección permanente del defecto genético y la posibilidad de evitar complicaciones graves derivadas de la falta de inmunidad en estos pacientes.
¿Existen riesgos asociados a la terapia génica ex vivo para SCID?
Aunque es un tratamiento prometedor, existen riesgos potenciales como el desarrollo de efectos secundarios hematológicos, la activación accidental de oncogenes durante la modificación genética o respuestas inmunitarias no deseadas tras la reinserción celular.
¿Cómo se compara la terapia génica ex vivo con otras opciones para SCID, como el trasplante de médula ósea?
La terapia génica ex vivo evita la necesidad de encontrar un donante compatible, reduciendo el riesgo de enfermedad injerto contra huésped, pero su eficacia a largo plazo aún se estudia en comparación con el trasplante de médula ósea, considerado el estándar actual en muchos casos.