Introducción
La investigación oncológica ha avanzado significativamente gracias a la innovación en bioingeniería, permitiendo desarrollar herramientas más precisas para el estudio del cáncer. Uno de los avances más relevantes es comprender cómo la bioingeniería crea modelos de tumores para probar fármacos, replicando las características biológicas y genéticas de los tejidos malignos en entornos controlados. Estos modelos, que incluyen cultivos celulares en 3D y órganos en chips, ofrecen una plataforma eficiente para evaluar la eficacia y toxicidad de nuevos tratamientos. Al imitar la complejidad de los tumores humanos, la bioingeniería optimiza el proceso de desarrollo de medicamentos, reduciendo costos y tiempos en la búsqueda de terapias más efectivas.
El papel de la bioingeniería en el desarrollo de modelos tumorales para ensayos farmacológicos
La bioingeniería ha revolucionado la investigación oncológica mediante la creación de modelos de tumores que imitan las características de los cánceres humanos. Estos modelos permiten probar fármacos de manera más precisa y ética antes de pasar a ensayos clínicos. Utilizando técnicas como la impresión 3D, cultivos celulares avanzados y organoides, los científicos pueden replicar microambientes tumorales para evaluar respuestas terapéuticas.
1. Técnicas de biofabricación en la creación de modelos tumorales
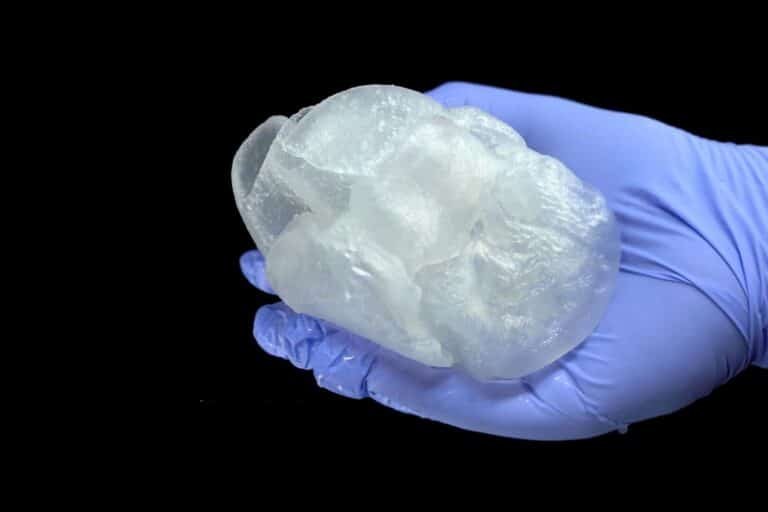
La bioingeniería emplea métodos como la bioimpresión 3D y cultivos en hidrogeles para construir estructuras que simulan la matriz extracelular de los tumores. Estos modelos conservan la heterogeneidad celular y las propiedades mecánicas del tejido original, esenciales para estudiar cómo los fármacos penetran y afectan al tumor.
2. Organoides tumorales: réplicas miniaturizadas de cánceres humanos
Los organoides derivados de pacientes ofrecen una plataforma personalizada para probar terapias. Estos modelos, generados mediante bioingeniería, capturan la genética y morfología del tumor original, permitiendo ensayos con alto valor predictivo para la eficacia de fármacos.
3. Ventajas de los modelos bioingenierizados frente a métodos tradicionales
A diferencia de los cultivos 2D o los modelos animales, los sistemas creados por bioingeniería reproducen la complejidad del microambiente tumoral, incluyendo factores como la hipoxia o la interacción con células inmunitarias. Esto mejora la precisión al evaluar cómo los fármacos interactúan con el tumor.
4. Aplicaciones en medicina personalizada
Estos modelos permiten probar combinaciones de fármacos en tumores específicos, optimizando tratamientos para pacientes individuales. La bioingeniería facilita así la transición hacia terapias dirigidas y reduce la dependencia de ensayos clínicos tradicionales.
5. Retos y futuras direcciones en la bioingeniería de tumores
A pesar de su potencial, persisten desafíos como la estandarización de protocolos y la escalabilidad. Innovaciones en bioingeniería, como la incorporación de inteligencia artificial, prometen mejorar la generación de modelos de tumores para acelerar el descubrimiento de fármacos.
| Técnica | Ventaja clave | Ejemplo de aplicación |
|---|---|---|
| Bioimpresión 3D | Precisión espacial en la arquitectura tumoral | Modelado de metástasis óseas |
| Organoides | Personalización con células del paciente | Pruebas de sensibilidad a quimioterápicos |
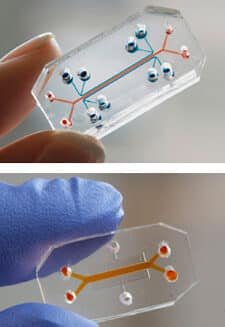
| Chips microfluídicos | Simulación de flujo vascular | Estudios de entrega de fármacos |
Preguntas Frecuentes
¿Qué técnicas de bioingeniería se utilizan para crear modelos tumorales?
La bioingeniería emplea técnicas avanzadas como la impresión 3D de tejidos, cultivos celulares en 3D y sistemas de microfluídica para recrear la estructura y microambiente de los tumores. Estos métodos permiten replicar las características biológicas de los tumores humanos, facilitando pruebas más precisas de fármacos.
¿Por qué los modelos bioingenierizados son más efectivos que los cultivos tradicionales?
Los modelos bioingenierizados imitan la complejidad tumoral al incluir múltiples tipos celulares, matriz extracelular y condiciones de flujo, lo que supera las limitaciones de los cultivos 2D. Esto proporciona datos más realistas y predictivos sobre la respuesta a los fármacos en pacientes.
¿Cómo se validan estos modelos de tumores para asegurar su precisión?
La validación implica comparar los resultados de los modelos con datos clínicos reales, utilizando biomarcadores, imágenes avanzadas y análisis genómicos. Además, se verifica la reproducibilidad y la capacidad de predecir respuestas terapéuticas en estudios preclínicos.
¿Qué ventajas ofrecen estos modelos en el desarrollo de nuevos fármacos?
Estos modelos aceleran el descubrimiento de fármacos al reducir costos y tiempo, permitiendo evaluar la eficacia y toxicidad en condiciones más humanizadas. También minimizan el uso de modelos animales, alineándose con enfoques más éticos y precisos.