La farmacogenómica ha revolucionado el campo de la medicina personalizada, permitiendo ajustar tratamientos según la predisposición genética de cada paciente. es esencial para médicos y profesionales de la salud, ya que estos documentos contienen información clave sobre cómo los genes influyen en la respuesta a fármacos. Este artículo ofrece una guía clara y concisa para entender los componentes fundamentales de estos informes, desde las variantes genéticas relevantes hasta las recomendaciones terapéuticas basadas en evidencia. Conocer su estructura y significado facilita una toma de decisiones más precisa y segura, optimizando los resultados clínicos.
Cómo interpretar un informe farmacogenómico básico
1. Entendiendo la estructura del informe farmacogenómico básico
Un informe farmacogenómico básico suele dividirse en secciones clave: información del paciente, variantes genéticas analizadas, fármacos evaluados y recomendaciones terapéuticas. La sección de variantes genéticas es fundamental, ya que detalle las mutaciones relevantes que afectan la metabolización de medicamentos. Cada gen analizado se asocia con enzimas específicas (como CYP2D6 o CYP2C19), lo que permite predecir la respuesta a ciertos tratamientos.
2. Identificación de genotipos y su impacto clínico
El informe incluirá el genotipo del paciente para cada gen analizado (ej. 1/1, 1/2). Estos resultados indican si el metabolismo del fármaco será normal, lento o rápido. Por ejemplo, un paciente con genotipo CYP2C19 2/2 tendrá un metabolismo lento de fármacos como clopidogrel, lo que puede requerir ajustes de dosis o medicamentos alternativos.
3. Interpretación de fenotipos metabólicos
Los fenotipos (ej. metabolizador ultrarrápido, intermedio o pobre) se derivan de los genotipos e indican cómo el cuerpo procesa un fármaco. En un informe farmacogenómico básico, estas categorías son críticas para personalizar tratamientos. Por ejemplo, un metabolizador pobre de CYP2D6 puede presentar mayor riesgo de efectos adversos con antidepresivos tricíclicos.
4. Relación entre genes y fármacos específicos
El informe incluirá tablas o listados que vinculan genes con fármacos. Por ejemplo, el gen TPMT está ligado a la toxicidad de la azatioprina. Estas asociaciones, respaldadas por guías clínicas como las del CPIC (Consorcio de Implementación de la Farmacogenómica), ayudan a tomar decisiones terapéuticas basadas en evidencia genética.
5. Recomendaciones terapéuticas y limitaciones
La última sección del informe suele contener sugerencias basadas en los hallazgos genéticos, como ajustes de dosis o fármacos alternativos. Es clave recordar que un informe farmacogenómico básico no cubre todas las interacciones posibles y debe integrarse con otros datos clínicos para una decisión integral.
| Gen analizado | Ejemplo de genotipo | Fenotipo asociado | Fármaco afectado |
|---|---|---|---|
| CYP2D6 | 4/4 | Metabolizador pobre | Codeína, tramadol |
| CYP2C19 | 1/17 | Metabolizador ultrarrápido | Clopidogrel |
| TPMT | 3A/3C | Actividad enzimática baja | Azatioprina |
| VKORC1 | GG | Sensibilidad aumentada | Warfarina |
Guía detallada: Cómo interpretar un informe farmacogenómico básico paso a paso
¿Cómo se debe interpretar la estructura y los componentes clave de un informe farmacogenómico básico?
La interpretación de un informe farmacogenómico básico requiere comprender su estructura y componentes clave, los cuales suelen incluir: datos del paciente, variantes genéticas analizadas, fármacos evaluados, resultados de metabolización (ej. fenotipo CYP450) y recomendaciones terapéuticas. Cada sección debe analizarse en conjunto, priorizando las interacciones entre genotipo y fármacos para personalizar el tratamiento. Es fundamental validar la fuente de datos genéticos y contrastar las conclusiones con guías clínicas actualizadas para asegurar precisión.
Datos del paciente y contexto clínico
Los datos del paciente (edad, sexo, historial médico) son esenciales para contextualizar los resultados genéticos. Un informe farmacogenómico básico debe incluir esta información para correlacionar las variantes genéticas con condiciones específicas, como enfermedades crónicas o polimedicación. Por ejemplo, un paciente con deficiencia en CYP2D6 podría requerir ajustes en dosis de antidepresivos.
| Componente | Importancia |
|---|---|
| Edad/Sexo | Influye en metabolismo y riesgo de efectos adversos |
| Medicamentos actuales | Identifica interacciones potenciales |
| Historial clínico | Contextualiza relevancia de variantes |
Variantes genéticas y su impacto farmacológico
Las variantes genéticas (ej. SNPs en genes CYP450) determinan la capacidad de metabolizar fármacos. Cómo interpretar un informe farmacogenómico básico implica analizar si el paciente es metabolizador rápido, intermedio o lento, lo que afecta la elección y dosificación de medicamentos. Por ejemplo, una mutación en TPMT contraindica el uso estándar de azatioprina por riesgo de toxicidad hematológica.
Recomendaciones terapéuticas y guías clínicas
Las recomendaciones terapéuticas deben basarse en evidencia científica consolidada (ej. guías CPIC o DPWG). Este apartado sugiere alternativas farmacológicas o ajustes de dosis según el genotipo, asegurando seguridad y eficacia. Por ejemplo, pacientes con HLA-B15:02 deben evitar carbamazepina por riesgo de reacciones cutáneas graves.
¿Qué información específica sobre la respuesta a medicamentos puede derivarse de los resultados de un informe farmacogenómico?
Un informe farmacogenómico proporciona información detallada sobre cómo las variantes genéticas de un individuo pueden influir en su respuesta a medicamentos, incluyendo datos sobre la eficacia, la toxicidad y la dosis óptima de fármacos específicos. Este análisis permite identificar si un paciente es metabolizador rápido, intermedio o lento de ciertos medicamentos, lo que ayuda a predecir posibles efectos adversos o la necesidad de ajustar la terapia. Además, el informe puede revelar la presencia de marcadores genéticos asociados a reacciones alérgicas o resistencia a tratamientos, facilitando una medicina personalizada. Cómo interpretar un informe farmacogenómico básico requiere comprender estos aspectos para optimizar decisiones clínicas.
Eficacia de los medicamentos según el perfil genético
El informe farmacogenómico evalúa cómo las variantes genéticas afectan la eficacia de un fármaco, determinando si un paciente tiene mayor o menor probabilidad de beneficiarse de un tratamiento. Por ejemplo, ciertos polimorfismos en genes como CYP2D6 o VKORC1 pueden indicar si un medicamento será efectivo o requiere alternativas. Esta información es crucial para evitar terapias innecesarias y seleccionar opciones con mayor probabilidad de éxito.
Riesgo de toxicidad y efectos adversos
Los resultados del informe identifican predisposiciones genéticas a toxicidad o efectos adversos, como reacciones graves a medicamentos como la carbamazepina en pacientes con el alelo HLA-B15:02. Esto permite a los profesionales evitar fármacos de alto riesgo o monitorizar estrechamente al paciente, reduciendo complicaciones.
Ajuste de dosis basado en la genética
La farmacogenómica guía el ajuste de dosis según la capacidad de metabolización, particularmente en fármacos con estrecho margen terapéutico como la warfarina o los antidepresivos. Por ejemplo, los metabolizadores lentos de CYP2C19 pueden requerir dosis menores para evitar acumulación tóxica.
| Gen analizado | Medicamento afectado | Implicación clínica |
|---|---|---|
| CYP2D6 | Codeína | Metabolizadores ultrarrápidos tienen riesgo de toxicidad |
| TPMT | Azatioprina | Dosis reducida en metabolizadores lentos |
¿En qué consiste un estudio farmacogenético y cómo se relaciona con la interpretación de un informe básico?
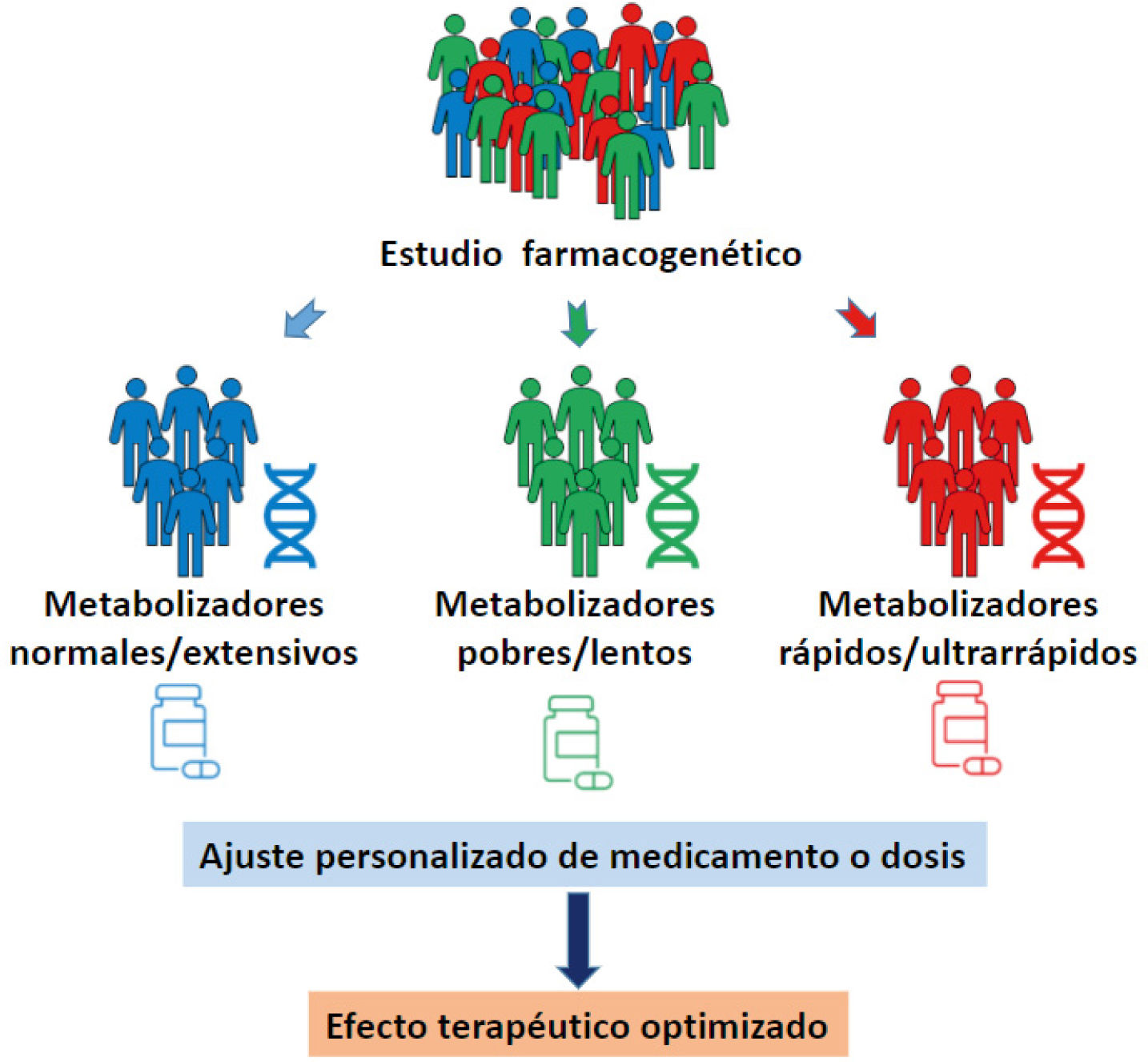
Un estudio farmacogenético consiste en analizar variaciones genéticas específicas en un individuo para determinar cómo estos genes afectan la respuesta a fármacos, optimizando así la eficacia y reduciendo los efectos adversos. Este estudio se relaciona directamente con cómo interpretar un informe farmacogenómico básico, ya que el informe detalla los resultados genéticos y proporciona recomendaciones personalizadas sobre dosis, selección de medicamentos y posibles riesgos basados en las variantes identificadas, lo que permite a profesionales de la salud tomar decisiones terapéuticas más precisas.
Componentes clave de un estudio farmacogenético
Un estudio farmacogenético se centra en genes específicos como CYP2D6, CYP2C19 o VKORC1, que influyen en el metabolismo de fármacos. Estos genes se analizan mediante técnicas como la secuenciación genómica o PCR, identificando polimorfismos que pueden alterar la actividad enzimática. Los resultados se traducen en un informe que clasifica al paciente en categorías como metabolizador rápido, intermedio o lento, lo cual es crucial para cómo interpretar un informe farmacogenómico básico y ajustar tratamientos.
Relación entre genes y respuesta a medicamentos
La farmacogenética explora cómo ciertas variantes genéticas afectan la absorción, distribución, metabolismo y excreción de fármacos. Por ejemplo, una mutación en el gen CYP2C19 puede reducir la eficacia del clopidogrel, aumentando el riesgo cardiovascular. Cómo interpretar un informe farmacogenómico básico implica entender estas interacciones para evitar fármacos ineficaces o peligrosos en pacientes con perfiles genéticos específicos.
Estructura de un informe farmacogenético básico
Un informe típico incluye secciones como genes analizados, resultados genotípicos, interpretación clínica y recomendaciones terapéuticas. La tabla siguiente resume elementos esenciales:
| Sección | Contenido |
|---|---|
| Genes analizados | Lista de genes evaluados (ej. CYP2D6, TPMT) |
| Resultados | Genotipo detectado (ej. 1/2) |
| Interpretación | Fenotipo (metabolizador rápido/lento) |
| Recomendaciones | Ajustes de dosis o fármacos alternativos |
Entender cómo interpretar un informe farmacogenómico básico requiere evaluar cada sección en contexto con la historia clínica del paciente para personalizar el tratamiento.
¿Cómo se puede explicar el concepto de farmacogenómica y su aplicación práctica en el contexto de un informe básico?
La farmacogenómica es el estudio de cómo las variaciones genéticas individuales afectan la respuesta a los fármacos, permitiendo personalizar tratamientos para maximizar su eficacia y minimizar efectos adversos. En un informe básico, esto se traduce en analizar genes específicos relacionados con el metabolismo de medicamentos, como CYP2D6 o VKORC1, para predecir dosis óptimas o riesgo de toxicidad. Cómo interpretar un informe farmacogenómico básico implica comprender estos marcadores genéticos y su impacto clínico, facilitando decisiones terapéuticas basadas en evidencia científica.
¿Qué genes se analizan en farmacogenómica?
En la farmacogenómica, se estudian genes clave como CYP2C19, CYP3A4 y TPMT, que influyen en el metabolismo de fármacos como anticoagulantes, antidepresivos o quimioterápicos. Por ejemplo, variantes en TPMT pueden indicar riesgo de toxicidad grave con medicamentos como la azatioprina. Estos análisis permiten ajustar dosis o seleccionar alternativas terapéuticas más seguras.
| Gen | Fármaco asociado | Impacto clínico |
|---|---|---|
| CYP2D6 | Codeína | Metabolismo acelerado o deficiente |
| VKORC1 | Warfarina | Dosis requerida ajustada |
| HLA-B57:01 | Abacavir | Riesgo de reacción alérgica |
¿Cómo se aplica la farmacogenómica en la práctica clínica?
La aplicación práctica se centra en integrar resultados genómicos en historias clínicas para guiar prescripciones. Por ejemplo, pacientes con variantes en CYP2C19 podrían recibir alternativas al clopidogrel si son metabolizadores pobres. Esta aproximación reduce ensayo-error en tratamientos y mejora outcomes.
¿Qué limitaciones tiene la farmacogenómica?
A pesar de su potencial, la farmacogenómica enfrenta desafíos como la falta de acceso a pruebas genéticas, interpretación compleja de resultados y variabilidad étnica en frecuencias genéticas. Además, no todos los fármacos cuentan con directrices basadas en genética, limitando su uso generalizado.
Preguntas Frecuentes
¿Qué es un informe farmacogenómico básico?
Un informe farmacogenómico básico es un documento que analiza cómo las variantes genéticas de un paciente pueden influir en su respuesta a determinados medicamentos, permitiendo ajustar dosis o seleccionar fármacos más seguros y eficaces según su perfil genético.
¿Qué información clave incluye este tipo de informe?
El informe suele contener datos sobre genes específicos (como CYP2D6 o CYP2C19), su estatus metabólico (rápido, intermedio o lento), y recomendaciones basadas en evidencia para optimizar el tratamiento farmacológico y reducir riesgos de efectos adversos.
¿Cómo se interpretan los resultados relacionados con el metabolismo de fármacos?
Los resultados indican si el paciente tiene una capacidad metabólica alterada para procesar ciertos medicamentos, lo que puede requerir ajustes de dosis o evitar fármacos específicos para prevenir toxicidad o falta de eficacia.
¿Quiénes deben utilizar estos informes y cómo aplicarlos en la práctica clínica?
Médicos, farmacéuticos y otros profesionales de la salud pueden usar el informe para tomar decisiones terapéuticas personalizadas, integrando los datos genéticos con el historial clínico del paciente para mejorar la seguridad y efectividad del tratamiento.