La azatioprina es un fármaco inmunosupresor ampliamente utilizado en el tratamiento de enfermedades autoinmunes y trasplantes de órganos. Sin embargo, su eficacia y seguridad varían significativamente entre pacientes, lo cual está fuertemente influenciado por factores genéticos. Comprender cómo la genética afecta la toxicidad de la azatioprina es clave para optimizar su dosificación y minimizar efectos adversos graves, como mielotoxicidad y hepatotoxicidad. Variantes en genes como TPMT y NUDT15 desempeñan un papel determinante en el metabolismo del fármaco, afectando su respuesta clínica. Este artículo explora los mecanismos genéticos subyacentes y su impacto en la seguridad del tratamiento con azatioprina.
Cómo la genética afecta la toxicidad de la azatioprina
La toxicidad de la azatioprina está estrechamente relacionada con variantes genéticas que influyen en su metabolismo y eficacia. Esta variabilidad genética puede determinar tanto la efectividad del tratamiento como el riesgo de efectos adversos. A continuación, se detallan los aspectos clave de Cómo la genética afecta la toxicidad de la azatioprina.
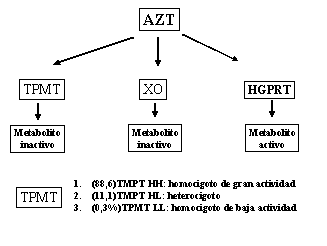
1. El papel de la enzima TPMT en el metabolismo de la azatioprina
La enzima TPMT (tioipurina metiltransferasa) es fundamental para metabolizar la azatioprina. Pacientes con mutaciones en el gen TPMT pueden presentar deficiencia enzimática, lo que aumenta la acumulación de metabolitos tóxicos. Esto eleva el riesgo de mielosupresión, una condición grave que afecta la médula ósea.
2. Variantes genéticas en el gen NUDT15 y su impacto
Otra enzima crítica es la NUDT15, codificada por el gen del mismo nombre. Mutaciones en este gen están asociadas a una mayor susceptibilidad a efectos adversos como leucopenia y alopecia. Estudios indican que ciertas poblaciones, como las de origen asiático, presentan mayor frecuencia de estas variantes.
3. Diferencias étnicas en la respuesta a la azatioprina
La predisposición genética varía según la etnia. Por ejemplo, la deficiencia de TPMT es más común en poblaciones caucásicas, mientras que las mutaciones en NUDT15 predominan en asiáticos. Estas diferencias requieren ajustes posológicos personalizados para minimizar la toxicidad.
4. Pruebas farmacogenéticas antes del tratamiento
Realizar pruebas genéticas para evaluar TPMT y NUDT15 antes de iniciar el tratamiento con azatioprina es una práctica clínica recomendada. Estas pruebas permiten identificar pacientes con alto riesgo de toxicidad y adaptar la dosis o buscar alternativas terapéuticas.
5. Estrategias para reducir la toxicidad basadas en genética
Una vez identificadas las variantes genéticas de riesgo, se pueden implementar estrategias como reducción de dosis o uso de fármacos alternativos. La farmacogenética está transformando el enfoque terapéutico, permitiendo tratamientos más seguros y efectivos.
| Gen | Función | Efecto de las mutaciones |
|---|---|---|
| TPMT | Metaboliza la azatioprina | Aumento de toxicidad hematológica |
| NUDT15 | Protege contra metabolitos tóxicos | Mayor riesgo de leucopenia |
Preguntas Frecuentes
¿Cómo influyen las variantes genéticas en la metabolización de la azatioprina?
Las variantes genéticas en enzimas como la TPMT y NUDT15 afectan la velocidad de metabolización de la azatioprina, lo que puede aumentar el riesgo de toxicidad hematológica en pacientes con actividad enzimática reducida.
¿Qué pruebas genéticas se recomiendan antes de iniciar tratamiento con azatioprina?
Se recomienda analizar los polimorfismos en los genes TPMT y NUDT15 para identificar a pacientes con mayor riesgo de efectos adversos, permitiendo ajustar la dosis o buscar alternativas terapéuticas.
¿Por qué algunos pacientes experimentan toxicidad grave con dosis estándar de azatioprina?
Pacientes con deficiencia genética en TPMT o NUDT15 acumulan metabolitos tóxicos como las 6-TGN, lo que eleva el riesgo de supresión medular y otros efectos secundarios severos incluso con dosis normales.
¿Cómo se puede personalizar el tratamiento con azatioprina basado en la genética?
La farmacogenómica permite ajustar la dosis según el genotipo del paciente: dosis reducidas para metabolizadores lentos y estándar para aquellos con actividad enzimática normal, optimizando eficacia y minimizando riesgos.