es un tema de creciente relevancia en el campo de la oncología y la farmacogenómica. Estas variantes genéticas juegan un papel crucial en el metabolismo de fármacos como las tiopurinas, utilizadas en tratamientos contra el cáncer y enfermedades autoinmunes. Estudios recientes demuestran que mutaciones en TPMT y NUDT15 pueden generar toxicidad grave o falta de eficacia terapéutica, lo que subraya la necesidad de pruebas genéticas previas. Comprender su influencia permite personalizar dosis y reducir efectos adversos, optimizando así los resultados clínicos. Este artículo analiza su mecanismo, implicaciones y avances en medicina personalizada para mejorar la seguridad del paciente.
El impacto de los genes TPMT y NUDT15 en quimioterapia: Una perspectiva genética
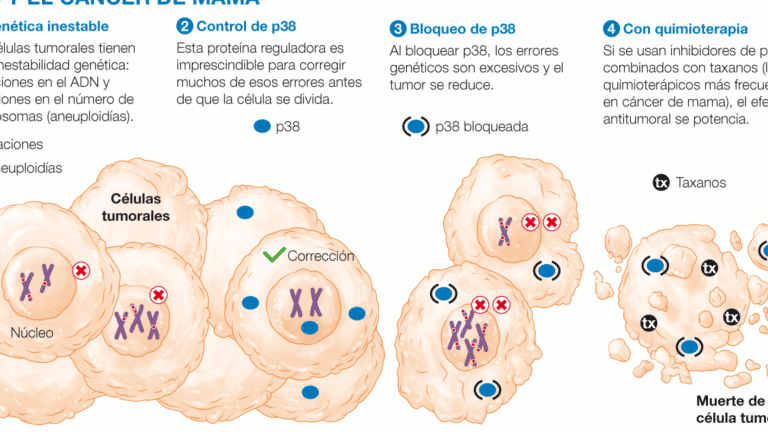
El estudio de los genes TPMT y NUDT15 ha revolucionado el campo de la oncología, particularmente en la administración de quimioterapia. Estas variantes genéticas influyen en la metabolización de fármacos como las tiopurinas, determinando la eficacia y toxicidad de los tratamientos. Comprender su rol permite ajustar dosis de manera personalizada, reduciendo efectos adversos graves como la mielosupresión.
1. ¿Qué son los genes TPMT y NUDT15?
Los genes TPMT (Tiopurina S-Metiltransferasa) y NUDT15 (Nucleósido Difosfato Linked Moieties X-Type Motif 15) codifican enzimas clave en el metabolismo de fármacos utilizados en quimioterapia, especialmente las tiopurinas (6-mercaptopurina y azatioprina). Pacientes con mutaciones en estos genes pueden presentar alteraciones en la degradación de estos medicamentos, aumentando el riesgo de toxicidad.
2. Mecanismos de acción de TPMT y NUDT15 en la metabolización de fármacos
La enzima TPMT actúa metilando tiopurinas, inactivándolas para su excreción, mientras que NUDT15 regula los niveles de metabolitos activos intracelulares. Mutaciones en estos genes reducen su actividad enzimática, acumulando compuestos tóxicos que dañan células hematopoyéticas, generando efectos como leucopenia o anemia.
3. Implicaciones clínicas en tratamientos oncológicos
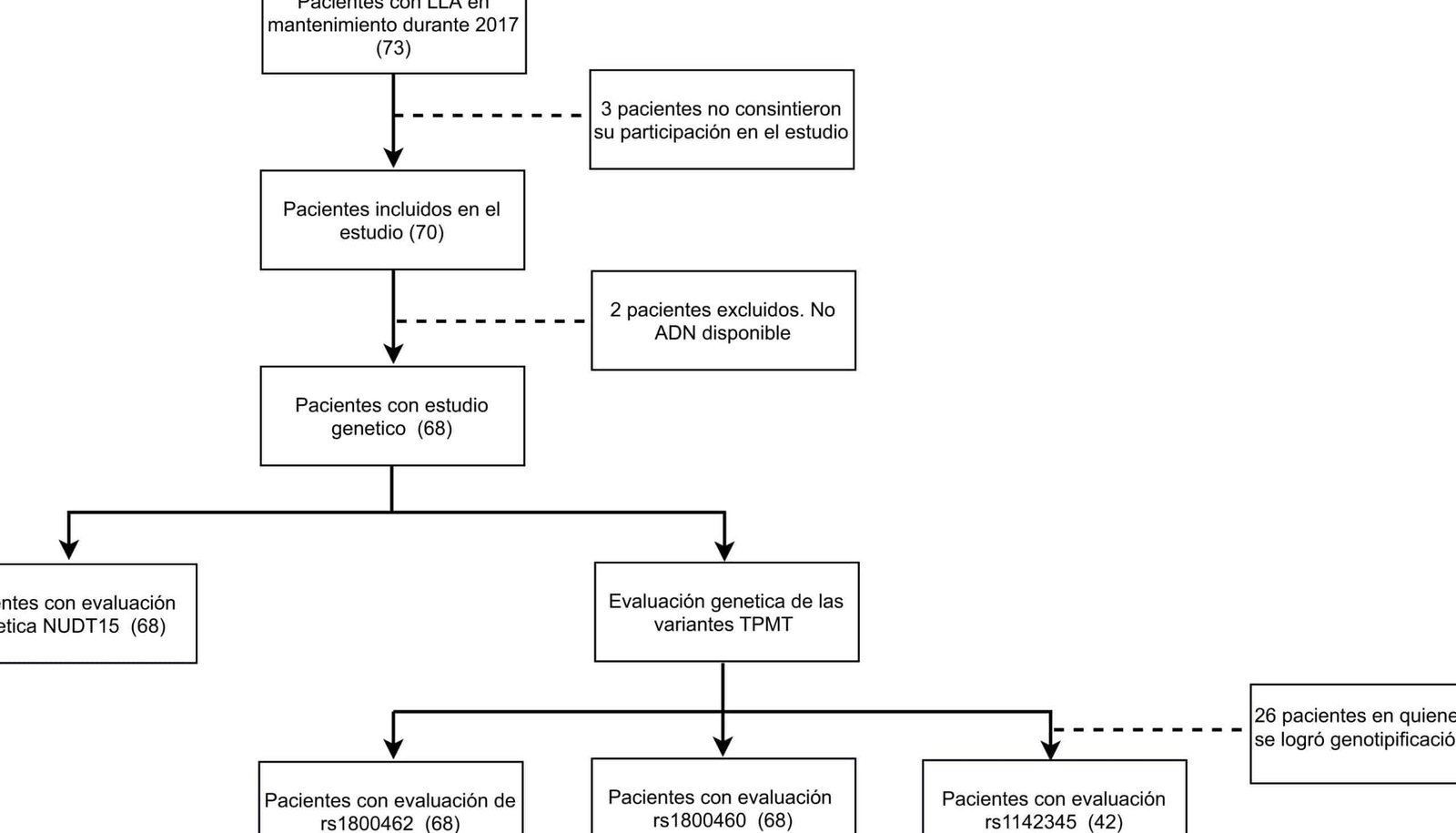
El impacto de los genes TPMT y NUDT15 en quimioterapia es crítico en enfermedades como la leucemia linfoblástica aguda (LLA). Protocolos actuales recomiendan pruebas genéticas previas al tratamiento: pacientes con variantes de riesgo requieren dosis reducidas hasta en un 90% para evitar toxicidad severa y mejorar la supervivencia.
4. Diferencias étnicas en la prevalencia de mutaciones
Las mutaciones en TPMT son más frecuentes en poblaciones caucásicas (3-14%), mientras que las de NUDT15 predominan en asiáticos (10-30%). Esta disparidad subraya la necesidad de estrategias de diagnóstico adaptadas a la diversidad genética global, optimizando la seguridad en quimioterapia.
5. Tecnologías de diagnóstico y guías farmacogenómicas
Métodos como PCR en tiempo real o secuenciación de ADN identifican polimorfismos en TPMT/NUDT15. Organismos como la FDA incluyen recomendaciones farmacogenómicas en prospectos de tiopurinas, destacando el impacto de estos genes en pautas posológicas y monitoreo hematológico durante la quimioterapia.
| Gen | Función Enzimática | Fármacos Afectados | Efecto de Mutaciones |
|---|---|---|---|
| TPMT | Metilación de tiopurinas | 6-mercaptopurina, Azatioprina | Mielosupresión grave |
| NUDT15 | Degradación de metabolitos activos | 6-mercaptopurina | Hepatotoxicidad, alopecia |
Preguntas Frecuentes
¿Qué papel desempeñan los genes TPMT y NUDT15 en la quimioterapia?
Los genes TPMT y NUDT15 son cruciales en el metabolismo de ciertos fármacos utilizados en quimioterapia, como la mercaptopurina y la tioguanina. Variantes genéticas en estos genes pueden afectar la actividad enzimática, lo que influye en la eficacia y toxicidad del tratamiento, aumentando el riesgo de efectos secundarios graves como mielosupresión.
¿Cómo afectan las variantes genéticas de TPMT y NUDT15 a la dosis de medicamentos?
Pacientes con variantes genéticas en TPMT o NUDT15 pueden requerir ajustes de dosis o medicamentos alternativos, ya que una actividad enzimática reducida puede provocar acumulación de fármacos tóxicos en el organismo. Los médicos usan pruebas genéticas para personalizar tratamientos y minimizar riesgos de toxicidad hematológica.
¿Es necesario realizar pruebas genéticas antes de iniciar quimioterapia con tiopurinas?
Sí, se recomienda realizar pruebas genéticas previas para evaluar las variantes en TPMT y NUDT15, especialmente en tratamientos con tiopurinas. Esto permite identificar pacientes con mayor riesgo de efectos adversos y ajustar el régimen terapéutico, mejorando la seguridad y eficacia del tratamiento.
¿Qué consecuencias tiene ignorar los resultados de las pruebas de TPMT y NUDT15?
Ignorar los resultados de estas pruebas puede llevar a toxicidad grave, como daño medular, infecciones o hemorragias, debido a la incapacidad de metabolizar adecuadamente los fármacos. La medicina personalizada basada en genética es clave para evitar complicaciones y optimizar los resultados del tratamiento.