Introducción
es un tema de creciente relevancia en el campo de la oncología y la farmacogenómica. El 5-fluorouracilo (5-FU) es un fármaco ampliamente utilizado en el tratamiento de diversos tipos de cáncer, pero su eficacia puede verse comprometida por reacciones adversas graves en pacientes con variantes genéticas específicas en el gen DPYD. Este gen codifica la enzima dihidropirimidina deshidrogenasa, responsable del metabolismo del 5-FU. La identificación de polimorfismos en DPYD permite predecir el riesgo de toxicidad severa, optimizando así la seguridad y eficacia del tratamiento. Este artículo explora cómo las variaciones genéticas en DPYD influyen en la respuesta a la quimioterapia y su aplicación en la medicina personalizada.
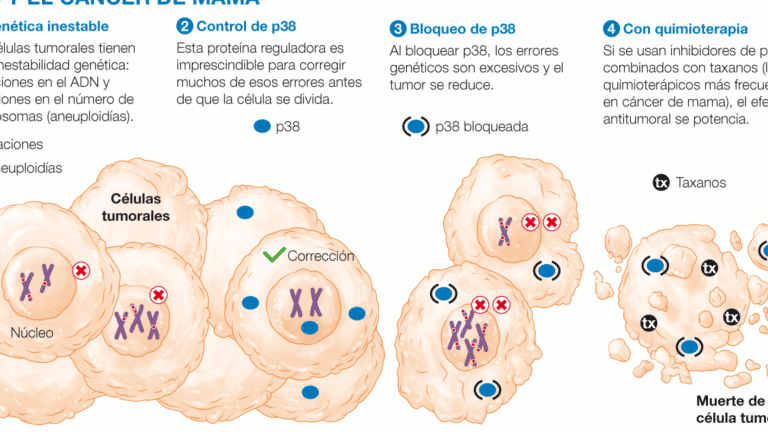
El impacto del gen DPYD en la toxicidad de la quimioterapia (5-FU)
El gen DPYD juega un papel crucial en el metabolismo del fármaco quimioterapéutico 5-fluorouracilo (5-FU), comúnmente utilizado en el tratamiento de cánceres como el colorrectal, de mama y de cabeza y cuello. Variantes genéticas en DPYD pueden reducir la actividad de la enzima dihidropirimidina deshidrogenasa (DPD), encargada de metabolizar el 5-FU, lo que aumenta el riesgo de toxicidad grave, como neutropenia, mucositis o incluso la muerte. Por ello, el análisis farmacogenético de DPYD es esencial para personalizar las dosis y minimizar efectos adversos.
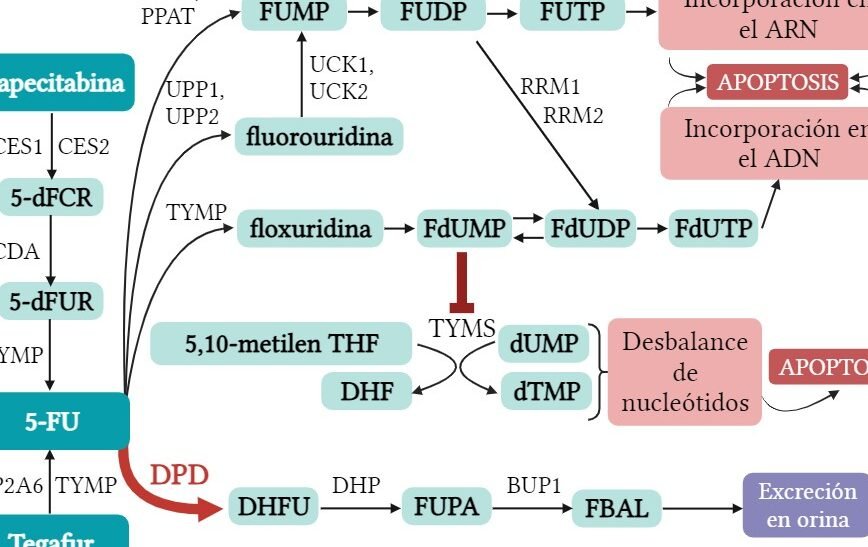
1. ¿Qué es el gen DPYD y cómo afecta al metabolismo del 5-FU?
El gen DPYD codifica la enzima DPD, responsable de degradar más del 80% del 5-FU administrado. Pacientes con mutaciones en este gen, como DPYD2A, presentan una actividad enzimática reducida, lo que provoca una acumulación del fármaco en el organismo. Esto incrementa significativamente el riesgo de toxicidad grave, afectando principalmente a la médula ósea y el tracto gastrointestinal.
2. Principales variantes genéticas de DPYD asociadas a toxicidad
Algunas variantes críticas de DPYD incluyen:
- DPYD2A (rs3918290): Asociada a una actividad enzimática nula.
- DPYD13 (rs55886062): Reduce la función de la enzima.
- rs67376798: Disminuye la afinidad por el sustrato.
La presencia de estas mutaciones eleva el riesgo de efectos adversos severos con dosis estándar de 5-FU.
3. Pruebas genéticas para detectar deficiencia de DPD
Antes de iniciar un tratamiento con 5-FU, se recomienda un análisis farmacogenético para identificar mutaciones en DPYD. Métodos como la secuenciación o PCR en tiempo real permiten detectar variantes de riesgo. En casos de deficiencia parcial o total de DPD, se ajusta la dosis o se opta por terapias alternativas para evitar complicaciones.
4. Síntomas de toxicidad por 5-FU en pacientes con deficiencia de DPD
Los pacientes con mutaciones en DPYD pueden presentar:
- Neutropenia febril (recuento bajo de glóbulos blancos).
- Mucositis grave (inflamación del tracto digestivo).
- Neurotoxicidad o cardiotoxicidad.
Estos síntomas suelen aparecer en los primeros ciclos de quimioterapia.
5. Estrategias para minimizar la toxicidad del 5-FU
Para reducir riesgos en pacientes con alteraciones en DPYD, se implementan:
- Reducción de dosis basada en el genotipo.
- Uso de terapias alternativas como capecitabina (con precaución).
- Monitorización estrecha de parámetros hematológicos.
| Variante de DPYD | Efecto en la enzima DPD | Riesgo de toxicidad |
|---|---|---|
| DPYD2A (rs3918290) | Actividad nula | Muy alto |
| DPYD13 (rs55886062) | Reducción severa | Alto |
| rs67376798 | Función disminuida | Moderado |
Preguntas Frecuentes
¿Qué es el gen DPYD y cómo afecta a la quimioterapia con 5-FU?
El gen DPYD codifica la enzima dihidropirimidina deshidrogenasa (DPD), responsable de metabolizar el 5-fluorouracilo (5-FU), un fármaco común en quimioterapia. Las variantes genéticas en DPYD pueden reducir la actividad de esta enzima, aumentando el riesgo de toxicidad grave como neutropenia, diarrea o neurotoxicidad.
¿Cómo se diagnostica la deficiencia de DPD antes del tratamiento con 5-FU?
La deficiencia de DPD puede identificarse mediante test genéticos que detectan variantes en el gen DPYD, como 2A, 13 o D949V. También existen pruebas bioquímicas para medir la actividad enzimática en sangre. Estas pruebas son clave para ajustar la dosis o evitar el uso de 5-FU en pacientes de alto riesgo.
¿Qué opciones tienen los pacientes con deficiencia de DPYD para recibir quimioterapia?
En casos de deficiencia severa de DPD, se recomienda evitar el 5-FU o usar alternativas terapéuticas como capecitabina (con precaución) o regímenes sin fluoropirimidinas. En deficiencias parciales, puede reducirse la dosis bajo monitoreo estrecho para minimizar la toxicidad sin comprometer la eficacia.
¿Por qué no todos los hospitales realizan pruebas de DPYD antes de administrar 5-FU?
Aunque las guías clínicas recomiendan el cribado genético previo, su implementación varía debido a factores como disponibilidad de tests, costos o falta de protocolos estandarizados. Sin embargo, la evidencia respalda su uso para prevenir efectos adversos graves y optimizar el tratamiento.