La representa un avance fundamental en el campo de la neurología y la medicina personalizada, permitiendo optimizar el tratamiento de la epilepsia según el perfil genético de cada paciente. Esta disciplina estudia cómo las variaciones genéticas influyen en la respuesta a los fármacos, reduciendo efectos adversos y mejorando su eficacia. Con el análisis de biomarcadores específicos, es posible seleccionar el medicamento más adecuado y ajustar su dosificación de manera precisa. La integración de la en la práctica clínica promete transformar el manejo de esta enfermedad, ofreciendo terapias más seguras y efectivas.
Farmacogenómica de los medicamentos antiepilépticos: Personalización del tratamiento en epilepsia
La Farmacogenómica de los medicamentos antiepilépticos estudia cómo las variaciones genéticas individuales influyen en la respuesta a estos fármacos, permitiendo optimizar su eficacia y reducir efectos adversos. Este enfoque facilita la selección de tratamientos personalizados, mejorando los resultados en pacientes con epilepsia.
1. Bases genéticas de la respuesta a los antiepilépticos
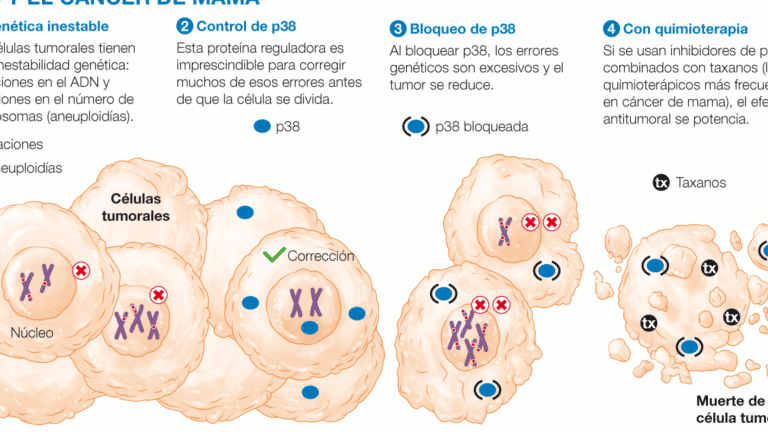
La Farmacogenómica de los medicamentos antiepilépticos identifica polimorfismos en genes como CYP2C9, CYP2C19 o SCN1A, que afectan el metabolismo y la efectividad de estos fármacos. Por ejemplo, variantes en HLA-B15:02 aumentan el riesgo de reacciones cutáneas graves con carbamazepina.
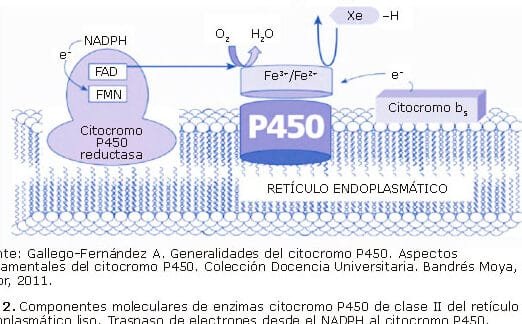
2. Metabolismo y variantes en enzimas CYP450
Las enzimas CYP450 (especialmente CYP2C9 y CYP2C19) metabolizan fármacos como fenitoína o diazepam. La Farmacogenómica de los medicamentos antiepilépticos analiza estas vías para predecir dosis óptimas y evitar toxicidad en metabolizadores lentos o ultra-rápidos.
3. Farmacogenómica y efectos adversos
Marcadores genéticos como HLA-A31:01 se asocian a reacciones adversas. La Farmacogenómica de los medicamentos antiepilépticos contribuye a la prevención, especialmente en poblaciones con mayor prevalencia de estos alelos, como los asiáticos.
4. Aplicaciones clínicas actuales
Guías basadas en la Farmacogenómica de los medicamentos antiepilépticos recomiendan pruebas genéticas previas a prescribir carbamazepina o fenitoína. Esto es clave en pacientes con historial familiar de intolerancia o resistencia farmacológica.
5. Futuro de la farmacogenómica en epilepsia
La integración de paneles genómicos y IA podría expandir la Farmacogenómica de los medicamentos antiepilépticos, permitiendo terapias más precisas y reduciendo el periodo de prueba-error en la selección de fármacos.
| Gen | Fármaco asociado | Impacto clínico |
|---|---|---|
| CYP2C9 | Fenitoína | Metabolismo lento → Toxicidad |
| HLA-B15:02 | Carbamazepina | Riesgo de SJS/NET |
| SCN1A | Fenitoína, Carbamazepina | Resistencia terapéutica |
| UGT1A4 | Lamotrigina | Variación en clearance |
Preguntas Frecuentes
¿Qué es la farmacogenómica en el tratamiento con medicamentos antiepilépticos?
La farmacogenómica estudia cómo las variaciones genéticas de un paciente influyen en su respuesta a los medicamentos antiepilépticos. Este enfoque permite personalizar el tratamiento para mejorar su eficacia y reducir efectos adversos, como reacciones cutáneas graves o falta de respuesta terapéutica.
¿Qué genes están asociados a la respuesta de los antiepilépticos?
Algunos genes clave incluyen HLA (asociado a reacciones de hipersensibilidad), CYP2C9 y CYP2C19 (metabolismo de fármacos como fenitoína), y SCN1A (respuesta a carbamazepina o fenitoína). Analizar estos marcadores ayuda a predecir riesgos y seleccionar el fármaco más seguro y efectivo.
¿Cómo beneficia la farmacogenómica a pacientes con epilepsia?
La farmacogenómica optimiza el tratamiento al identificar terapias dirigidas, minimizando ensayos de error y reduciendo efectos secundarios graves. Esto es especialmente relevante en pacientes con epilepsia refractaria o susceptibilidad genética a reacciones adversas.
¿Está disponible la prueba farmacogenómica para antiepilépticos?
Sí, existen pruebas genéticas comerciales que analizan variantes relacionadas con la metabolización y eficacia de los antiepilépticos. Sin embargo, su implementación clínica varía según el país y requiere la interpretación de un especialista en genética médica o neurología.