La farmacogenómica en pediatría: dosis seguras para niños representa un avance crucial en la medicina personalizada, permitiendo optimizar tratamientos según la genética de cada paciente. En pediatría, donde las diferencias metabólicas y de desarrollo exigen precisiones únicas, esta disciplina cobra especial relevancia. Al analizar variantes genéticas, los profesionales pueden determinar dosis más seguras y eficaces, minimizando riesgos de reacciones adversas o ineficacia terapéutica. Este enfoque no solo mejora los resultados clínicos, sino que también reduce la experimentación innecesaria en población infantil. La integración de la farmacogenómica en pediatría promete revolucionar el manejo farmacológico, garantizando terapias más seguras y adaptadas a las necesidades de los niños.
La importancia de la Farmacogenómica en pediatría: Dosis seguras para niños
La Farmacogenómica en pediatría: Dosis seguras para niños es un campo de estudio crucial que busca personalizar los tratamientos médicos en función de la genética del paciente. En la población pediátrica, las variaciones genéticas pueden influir en la metabolización de medicamentos, lo que hace necesario ajustar las dosis para evitar efectos adversos o falta de eficacia. Esta disciplina combina la farmacología y la genómica para optimizar la seguridad y eficacia de los tratamientos en los más pequeños.
1. ¿Qué es la Farmacogenómica y por qué es relevante en pediatría?
La Farmacogenómica estudia cómo las variaciones genéticas afectan la respuesta a los fármacos. En pediatría, su relevancia radica en que los niños presentan diferencias metabólicas y fisiológicas comparadas con los adultos. La aplicación de la Farmacogenómica en pediatría: Dosis seguras para niños permite disminuir riesgos como toxicidad o subdosificación, especialmente en fármacos con márgenes terapéuticos estrechos.
2. Principales genes involucrados en la respuesta a fármacos en niños
Algunos genes clave que influyen en la metabolización de medicamentos en niños incluyen CYP2D6, CYP2C9, CYP2C19 y TPMT. Estos genes están asociados a la metabolización de fármacos como antiepilépticos, antidepresivos y quimioterápicos. Identificar polimorfismos en estos genes ayuda a ajustar la dosis segura en tratamientos pediátricos.
3. Desafíos en la implementación de la Farmacogenómica en pediatría
Entre los retos principales se encuentran la falta de estudios clínicos específicos en niños, la variabilidad genética en poblaciones diversas y la necesidad de equipos multidisciplinarios. La Farmacogenómica en pediatría: Dosis seguras para niños requiere avances en investigación y herramientas accesibles para su aplicación rutinaria.
4. Casos prácticos de Farmacogenómica aplicada a dosis pediátricas
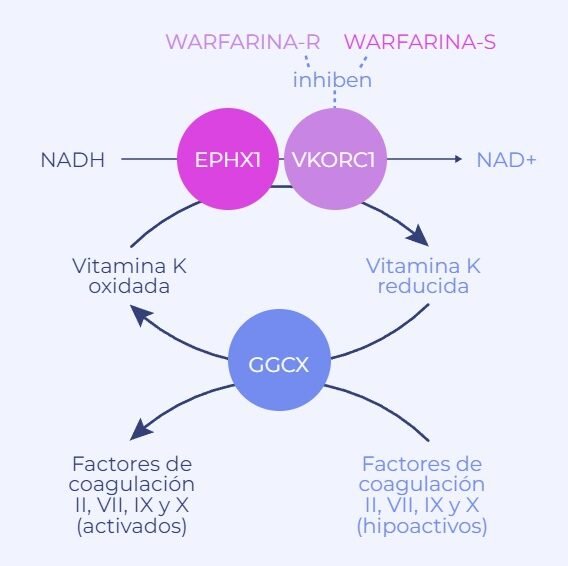
Un ejemplo es el uso de codeína, donde niños con variantes en CYP2D6 pueden ser metabolizadores ultrarrápidos, aumentando el riesgo de depresión respiratoria. Otro caso es la warfarina, cuya dosis debe personalizarse según variantes en CYP2C9 y VKORC1.
5. Futuro y avances tecnológicos en Farmacogenómica pediátrica
La secuenciación genómica masiva y la inteligencia artificial están impulsando la Farmacogenómica en pediatría: Dosis seguras para niños. Estas tecnologías permitirán predecir respuestas a fármacos con mayor precisión y reducir errores en la prescripción pediátrica.
| Gen | Fármaco relacionado | Efecto en la dosis pediátrica |
|---|---|---|
| CYP2D6 | Codeína, antidepresivos | Ajuste necesario en metabolizadores rápidos o lentos |
| TPMT | Azatioprina, mercaptopurina | Reducción de dosis para evitar toxicidad hematológica |
| CYP2C9 | Warfarina, AINEs | Modificación según genotipo para evitar sangrado |
Guía detallada sobre Farmacogenómica en pediatría: Dosis seguras para niños
¿Cómo influye la farmacogenómica en la determinación de dosis seguras y personalizadas para pacientes pediátricos?
La farmacogenómica en pediatría: dosis seguras para niños permite optimizar el tratamiento farmacológico al analizar las variaciones genéticas que afectan la respuesta a medicamentos en pacientes pediátricos. Al identificar polimorfismos en genes como CYP2D6 o TPMT, se pueden ajustar las dosis para evitar toxicidad o falta de eficacia, especialmente crucial en niños debido a su desarrollo fisiológico único. Esta personalización mejora la seguridad y eficacia terapéutica, reduciendo el riesgo de reacciones adversas y garantizando tratamientos más precisos.
Variantes genéticas y metabolismo de fármacos en niños
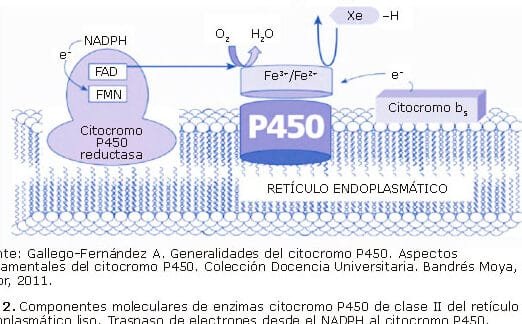
Las variantes genéticas en enzimas metabolizadoras, como las del citocromo P450, determinan la velocidad de procesamiento de fármacos en niños. Por ejemplo, mutaciones en CYP2C19 pueden alterar la efectividad de antiepilépticos como el clobazam, requiriendo ajustes en la dosis. Esto evita efectos secundarios graves y asegura una terapia personalizada.
| Gen | Fármaco afectado | Impacto en dosis pediátricas |
|---|---|---|
| CYP2D6 | Codeína | Evitar en metabolizadores ultrarrápidos (riesgo de depresión respiratoria) |
| TPMT | Azatioprina | Reducción de dosis en pacientes con actividad enzimática baja |
Reducción de errores terapéuticos mediante farmacogenómica
La farmacogenómica minimiza errores en prescripciones pediátricas al predecir interacciones y sensibilidades individuales. Por ejemplo, niños con alteraciones en SLCO1B1 pueden presentar toxicidad con estatinas, lo que obliga a modificar esquemas terapéuticos. Esto refuerza la necesidad de pruebas genéticas previas a tratamientos complejos.
Aplicaciones clínicas en oncología pediátrica
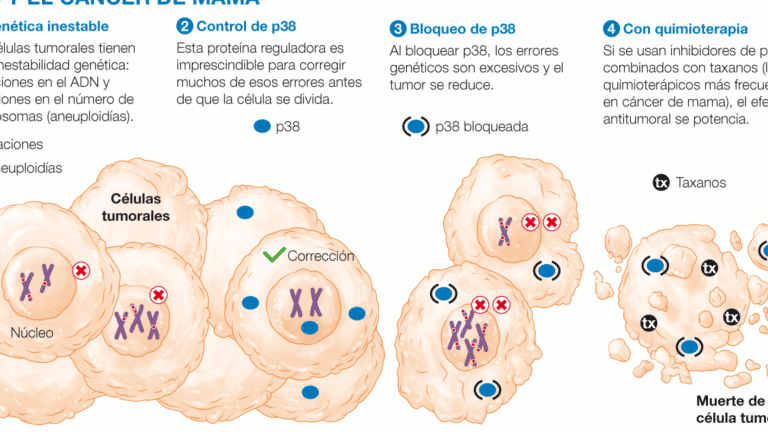
En cáncer infantil, la farmacogenómica en pediatría: dosis seguras para niños es vital para fármacos como la mercaptopurina, donde mutaciones en TPMT exigen ajustes para prevenir mielotoxicidad. Estas herramientas permiten protocolos más seguros y evitan complicaciones en pacientes con perfiles genéticos de alto riesgo.
¿Qué vías de administración de medicamentos son más recomendables en pediatría según los estudios farmacogenómicos?
Según estudios farmacogenómicos, en pediatría las vías de administración más recomendables son la oral, por su seguridad y facilidad de uso, seguida de la intravenosa para situaciones críticas donde se requiere un efecto rápido y preciso, y la transdérmica en casos seleccionados para evitar el metabolismo hepático de primer paso. La Farmacogenómica en pediatría: Dosis seguras para niños demuestra que estas vías optimizan la respuesta terapéutica y reducen efectos adversos, adaptándose a las variaciones genéticas en el metabolismo infantil.
Vía oral en pediatría: beneficios y consideraciones farmacogenómicas
La vía oral es la más utilizada en pediatría debido a su no invasividad y aceptación por parte de los niños. Estudios de farmacogenómica destacan que esta vía permite ajustar dosis según polimorfismos genéticos que afectan la absorción y metabolismo de fármacos, como en el caso de la warfarina o el metilfenidato. Sin embargo, se debe considerar la variabilidad en la maduración enzimática gastrointestinal y hepática, especialmente en neonatos y lactantes.
Vía intravenosa: precisión y farmacogenómica en situaciones críticas
La vía intravenosa es clave en emergencias pediátricas, ya que ofrece un control exacto de la dosis y evita variabilidades en la absorción. La Farmacogenómica en pediatría: Dosis seguras para niños revela que esta vía es ideal para fármacos con estrecho índice terapéutico, como vancomicina, donde variantes genéticas en el gen _CYP2D6_ influyen en su clearance. La monitorización terapéutica es esencial para evitar toxicidad.
| Vía de administración | Ventajas | Consideraciones farmacogenómicas |
|---|---|---|
| Oral | No invasiva, fácil administración | Variabilidad en enzimas CYP450 y transportadores |
| Intravenosa | Efecto rápido, dosificación precisa | Genes implicados en metabolismo (ej. _CYP2C19_) |
Vía transdérmica y farmacogenómica: alternativas en pediatría
La vía transdérmica es una opción en pediatría para fármacos con baja biodisponibilidad oral o alta toxicidad sistémica. La farmacogenómica identifica pacientes con variantes en genes como _GSTA1_, que afectan la detoxificación de parches de fentanilo. Esta vía evita el metabolismo hepático, pero requiere evaluar la integridad de la piel y posibles reacciones locales.
¿Cuáles son los fármacos con mayor variabilidad en respuesta terapéutica en población pediátrica, según los hallazgos farmacogenómicos?
Los fármacos con mayor variabilidad en respuesta terapéutica en población pediátrica, según los hallazgos farmacogenómicos, incluyen antiepilépticos (como fenitoína y carbamazepina), inmunosupresores (tacrolimus y ciclosporina), analgésicos (codeína y tramadol), antipsicóticos (risperidona) y antidepresivos (sertralina y fluoxetina), donde las diferencias genéticas en enzimas como CYP2D6, CYP2C9 y CYP3A4 influyen en su metabolismo, requiriendo ajustes individualizados para lograr Farmacogenómica en pediatría: Dosis seguras para niños.
Antiepilépticos y su relación con polimorfismos genéticos
Los antiepilépticos, como la fenitoína y la carbamazepina, presentan alta variabilidad en niños debido a polimorfismos en los genes CYP2C9 y CYP3A4, que afectan su metabolismo y eficacia. Estudios demuestran que variantes genéticas pueden aumentar el riesgo de toxicidad o fallo terapéutico, destacando la necesidad de pruebas farmacogenómicas previas para ajustar dosis y minimizar riesgos en la población pediátrica.
Inmunosupresores y su sensibilidad genética en niños
El tacrolimus y la ciclosporina, usados en trasplantes, muestran variabilidad clínica asociada a genes como CYP3A5 y ABCB1. En niños, las diferencias en la expresión de estas enzimas pueden llevar a concentraciones subóptimas o tóxicas, requiriendo monitorización estrecha y ajustes basados en Farmacogenómica en pediatría: Dosis seguras para niños para optimizar resultados.
Analgésicos opioides y riesgos en metabolizadores extremos
La codeína y el tramadol son ejemplos de fármacos con riesgos graves en niños debido a polimorfismos en CYP2D6. Metabolizadores ultrarrápidos pueden convertir estos fármacos en morfina de forma acelerada, causando depresión respiratoria, mientras que los metabolizadores lentos tienen menor alivio del dolor. Esto subraya la importancia de evaluar el perfil genético antes de su prescripción.
| Fármaco | Gen asociado | Riesgo en pediatría |
|---|---|---|
| Fenitoína | CYP2C9 | Toxicidad o ineficacia |
| Tacrolimus | CYP3A5 | Niveles séricos impredecibles |
| Codeína | CYP2D6 | Depresión respiratoria |
¿Qué limitaciones actuales impiden una implementación más amplia de la farmacogenómica en la práctica clínica pediátrica?
La implementación más amplia de la farmacogenómica en pediatría: dosis seguras para niños enfrenta varias limitaciones, como la falta de evidencia clínica robusta en poblaciones pediátricas debido a la escasez de estudios farmacogenómicos específicos para niños, la variabilidad genética y ontogénica que complica la interpretación de los resultados, y las barreras económicas y logísticas que dificultan el acceso a pruebas genéticas en entornos clínicos rutinarios. Además, existen desafíos en la integración de datos genómicos en los sistemas de salud, la falta de pautas estandarizadas para su aplicación, y la necesidad de mayor formación entre los profesionales de la salud sobre cómo utilizar esta información para personalizar tratamientos.
Falta de evidencia clínica en poblaciones pediátricas
La farmacogenómica en pediatría: dosis seguras para niños se ve limitada por la escasez de estudios clínicos que validen las asociaciones entre variantes genéticas y respuestas a medicamentos en niños. A diferencia de los adultos, los niños experimentan cambios dinámicos en el metabolismo y la farmacocinética debido a su desarrollo, lo que dificulta extrapolar resultados. Además, los requisitos éticos y logísticos para incluir pacientes pediátricos en ensayos clínicos son más estrictos, reduciendo la disponibilidad de datos relevantes.
Barreras económicas y logísticas
La implementación de la farmacogenómica en entornos pediátricos enfrenta desafíos económicos, como los altos costos de las pruebas genéticas y la falta de cobertura por parte de los sistemas de salud. Además, la infraestructura necesaria para procesar y almacenar datos genómicos no está ampliamente disponible en todos los centros médicos, especialmente en regiones con recursos limitados. Esto limita el acceso equitativo a terapias personalizadas basadas en la genética.
| Desafío | Impacto en Pediatría |
|---|---|
| Falta de evidencia clínica | Dificulta la validación de pautas farmacogenómicas |
| Altos costos | Limita el acceso a pruebas genéticas |
| Infraestructura insuficiente | Obstaculiza el procesamiento de datos genómicos |
Variabilidad genética y ontogénica
La farmacogenómica en pediatría: dosis seguras para niños debe considerar la variabilidad genética única y los cambios ontogénicos que afectan la metabolización de fármacos en diferentes etapas del desarrollo. Los niños no son simplemente adultos pequeños, ya que su perfil farmacológico evoluciona con la edad, lo que complica la interpretación de marcadores genéticos. Esta complejidad requiere algoritmos más sofisticados y estudios longitudinales para garantizar la seguridad y eficacia de los tratamientos.
Preguntas Frecuentes
¿Qué es la farmacogenómica en pediatría y cómo ayuda a determinar dosis seguras para niños?
La farmacogenómica en pediatría estudia cómo las variaciones genéticas de cada niño influyen en su respuesta a los medicamentos, permitiendo ajustar las dosis seguras y minimizar efectos adversos.
¿Por qué es importante la farmacogenómica para los tratamientos médicos en niños?
Es crucial porque los niños metabolizan los fármacos de manera diferente a los adultos, y la farmacogenómica ayuda a personalizar tratamientos basados en su perfil genético, mejorando la eficacia y reduciendo riesgos.
¿Qué tipos de pruebas farmacogenómicas se utilizan en pediatría?
Se emplean pruebas que analizan genes específicos relacionados con el metabolismo de fármacos, como CYP2D6 o CYP3A4, para predecir reacciones y ajustar dosis según la genética individual del paciente.
¿Cómo se implementa la farmacogenómica en la práctica clínica pediátrica?
Se integra mediante guías clínicas y herramientas de apoyo, donde los médicos combinan resultados genéticos con factores como edad, peso y condición médica para optimizar las terapias farmacológicas.