Las variantes genéticas que hacen peligrosos a ciertos antibióticos representan un desafío creciente en la medicina moderna. Estas mutaciones, presentes en bacterias patógenas, pueden conferir resistencia a fármacos diseñados para combatir infecciones, poniendo en riesgo la eficacia de tratamientos esenciales. Estudios recientes demuestran cómo cambios en el ADN bacteriano alteran la sensibilidad a los antibióticos, facilitando su supervivencia y propagación. Este fenómeno no solo complica el manejo de enfermedades, sino que también exige el desarrollo de nuevas estrategias terapéuticas. Comprender estas variantes genéticas es clave para mitigar su impacto y preservar la efectividad de los antibióticos en el futuro.
Variantes genéticas que hacen peligrosos a ciertos antibióticos
Las variantes genéticas en bacterias y en humanos pueden influir en la eficacia y seguridad de los antibióticos. Estas mutaciones pueden provocar resistencia bacteriana a los medicamentos o aumentar el riesgo de efectos adversos en pacientes. Comprender estos mecanismos es clave para optimizar tratamientos y prevenir complicaciones.
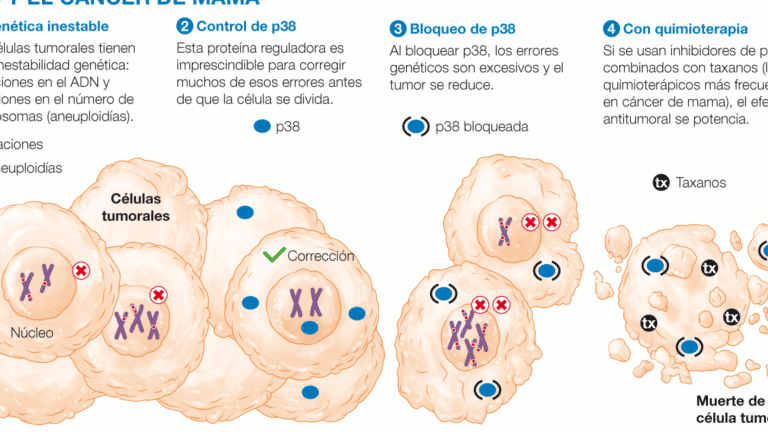
1. Resistencia bacteriana por mutaciones genéticas
Las bacterias desarrollan variantes genéticas que las hacen resistentes a antibióticos como la penicilina o los carbapenémicos. Estas mutaciones pueden alterar las dianas farmacológicas, producir enzimas destructoras (como las beta-lactamasas) o activar bombas de eflujo que expulsan el fármaco de la célula. Este fenómeno reduce las opciones terapéuticas y aumenta la mortalidad en infecciones graves.
2. Efectos adversos en pacientes con polimorfismos genéticos
Algunas variantes genéticas humanas, como las del gen CYP2C9, afectan el metabolismo de antibióticos como sulfonamidas, elevando el riesgo de toxicidad. Pacientes con estas mutaciones pueden sufrir reacciones cutáneas, daño hepático o anemia hemolítica. Un cribado genético previo ayudaría a ajustar dosis o evitar medicamentos peligrosos.
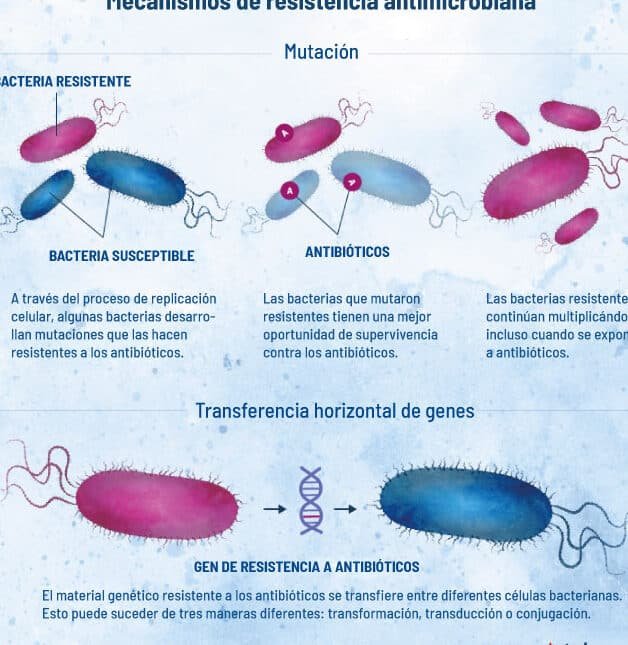
3. Mecanismos de transferencia horizontal de genes
La propagación de variantes genéticas resistentes ocurre mediante plásmidos o transposones, que se intercambian entre bacterias. Este proceso acelera la diseminación de resistencia a múltiples antibióticos, incluso en especies diferentes. Especialmente crítico en entornos hospitalarios donde el uso intensivo de antibióticos favorece su selección.
4. Implicaciones clínicas de las variantes en farmacodinámica
Las mutaciones en genes bacterianos como gyrA o rpoB modifican la unión de antibióticos (quinolonas, rifampicina), reduciendo su eficacia. Estas variantes genéticas obligan a emplear dosis más altas o combinaciones de fármacos, incrementando costos y efectos secundarios.
5. Avances en diagnóstico genómico para combatir la resistencia
Técnicas como la secuenciación masiva permiten identificar variantes genéticas asociadas a resistencia en horas. Esto facilita terapias personalizadas y vigilancia epidemiológica. La integración de estos datos en sistemas de salud es crucial para contener brotes y preservar antibióticos críticos.
| Variante genética | Antibiótico afectado | Consecuencia |
|---|---|---|
| Mutación en mecA | Metilicilina | Resistencia en S. aureus (MRSA) |
| Polimorfismo CYP2C192 | Claritromicina | Metabolismo lento, toxicidad |
| Gen NDM-1 | Carbapenémicos | Degradación del fármaco |
Variantes genéticas que hacen peligrosos a ciertos antibióticos: Guía detallada y actualizada
¿Qué variantes genéticas están asociadas a la resistencia de ciertos antibióticos?
La resistencia a ciertos antibióticos está ligada a variantes genéticas específicas que permiten a las bacterias evadir su efecto, como los genes blaTEM y blaCTX-M, asociados a la producción de β-lactamasas que inactivan penicilinas y cefalosporinas, o los genes mecA en Staphylococcus aureus, que confieren resistencia a meticilina. Otros ejemplos incluyen mutaciones en los genes gyrA y parC, vinculados a resistencia a fluoroquinolonas, y los genes erm, que modifican los ribosomas para resistir macrólidos. Estas variantes genéticas que hacen peligrosos a ciertos antibióticos se propagan mediante plásmidos o transposones, facilitando su diseminación entre bacterias.
Mecanismos moleculares de resistencia a β-lactámicos
La resistencia a antibióticos β-lactámicos, como penicilinas y cefalosporinas, se debe principalmente a la producción de enzimas β-lactamasas, codificadas por genes como blaTEM-1, blaSHV y blaCTX-M. Estas enzimas hidrolizan el anillo β-lactámico, inactivando el antibiótico. Además, algunas bacterias desarrollan mutaciones en las proteínas de unión a penicilina (PBPs), como PBP2a en S. aureus, reduciendo la afinidad por estos fármacos.
| Gen | Antibiótico afectado | Mecanismo |
|---|---|---|
| blaTEM-1 | Penicilinas | Producción de β-lactamasas |
| mecA | Meticilina | Modificación de PBP2a |
| blaCTX-M | Cefalosporinas | Hidrólisis del anillo β-lactámico |
Genes asociados a resistencia a fluoroquinolonas
Las fluoroquinolonas son neutralizadas por mutaciones en los genes gyrA (ADN girasa) y parC (topoisomerasa IV), que alteran los sitios diana del antibiótico en bacterias como E. coli y Pseudomonas aeruginosa. Otras variantes, como los genes qnr en plásmidos, protegen estas enzimas al unirse a ellas, reduciendo la eficacia del fármaco. Estas variantes genéticas que hacen peligrosos a ciertos antibióticos son clave en infecciones hospitalarias.
Resistencia a macrólidos y modificaciones ribosomales
Los macrólidos, como eritromicina, son evadeos mediante genes erm, que metilan el ARNr 23S en el ribosoma bacteriano, impidiendo la unión del antibiótico. Otros genes, como mef y msr, promueven el bombeo activo del fármaco fuera de la célula. Estas adaptaciones genéticas son frecuentes en patógenos como Streptococcus pneumoniae y Staphylococcus aureus.
¿Qué antibióticos presentan mayor riesgo debido a estas variantes genéticas?
Los antibióticos que presentan mayor riesgo debido a variantes genéticas que hacen peligrosos a ciertos antibióticos incluyen fluoroquinolonas (como ciprofloxacino), aminoglucósidos (como gentamicina) y sulfonamidas (como sulfametoxazol), ya que polimorfismos en genes como G6PD, MT-RNR1 o CYP2C9 pueden generar reacciones adversas graves, desde anemia hemolítica hasta toxicidad auditiva o hepatotoxicidad, dependiendo de la predisposición genética del paciente.
Fluoroquinolonas y su relación con variantes genéticas
Las fluoroquinolonas, como ciprofloxacino o levofloxacino, pueden causar roturas tendinosas o neuropatía periférica en pacientes con variantes en genes como COL5A1 o SLCO1B1. Estas variantes genéticas que hacen peligrosos a ciertos antibióticos aumentan el riesgo de daño en tejidos conectivos o alteran el metabolismo del fármaco, lo que exige monitorización estrecha en individuos susceptibles.
Aminoglucósidos y riesgo de toxicidad auditiva
Los aminoglucósidos (ej. gentamicina, amikacina) están asociados a ototoxicidad irreversible en portadores de mutaciones en el gen MT-RNR1, que afecta la función mitocondrial en células ciliadas del oído interno. Esta condición resalta cómo las variantes genéticas que hacen peligrosos a ciertos antibióticos pueden convertir tratamientos rutinarios en intervenciones de alto riesgo sin un cribado genético previo.
Sulfonamidas y déficit de G6PD
| Antibiótico | Gen afectado | Riesgo principal |
|---|---|---|
| Sulfametoxazol | G6PD | Anemia hemolítica |
Las sulfonamidas, como sulfametoxazol, desencadenan anemia hemolítica en pacientes con déficit de G6PD, una enzima clave en la protección de glóbulos rojos. Aquí, las variantes genéticas que hacen peligrosos a ciertos antibióticos evidencian la necesidad de pruebas genéticas antes de prescribir estos fármacos en poblaciones con alta prevalencia de esta deficiencia.
¿Pueden las variantes genéticas inducidas por antibióticos aumentar su peligrosidad?
Sí, las variantes genéticas inducidas por antibióticos pueden aumentar su peligrosidad al desarrollar mecanismos de resistencia en bacterias, como mutaciones en genes que neutralizan el fármaco o activan bombas de eflujo que lo expulsan. Estas adaptaciones genéticas no solo reducen la eficacia del tratamiento, sino que también pueden transferirse entre bacterias, exacerbando la propagación de cepas resistentes. Un ejemplo son las variantes genéticas que hacen peligrosos a ciertos antibióticos, como las enzimas betalactamasas, que desactivan penicilinas y cefalosporinas, limitando opciones terapéuticas.
Mecanismos de resistencia inducidos por mutaciones genéticas
Las bacterias pueden desarrollar mutaciones espontáneas en genes clave bajo presión antibiótica, como las que alteran el sitio de unión del fármaco a su diana. Por ejemplo, en Mycobacterium tuberculosis, mutaciones en el gen rpoB confieren resistencia a la rifampicina. Estas variantes genéticas que hacen peligrosos a ciertos antibióticos surgen por selección natural y pueden volverse dominantes en poblaciones bacterianas expuestas recurrentemente a tratamientos.
Transferencia horizontal de genes de resistencia
Además de mutaciones, las bacterias adquieren resistencia mediante plásmidos o transposones que portan genes como blaNDM-1 (resistencia a carbapenémicos). Estos elementos genéticos móviles facilitan la diseminación rápida de resistencia entre especies, incluso en ambientes clínicos. La exposición a antibióticos acelera este proceso, creando reservorios de patógenos multirresistentes difíciles de erradicar.
| Gen de resistencia | Antibiótico afectado | Mecanismo |
|---|---|---|
| mecA | Meticilina | Altera la proteína de unión a penicilina (PBP2a) |
| vanA | Vancomicina | Modifica el precursor de la pared celular bacteriana |
Impacto clínico de las variantes resistentes
La emergencia de cepas resistentes debido a variantes genéticas obliga a emplear fármacos de último recurso, como colistina, con mayores efectos secundarios. En infecciones hospitalarias, esto eleva la mortalidad y los costos sanitarios. La vigilancia genómica es crucial para detectar tempranamente variantes genéticas que hacen peligrosos a ciertos antibióticos y ajustar protocolos terapéuticos.
¿Cuáles son los cuatro principales grupos de antibióticos afectados por estas variantes genéticas?
Los cuatro principales grupos de antibióticos afectados por variantes genéticas que hacen peligrosos a ciertos antibióticos son los beta-lactámicos (como las penicilinas y cefalosporinas), los aminoglucósidos (como la gentamicina), las fluoroquinolonas (como la ciprofloxacina) y los macrólidos (como la eritromicina). Estas variantes genéticas pueden generar resistencias bacterianas, reducir la eficacia del tratamiento o incluso aumentar los efectos adversos en pacientes con predisposiciones genéticas específicas.
Beta-lactámicos y resistencia genética
Los beta-lactámicos, incluyendo penicilinas y cefalosporinas, son afectados por variantes genéticas que producen enzimas como las beta-lactamasas, capaces de degradar estos antibióticos. Estas mutaciones son comunes en bacterias como Staphylococcus aureus y Escherichia coli, volviéndolas resistentes y limitando las opciones terapéuticas.
Aminoglucósidos y mutaciones bacterianas
Los aminoglucósidos, como la gentamicina, pueden volverse menos efectivos debido a mutaciones en genes bacterianos que alteran la permeabilidad de la membrana celular o modifican las dianas de estos fármacos. La presencia de variantes genéticas que hacen peligrosos a ciertos antibióticos en patógenos como Pseudomonas aeruginosa complica el tratamiento de infecciones graves.
Fluoroquinolonas y macrólidos en riesgo
Las fluoroquinolonas y los macrólidos enfrentan resistencia por mutaciones en los genes bacterianos que codifican las topoisomerasas o los ribosomas, respectivamente. Por ejemplo, Campylobacter jejuni puede desarrollar resistencia a la ciprofloxacina mediante cambios genéticos, mientras que mutaciones en Streptococcus pneumoniae reducen la eficacia de la eritromicina.
| Grupo de antibióticos | Ejemplo | Mecanismo de resistencia |
|---|---|---|
| Beta-lactámicos | Penicilina | Producción de beta-lactamasas |
| Aminoglucósidos | Gentamicina | Modificación enzimática del antibiótico |
| Fluoroquinolonas | Ciprofloxacina | Mutaciones en topoisomerasas |
| Macrólidos | Eritromicina | Alteración del sitio ribosomal |
Preguntas Frecuentes
¿Qué son las variantes genéticas que hacen peligrosos a ciertos antibióticos?
Las variantes genéticas son cambios en el ADN de las bacterias que les otorgan resistencia a uno o más antibióticos, volviéndolos ineficaces y aumentando el riesgo de infecciones difíciles de tratar.
¿Cómo se transmiten estas variantes genéticas entre bacterias?
Estas variantes pueden propagarse mediante transferencia horizontal de genes, mecanismos como plásmidos o transposones, que permiten a las bacterias compartir genes de resistencia rápidamente, incluso entre especies diferentes.
¿Qué antibióticos son más afectados por estas variantes?
Antibióticos de amplio espectro como las penicilinas, cefalosporinas y fluoroquinolonas son comúnmente impactados, especialmente en infecciones causadas por bacterias como Staphylococcus aureus resistente a meticilina (SARM) o Escherichia coli.
¿Qué medidas pueden prevenir la propagación de estas resistencias?
El uso racional de antibióticos, programas de vigilancia epidemiológica y el desarrollo de nuevos fármacos son estrategias clave para reducir la aparición y diseminación de estas variantes peligrosas.