La transferencia de genes al interior de las células representa un desafío clave en la terapia génica y la investigación biomédica. es un tema de gran relevancia científica, ya que estas partículas ofrecen una alternativa eficiente y segura frente a los vectores tradicionales. Su estructura porosa y biocompatible permite encapsular material genético, protegiéndolo de la degradación y facilitando su liberación controlada. Además, su superficie modificable mejora la especificidad celular, optimizando la entrega terapéutica. Este artículo explora los mecanismos, ventajas y aplicaciones de las nanopartículas de sílice en la administración dirigida de genes.
Mecanismos de transporte de genes mediante nanopartículas de sílice
1. ¿Qué son las nanopartículas de sílice y cómo interactúan con las células?
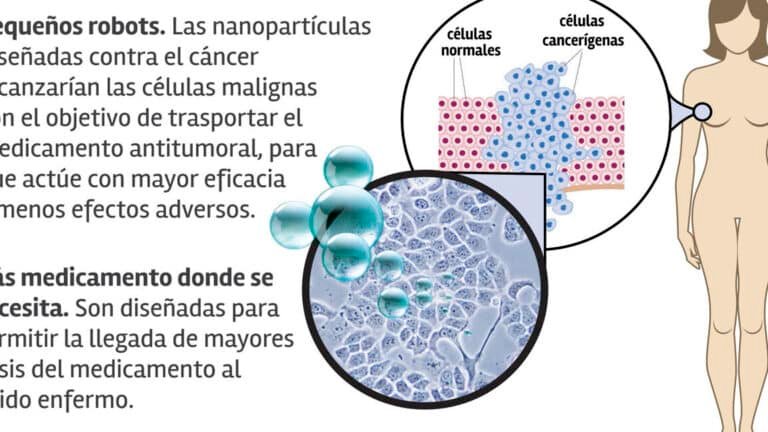
Las nanopartículas de sílice son estructuras microscópicas compuestas principalmente de dióxido de silicio (SiO₂), utilizadas como vectores en la entrega de material genético. Su tamaño nanométrico (1-100 nm) y superficie modificable les permite adsorber o encapsular genes, como plásmidos o ARN, y facilitar su entrada en células mediante endocitosis. Su biocompatibilidad y baja toxicidad las hacen ideales para aplicaciones en terapia génica.
2. Proceso de carga genética en nanopartículas de sílice
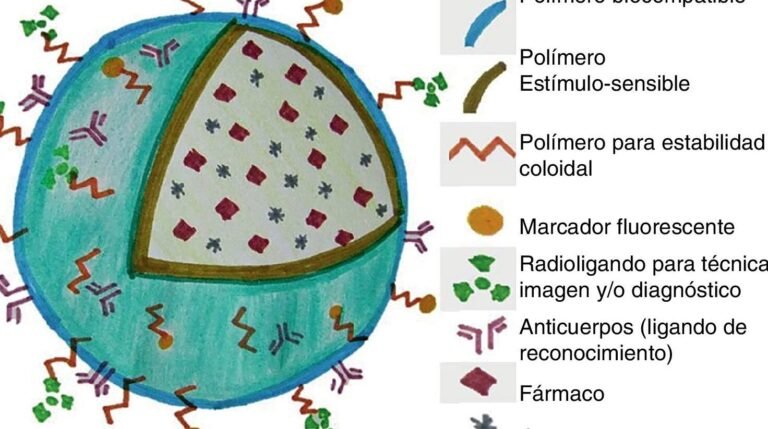
La unión de genes a estas nanopartículas ocurre mediante interacciones electrostáticas o enlaces covalentes. La carga superficial positiva de las nanopartículas (lograda con recubrimientos como polietilenimina) atrae el ADN/ARN (cargado negativamente), formando complejos estables. Otros métodos incluyen la encapsulación en poros mesoporosos de la sílice, protegiendo el material genético de enzimas degradativas.
3. Internalización celular de las nanopartículas de sílice
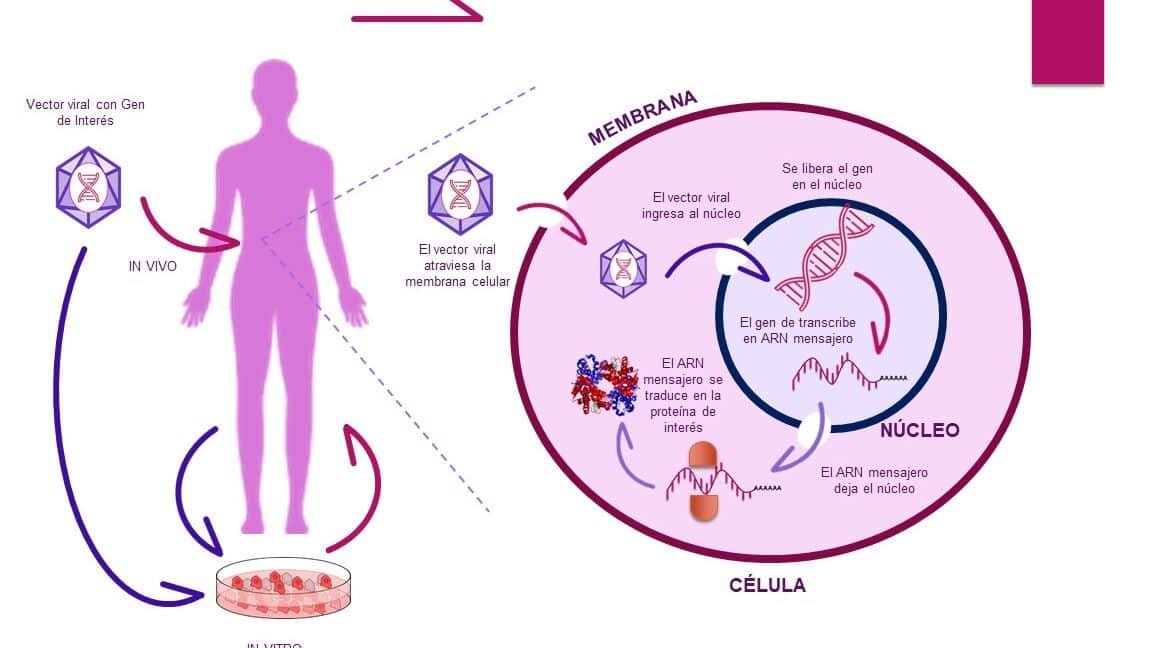
Una vez cargadas, las nanopartículas de sílice ingresan a las células principalmente por endocitosis mediada por receptores o fagocitosis. La superficie puede funcionalizarse con ligandos (como folato o péptidos) para dirigirse a células específicas. Tras la internalización, las nanopartículas escapan del endosoma mediante el efecto protón-esponja o mecanismos de ruptura de la membrana.
4. Liberación y expresión de los genes transportados
Dentro del citoplasma, las nanopartículas liberan los genes mediante degradación controlada de la matriz de sílice (en medios ácidos o enzimáticos). El material genético se transloca al núcleo (en el caso de ADN) o permanece en el citosol (ARN), donde se expresa o silencia genes diana, respectivamente. La eficiencia depende de la estabilidad del complejo y la capacidad de escape intracelular.
5. Ventajas y desafíos en la aplicación terapéutica
Entre las ventajas destacan su alta capacidad de carga, biodegradabilidad y versatilidad en modificaciones. Sin embargo, persisten desafíos como la posible toxicidad a largo plazo, la necesidad de optimizar la liberación controlada y evitar respuestas inmunes. Estudios preclínicos continúan evaluando su seguridad en modelos animales.
| Aspecto | Detalle |
|---|---|
| Tamaño de nanopartículas | 1-100 nm (óptimo para endocitosis) |
| Mecanismo de entrada celular | Endocitosis mediada por receptores |
| Métodos de carga genética | Adsorción electrostática o encapsulación |
| Ventaja principal | Biocompatibilidad y baja citotoxicidad |
| Desafío crítico | Escape endosomal eficiente |
Preguntas Frecuentes
¿Cómo se unen las nanopartículas de sílice a los genes para su transporte?
Las nanopartículas de sílice se funcionalizan químicamente para adsorber o unirse a moléculas de ADN o ARN mediante interacciones electrostáticas o enlaces covalentes. Esta unión permite proteger al material genético de enzimas degradantes y facilita su liberación controlada dentro de la célula.
¿Qué mecanismos permiten la entrada de las nanopartículas de sílice en las células?
Las nanopartículas de sílice ingresan principalmente mediante endocitosis, un proceso en el que la membrana celular las engloba en vesículas internas. Su tamaño pequeño (<100 nm) y superficie modificable optimizan su captación por distintos tipos celulares.
¿Cómo liberan las nanopartículas de sílice los genes en el interior celular?
Una vez dentro de la célula, las nanopartículas sufren degradación en los lisosomas debido al pH ácido o enzimas, liberando gradualmente los genes. Alternativamente, se diseñan partículas sensibles a estímulos como luz o redox para una liberación controlada en compartimentos específicos.
¿Qué ventajas ofrecen las nanopartículas de sílice frente a otros vectores génicos?
Destacan por su baja toxicidad, alta estabilidad y capacidad de modular su superficie para mejorar la especificidad celular. A diferencia de los vectores virales, evitan riesgos de mutagénesis y permiten cargar mayor cantidad de material genético.