El estudio de cómo las nanopartículas poliméricas atraviesan el moco intestinal ha cobrado relevancia en el campo de la medicina y la nanotecnología, debido a su potencial para mejorar la administración de fármacos. Estas nanopartículas, diseñadas a escala nanométrica, enfrentan el desafío de penetrar la barrera viscosa del moco, que tradicionalmente dificulta la absorción de terapias. Mediante estrategias como la modificación superficial y el control de tamaño, estos sistemas logran superar dicha barrera, permitiendo una liberación controlada de principios activos. Este artículo explora los mecanismos clave que facilitan este proceso y sus implicaciones en el desarrollo de tratamientos más eficaces.
Mecanismos clave de cómo las nanopartículas poliméricas atraviesan el moco intestinal
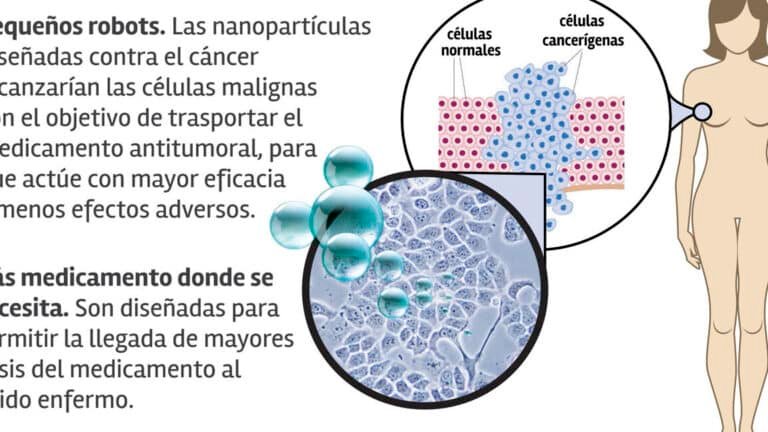
Las nanopartículas poliméricas representan una herramienta prometedora en la administración de fármacos debido a su capacidad para atravesar barreras biológicas como el moco intestinal. Estas partículas logran superar esta barrera gracias a propiedades físicas y químicas específicas, como su tamaño, carga superficial y funcionalización. Su interacción con la estructura del moco, compuesto principalmente por mucinas, determina su eficacia en la penetración y, por ende, en la liberación dirigida de principios activos.
1. Composición y función del moco intestinal como barrera
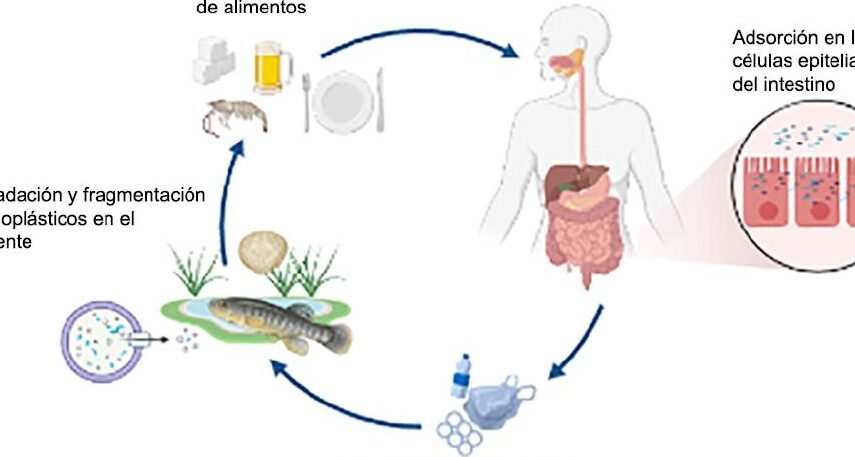
El moco intestinal está constituido por mucinas glicosiladas que forman una red viscosa y dinámica. Su principal función es proteger el epitelio de patógenos y partículas extrañas, pero también limita la absorción de fármacos. Las nanopartículas poliméricas deben ser diseñadas para evadir esta barrera mediante estrategias que reduzcan su adhesión a las mucinas o faciliten su difusión a través de los poros de la red.
2. Tamaño y carga superficial de las nanopartículas poliméricas
El tamaño y la carga superficial de las nanopartículas son determinantes en su capacidad para atravesar el moco. Partículas con diámetros inferiores a 200 nm y carga neutra o ligeramente negativa muestran mayor movilidad, ya que evitan la interacción electrostática con las mucinas cargadas negativamente. Esta optimización es esencial para comprender cómo las nanopartículas poliméricas atraviesan el moco intestinal eficientemente.
3. Funcionalización con ligandos hidrófilos
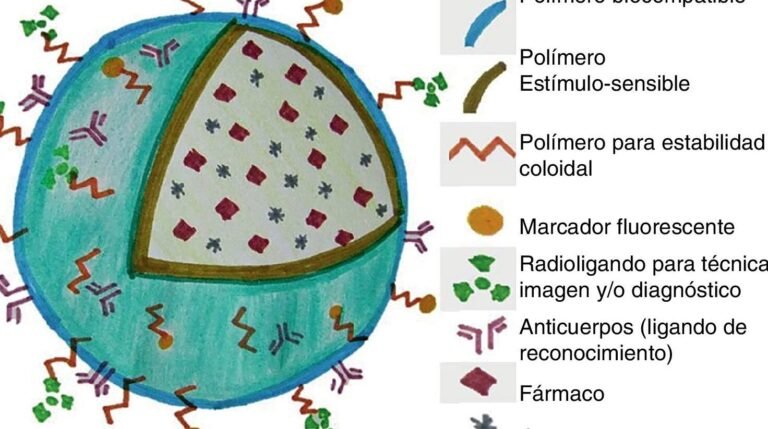
La modificación superficial con polímeros hidrófilos, como el polietilenglicol (PEG), incrementa la estabilidad coloidal y reduce la captura por el moco. Este enmascaramiento minimiza la adhesión a las mucinas, facilitando el desplazamiento de las partículas hacia el epitelio intestinal. Esta técnica mejora significativamente la entrega de fármacos en zonas específicas del intestino.
4. Papel de las enzimas en la degradación del moco
Algunas formulaciones incorporan enzimas como la mucinasa para degradar selectivamente las mucinas, generando caminos temporales que permiten el paso de las nanopartículas poliméricas. Sin embargo, este enfoque requiere un equilibrio, ya que una degradación excesiva podría comprometer la función protectora del moco.
5. Aplicaciones terapéuticas y desafíos futuros
El diseño de nanopartículas para superar el moco intestinal tiene aplicaciones en el tratamiento de enfermedades intestinales, como la enfermedad de Crohn o el cáncer colorrectal. No obstante, persisten desafíos en la escalabilidad, la biocompatibilidad y la reproducibilidad de estos sistemas, aspectos críticos para su traducción clínica.
| Factor | Impacto en la penetración del moco | Ejemplo de optimización |
|---|---|---|
| Tamaño de partícula | Partículas pequeñas (<200 nm) difunden mejor | Síntesis controlada por nanoprecipitación |
| Carga superficial | Carga neutra o negativa reduce interacciones | Recubrimiento con PEG |
| Hidrofilicidad | Superficies hidrófilas evitan adhesión | Funcionalización con polisacáridos |
| Estabilidad en pH intestinal | Resistencia a pH ácido/alcalino | Uso de polímeros entéricos |
Preguntas Frecuentes
¿Qué propiedades deben tener las nanopartículas poliméricas para atravesar el moco intestinal?
Las nanopartículas poliméricas deben poseer un tamaño reducido (menos de 200 nm) y una superficie hidrofílica o recubierta con moléculas neutras, como el polietilenglicol (PEG), para evitar la interacción con las proteínas del moco y facilitar su difusión a través de esta barrera.
¿Cómo afecta la carga superficial de las nanopartículas al transporte a través del moco intestinal?
Una carga superficial neutra o ligeramente negativa es clave, ya que las cargas positivas suelen interactuar fuertemente con los componentes mucosos, generando retención, mientras que una carga neutra o negativa reduce la adhesión y mejora la penetración.
¿Qué mecanismos utilizan las nanopartículas para superar la barrera del moco intestinal?
Los principales mecanismos incluyen la difusión pasiva debido al pequeño tamaño y la habilidad para evitar la captura por la red de mucinas, así como el uso de recubrimientos enzimáticos que degradan parcialmente el moco, acelerando el transporte.
¿Cómo influye la composición polimérica en la eficacia de las nanopartículas para atravesar el moco?
La selección de polímeros biocompatibles y biodegradables, como el PLGA o la quitosana modificada, es crucial, ya que determinan la estabilidad, la interacción con el moco y la capacidad de liberar fármacos de manera controlada tras superar esta barrera.