Introducción
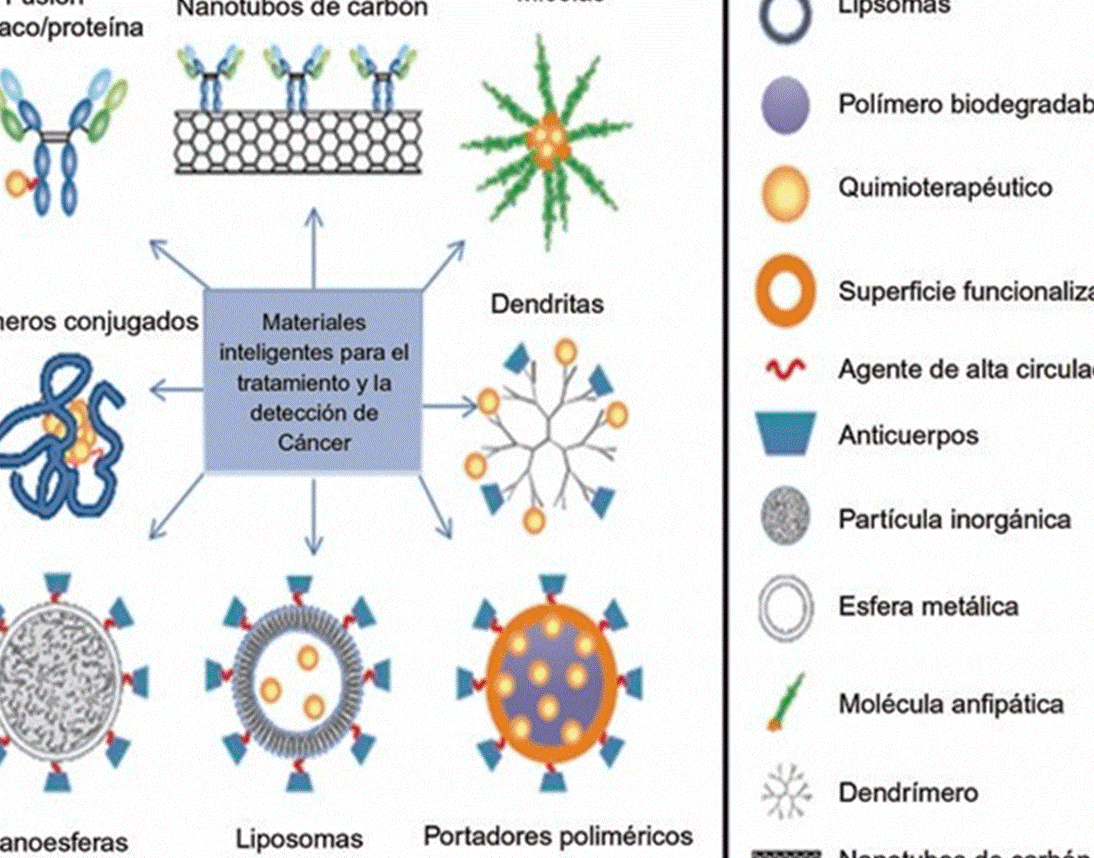
representa una estrategia innovadora en la nanomedicina oncológica. Estos sistemas de administración de fármacos, formados por estructuras autoensambladas, permiten mejorar la solubilidad, estabilidad y distribución de agentes terapéuticos en tejidos tumorales. Su diseño versátil facilita la encapsulación de moléculas hidrofóbicas y la liberación controlada, reduciendo efectos secundarios y aumentando la eficacia antitumoral. Además, la funcionalización superficial de las micelas poliméricas puede dirigirlas específicamente hacia células cancerosas, mejorando la selectividad. Este artículo explora los avances, desafíos y perspectivas futuras de el uso de micelas poliméricas en el tratamiento de tumores sólidos, destacando su potencial en la terapia contra el cáncer.
El uso de micelas poliméricas en el tratamiento de tumores sólidos
El uso de micelas poliméricas en el tratamiento de tumores sólidos representa una estrategia innovadora en la administración de fármacos oncológicos. Estas nanoestructuras permiten una mayor especificidad y reducen los efectos secundarios asociados a terapias convencionales, mejorando la eficacia terapéutica. Su capacidad para encapsular compuestos hidrofóbicos y liberarlos de manera controlada en el tumor las convierte en una herramienta prometedora en oncología.
Mecanismo de acción de las micelas poliméricas
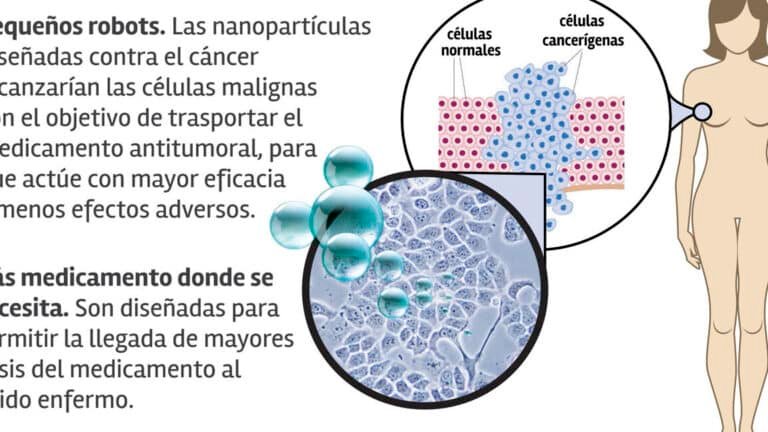
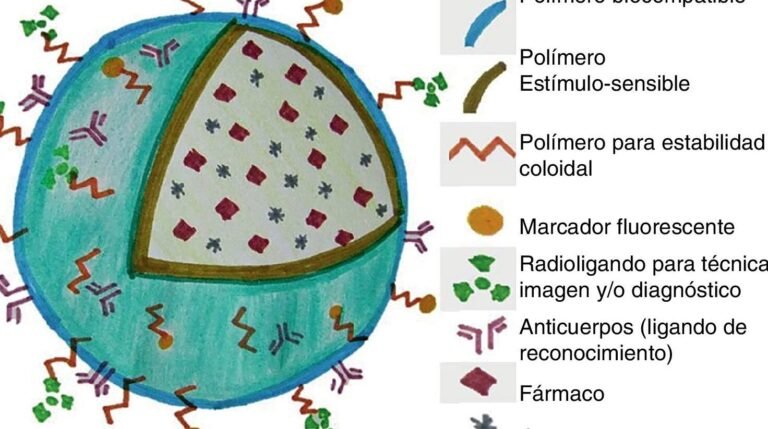
Las micelas poliméricas actúan como vehículos de entrega de fármacos, aprovechando su estructura anfifílica (con regiones hidrofílicas e hidrofóbicas). Al encapsular medicamentos oncológicos, protegen el principio activo de la degradación y facilitan su acumulación en el tejido tumoral gracias al efecto EPR (Enhanced Permeability and Retention).
Ventajas frente a terapias convencionales
El uso de micelas poliméricas en el tratamiento de tumores sólidos ofrece ventajas como mayor biodisponibilidad, menor toxicidad sistémica y capacidad de modificación superficial para dirigirse a receptores específicos en células cancerosas. Esto contrasta con la quimioterapia tradicional, que afecta tanto a células sanas como malignas.
Desafíos en su desarrollo clínico
A pesar de su potencial, su implementación enfrenta retos como la estabilidad en el torrente sanguíneo, escalado industrial y regulación de la liberación del fármaco. Además, la heterogeneidad de los tumores sólidos complica el diseño de micelas universales.
Aplicaciones específicas en oncología
El uso de micelas poliméricas en el tratamiento de tumores sólidos ha demostrado eficacia en cáncer de mama, páncreas y glioblastoma. Por ejemplo, formulaciones con paclitaxel muestran mayor penetración en tejidos metastásicos en comparación con terapias libres.
Futuras direcciones de investigación
Los estudios actuales se centran en micelas inteligentes que respondan a estímulos del microambiente tumoral (pH, enzimas) y en combinaciones con inmunoterapia. También se explora su uso en diagnósticos simultáneos (teranóstica).
| Ventaja | Impacto |
| Alta capacidad de encapsulación | Permite transportar fármacos poco solubles |
| Efecto EPR | Acumulación selectiva en tejido tumoral |
| Reducción de toxicidad | Menos daño a células sanas |
| Modificación superficial | Posibilita定向 al receptor específico |
Preguntas Frecuentes
¿Qué son las micelas poliméricas y cómo actúan en el tratamiento de tumores sólidos?
Las micelas poliméricas son nanoestructuras formadas por cadenas de polímeros anfífilicos que se autoensamblan en medios acuosos. En el tratamiento de tumores sólidos, actúan como vehículos de administración de fármacos, mejorando la solubilidad, estabilidad y entrega controlada de agentes terapéuticos al tejido tumoral, gracias a su capacidad de acumulación pasiva (EFecto EPR).
¿Qué ventajas ofrecen las micelas poliméricas frente a otros sistemas de liberación de fármacos?
Las micelas poliméricas destacan por su biocompatibilidad, baja toxicidad y capacidad para encapsular fármacos hidrofóbicos. Además, su pequeño tamaño (10–100 nm) les permite escapar del sistema reticuloendotelial y acumularse selectivamente en el tumor, reduciendo efectos secundarios y mejorando la eficacia terapéutica.
¿Cómo se logra la liberación controlada del fármaco desde las micelas poliméricas en el tumor?
La liberación controlada se debe a estímulos externos (como pH bajo o enzimas presentes en el microambiente tumoral) o internos (diseño de polímeros sensibles a estímulos). Estas características permiten que el fármaco se libere de forma dirigida en el tumor, minimizando daños a tejidos sanos y aumentando la concentración terapéutica local.
¿Cuáles son los desafíos clínicos actuales de las micelas poliméricas para tratar tumores sólidos?
Entre los principales desafíos están la escalabilidad de su producción, la estabilidad en circulación sanguínea y la posible activación del sistema inmune. Además, se investiga cómo superar la heterogeneidad tumoral y la barrera del estroma para optimizar su penetración y distribución en el tumor.