representa un avance revolucionario en la medicina genética. Estas diminutas estructuras permiten transportar el sistema de edición genética de manera precisa y segura a células específicas, superando desafíos como la degradación enzimática y la respuesta inmunológica. Al encapsular CRISPR en nanopartículas, se mejora su estabilidad y eficiencia, facilitando terapias dirigidas para enfermedades hereditarias, cáncer y trastornos infecciosos. Esta tecnología no solo optimiza la liberación controlada del material genético, sino que también reduce efectos secundarios no deseados. El potencial de esta herramienta promete transformar el tratamiento de condiciones médicas complejas de manera personalizada y accesible.
El uso de nanopartículas para entregar CRISPR en el cuerpo: Avances y aplicaciones
1. ¿Qué son las nanopartículas y cómo funcionan en la entrega de CRISPR?
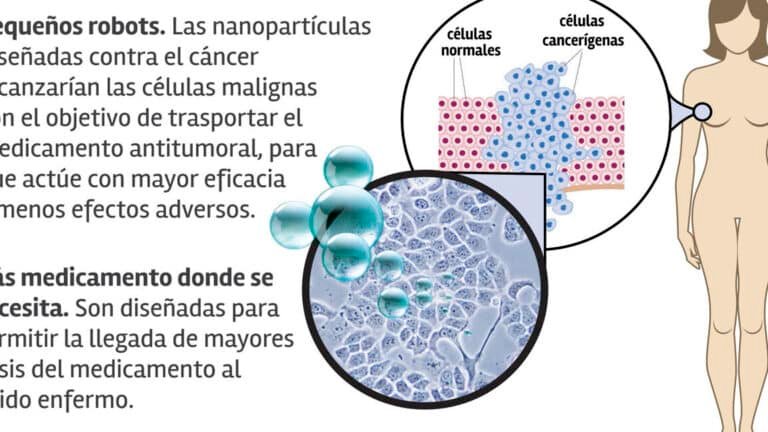
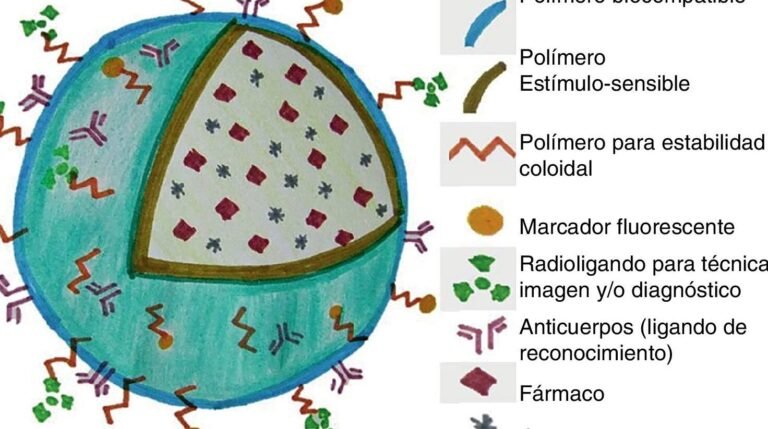
Las nanopartículas son estructuras microscópicas que miden entre 1 y 100 nanómetros, diseñadas para transportar moléculas con alta precisión. En el uso de nanopartículas para entregar CRISPR en el cuerpo, actúan como vehículos protectores, evitando que el sistema inmunológico degrade las herramientas de edición genética antes de llegar al objetivo. Estas partículas pueden ser liposomas, polímeros o materiales inorgánicos, optimizados para liberar CRISPR en células específicas mediante mecanismos como fusión de membranas o endocitosis.
2. Ventajas de utilizar nanopartículas frente a otros métodos de administración
El uso de nanopartículas para entregar CRISPR en el cuerpo ofrece ventajas clave sobre métodos tradicionales (como virus modificados). Entre ellas destacan: mayor seguridad (menor riesgo de mutaciones no deseadas), capacidad de modificación superficial (para dirigirse a tejidos precisos) y estabilidad en circulación sanguínea. Además, permiten cargar múltiples componentes (ARN guía, proteína Cas9) en una sola partícula, simplificando el proceso terapéutico.
3. Desafíos técnicos en el desarrollo de nanopartículas para CRISPR
A pesar del potencial de el uso de nanopartículas para entregar CRISPR en el cuerpo, existen desafíos como la toxicidad por acumulación en órganos no objetivo, la baja eficiencia de entrega intracelular en ciertos tejidos y la necesidad de escalar producción manteniendo uniformidad en tamaño y carga. Investigaciones recientes se centran en funcionalizar superficies con ligandos específicos y optimizar la relación carga/vector para superar estas limitaciones.
4. Aplicaciones actuales en investigación y terapias experimentales
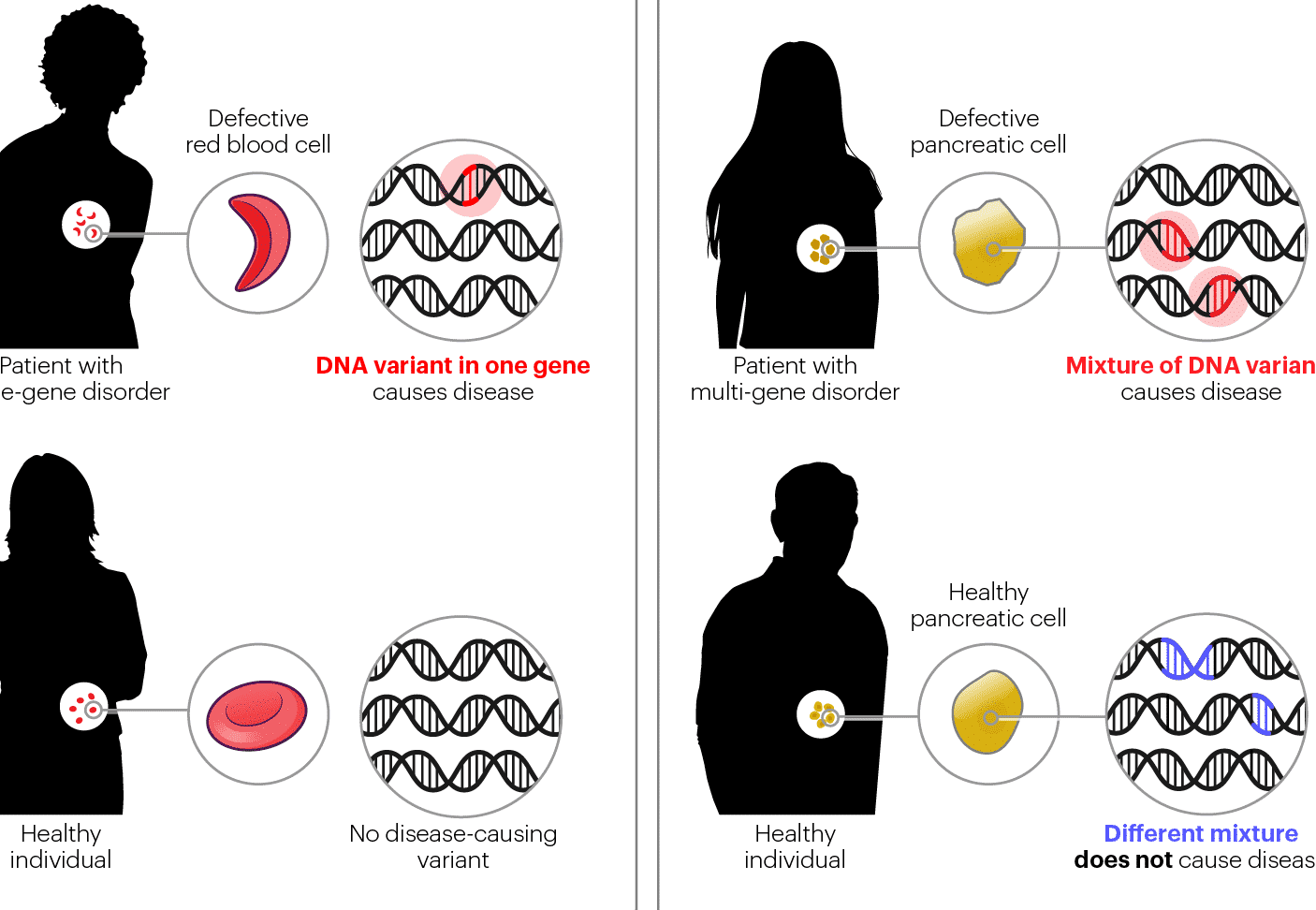
La aplicación más avanzada de el uso de nanopartículas para entregar CRISPR en el cuerpo se encuentra en terapias contra enfermedades genéticas (fibrosis quística, anemia falciforme) y cáncer (silenciamiento de oncogenes). En modelos preclínicos, nanopartículas lipídicas han demostrado éxito corrigiendo mutaciones en hepatocitos y neuronas. Proyectos como el desarrollado por MIT para tratar amiloidosis cardíaca ilustran su potencial traslacional.
5. Futuras direcciones: Personalización y combinación con otras tecnologías
Las perspectivas futuras de el uso de nanopartículas para entregar CRISPR en el cuerpo incluyen sistemas multi-funcionales que integren sensores de respuesta y liberación controlada. Se exploran combinaciones con inteligencia artificial para diseñar partículas adaptadas a perfiles genéticos individuales, así como acoplamientos con terapias inmunomoduladoras para potenciar efectos sinérgicos. La nanotermometría podría permitir activación espaciotemporal precisa mediante estímulos externos (luz, campos magnéticos).
| Tipo de Nanopartícula | Ventaja Principal | Ejemplo de Aplicación |
|---|---|---|
| Liposomas catiónicos | Alta afinidad por membranas celulares | Terapias hepáticas (enfermedad de Hunter) |
| Nanopartículas de oro | Liberación por estímulo lumínico | Edición en tumores superficiales |
| Polímeros dendríticos | Capacidad de carga múltiple | Entrega simultánea de CRISPR y fármacos |
Preguntas Frecuentes
¿Cómo funcionan las nanopartículas para entregar CRISPR en el cuerpo?
Las nanopartículas actúan como vehículos de transporte diseñados para encapsular y proteger los componentes del sistema CRISPR, como el ARN guía y la enzima Cas9. Estas partículas, al ser administradas, evaden el sistema inmunológico y liberan su carga en células específicas, permitiendo una edición genética precisa sin dañar tejidos circundantes.
¿Qué ventajas tienen las nanopartículas sobre otros métodos de entrega de CRISPR?
Las nanopartículas ofrecen ventajas clave como mayor precisión, menor toxicidad y la capacidad de atravesar barreras biológicas, como la membrana celular. Además, pueden ser funcionalizadas con ligandos para dirigirse a tejidos u órganos específicos, superando las limitaciones de métodos tradicionales como los vectores virales.
¿Existen riesgos asociados al uso de nanopartículas para CRISPR?
Aunque prometedoras, las nanopartículas pueden presentar riesgos como toxicidad acumulativa o respuestas inmunitarias no deseadas. La falta de estudios a largo plazo también plantea incógnitas sobre su seguridad y posibles efectos secundarios en la edición génica.
¿En qué etapas se encuentra la investigación actual sobre nanopartículas y CRISPR?
La investigación se centra en ensayos preclínicos y optimización de la eficacia de las nanopartículas, con algunos estudios avanzando hacia ensayos clínicos en humanos. Los esfuerzos actuales buscan mejorar la especificidad y reducir efectos no deseados antes de su aplicación terapéutica generalizada.