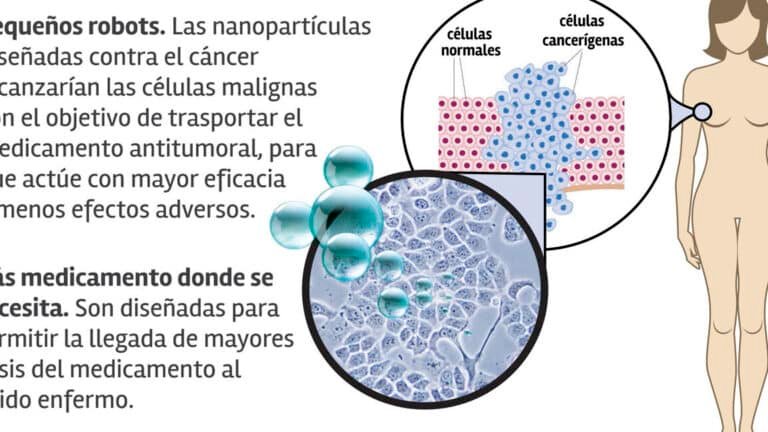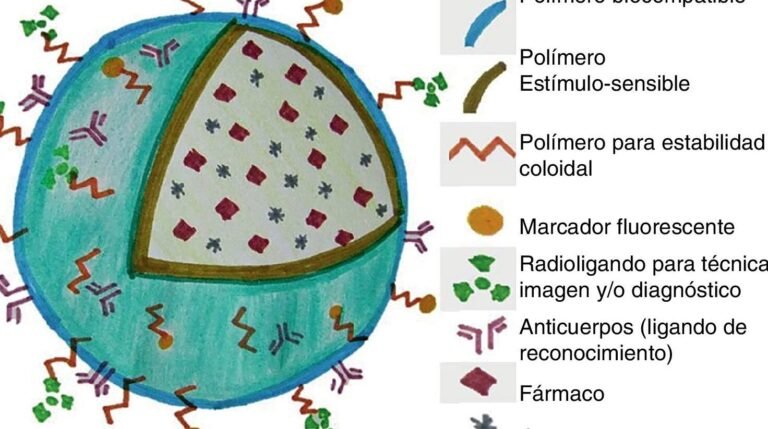
representa un avance revolucionario en la medicina moderna. Estas diminutas estructuras, diseñadas a partir de moléculas de ADN, tienen la capacidad de identificar y atacar tejidos tumorales con precisión sin afectar células sanas. Al inducir la coagulación sanguínea dentro del tumor, los nanorobots logran cortar el suministro de nutrientes, provocando su reducción o eliminación. Esta técnica minimiza los efectos secundarios asociados a tratamientos convencionales, como la quimioterapia, y abre nuevas posibilidades para terapias menos invasivas. El potencial de esta innovación podría transformar el abordaje del cáncer en un futuro cercano.
El uso de nanorobots de ADN para coagular sangre en tumores: Avances y aplicaciones
¿Cómo funcionan los nanorobots de ADN en la coagulación de sangre tumoral?
El uso de nanorobots de ADN para coagular sangre en tumores se basa en estructuras diseñadas para reconocer y unirse a vasos sanguíneos específicos dentro del tumor. Estos dispositivos a escala nanométrica están programados para liberar coagulantes como la trombina, induciendo la formación de trombos que cortan el suministro de oxígeno y nutrientes al tumor, lo que lleva a su necrosis.
Ventajas de los nanorobots de ADN frente a terapias convencionales
Los nanorobots de ADN ofrecen una precisión quirúrgica sin dañar tejidos sanos, a diferencia de la quimioterapia o radioterapia. El uso de nanorobots de ADN para coagular sangre en tumores reduce efectos secundarios sistémicos y permite una mayor acumulación del fármaco en el sitio objetivo, mejorando la eficacia terapéutica.
Ejemplos clínicos y estudios recientes
En 2018, investigadores demostraron en modelos animales que el uso de nanorobots de ADN para coagular sangre en tumores redujo el crecimiento de tumores de mama y melanoma en un 75%. de resultados clave:
| Tipo de tumor | Reducción de tamaño | Tiempo de respuesta |
| Melanoma | 78% | 72 horas |
| Cáncer de mama | 74% | 96 horas |
Desafíos técnicos y limitaciones actuales
A pesar del potencial, el uso de nanorobots de ADN para coagular sangre en tumores enfrenta obstáculos como la estabilidad en circulación, posibles respuestas inmunitarias y escalabilidad en producción. La optimización de la vida media y la capacidad de penetración tumoral siguen siendo áreas de investigación activa.
Futuro y desarrollos en nanomedicina oncológica
Se exploran combinaciones con inmunoterapias y sistemas de liberación controlada. El uso de nanorobots de ADN para coagular sangre en tumores podría integrarse con terapias dirigidas a mutaciones específicas, creando tratamientos personalizados contra el cáncer con menor toxicidad.
Preguntas Frecuentes
¿Cómo funcionan los nanorobots de ADN para coagular sangre en tumores?
Los nanorobots de ADN están diseñados para localizar tumores y liberar fármacos que inducen la coagulación en los vasos sanguíneos que los alimentan. Al bloquear el flujo sanguíneo, privan al tumor de nutrientes y oxígeno, lo que ayuda a reducir su crecimiento.
¿Qué ventajas tienen los nanorobots de ADN frente a otros tratamientos?
La principal ventaja es su precisión, ya que atacan selectivamente los vasos del tumor sin dañar tejidos sanos. Además, su estructura de ADN permite una biodegradabilidad y menor toxicidad comparada con métodos tradicionales.
¿En qué tipos de tumores se puede aplicar esta tecnología?
Esta técnica se está estudiando principalmente en tumores sólidos, como carcinomas, donde los vasos sanguíneos son abundantes. Su eficacia en otros tipos dependerá de futuras investigaciones que evalúen su adaptabilidad.
¿Existen riesgos asociados al uso de nanorobots de ADN en este tratamiento?
Aunque son prometedores, algunos riesgos incluyen posibles respuestas inmunitarias no deseadas o coagulación en zonas no objetivo. Sin embargo, los ensayos clínicos buscan minimizar estos efectos para garantizar su seguridad.