Las nanofábricas moleculares: producción de fármacos in situ representan un avance revolucionario en el campo de la medicina, permitiendo la síntesis de medicamentos directamente en el lugar donde se necesitan. Estas estructuras microscópicas, diseñadas para funcionar como líneas de ensamblaje a escala nanométrica, prometen transformar el tratamiento de enfermedades al garantizar una liberación precisa y controlada de principios activos. Al operar dentro del organismo, las nanofábricas moleculares: producción de fármacos in situ eliminan los desafíos asociados a la distribución y estabilidad de los fármacos tradicionales, abriendo nuevas posibilidades para terapias personalizadas y eficaces contra patologías complejas.
Nanofábricas moleculares: La revolución en la producción de fármacos in situ
¿Qué son las nanofábricas moleculares?
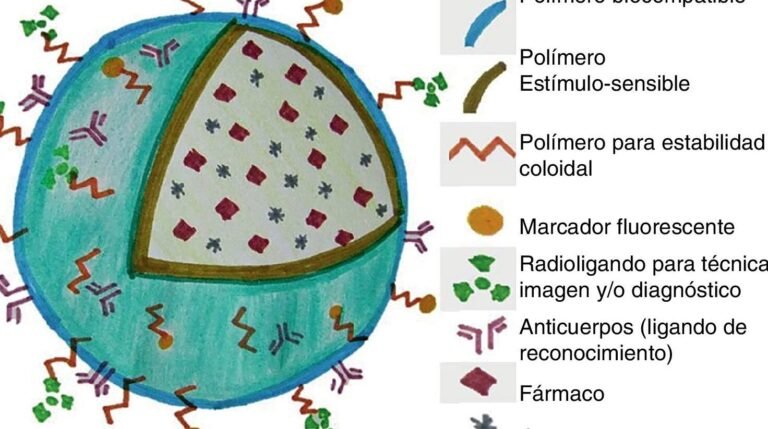
Las nanofábricas moleculares son sistemas nanométricos diseñados para sintetizar compuestos terapéuticos directamente en el lugar de acción dentro del organismo. Estas estructuras imitan procesos biológicos, utilizando enzimas o catalizadores para fabricar fármacos bajo demanda, optimizando así la precisión y reduciendo efectos secundarios. Este enfoque de producción de fármacos in situ minimiza la necesidad de manufactura externa y distribución convencional.
Mecanismos de funcionamiento de las nanofábricas moleculares
Estas nanofábricas operan mediante tres etapas clave: detección de señales bioquímicas, activación de reacciones enzimáticas y liberación controlada del fármaco. Por ejemplo, algunas utilizan nanopartículas sensibles al pH o a proteínas específicas para iniciar la síntesis molecular. La producción de fármacos in situ garantiza concentraciones terapéuticas precisas directamente en tejidos afectados.
Aplicaciones terapéuticas clave
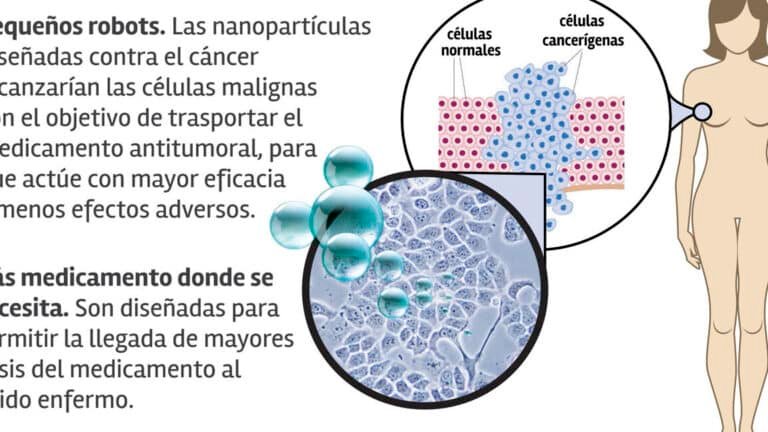
Las nanofábricas moleculares destacan en tratamientos oncológicos, diabetes y enfermedades autoinmunes. En cáncer, por ejemplo, generan agentes citotóxicos solo dentro de tumores, evitando daños a células sanas. Esta capacidad de producción de fármacos in situ también es prometedora para terapias génicas y antibióticos de acción localizada.
Ventajas frente a métodos tradicionales
- Reducción de toxicidad sistémica: Los fármacos actúan solo donde se necesitan.
- Menor dosis requerida: Mayor eficiencia al sintetizarse en el objetivo.
- Estabilidad mejorada: Evita degradación durante almacenamiento o transporte.
La producción de fármacos in situ mediante estas plataformas podría reducir costos logísticos en hasta un 40%.
Desafíos técnicos y futuras direcciones
Pese a su potencial, las nanofábricas moleculares enfrentan retos como el control preciso de reacciones en entornos biológicos variables y la escalabilidad industrial. Investigaciones actuales se centran en mejorar su biocompatibilidad y en integrar inteligencia artificial para optimizar la producción de fármacos in situ.
| Aspecto | Nanofábricas Moleculares | Producción Tradicional |
|---|---|---|
| Localización | Síntesis in situ (cuerpo humano) | Plantas farmacéuticas |
| Personalización | Adaptable a biomarcadores individuales | Dosis estandarizadas |
| Velocidad de actuación | Minutos/horas tras detección | Días (incluye distribución) |
Preguntas Frecuentes
¿Qué son las nanofábricas moleculares y cómo funcionan?
Las nanofábricas moleculares son sistemas nanoscópicos diseñados para producir fármacos directamente en el lugar donde se necesitan, como tejidos o células específicas. Funcionan mediante moléculas programables que ensamblan compuestos terapéuticos in situ, optimizando la eficacia y reduciendo efectos secundarios.
¿Qué ventajas ofrecen las nanofábricas en la producción de medicamentos?
Estas tecnologías permiten una liberación controlada de principios activos, minimizando la degradación prematura y mejorando la precisión terapéutica. Además, reducen costos de fabricación y logística al sintetizar fármacos directamente en el organismo del paciente.
¿Qué tipos de fármacos se pueden producir con nanofábricas moleculares?
Pueden generar desde moléculas pequeñas hasta biologicos complejos, como proteínas o ácidos nucleicos. Su flexibilidad permite adaptarse a tratamientos para cáncer, enfermedades autoinmunes o infecciones, según la programación de sus componentes.
¿Cuáles son los desafíos actuales de esta tecnología?
Los principales retos incluyen garantizar la seguridad y estabilidad de las nanofábricas en el organismo, así como escalar su producción. También se investiga cómo optimizar su especificidad para evitar interacciones no deseadas con tejidos sanos.