Las enfermedades mitocondriales son un grupo de trastornos genéticos complejos que afectan la producción de energía celular, generando síntomas debilitantes y, en muchos casos, irreversibles. En este contexto, cómo la terapia génica aborda las enfermedades mitocondriales se ha convertido en un campo prometedor de investigación médica. Esta innovadora estrategia busca corregir o compensar las mutaciones en el ADN mitocondrial o nuclear, restaurando así la función energética de las células. Aunque los desafíos técnicos y éticos persisten, los avances recientes abren nuevas posibilidades terapéuticas, ofreciendo esperanza a pacientes con estas condiciones hasta ahora incurables.
La terapia génica como solución innovadora para enfermedades mitocondriales
La terapia génica emerge como una estrategia prometedora para tratar las enfermedades mitocondriales, condiciones genéticas complejas que afectan la producción de energía celular. Estas enfermedades, causadas por mutaciones en el ADN mitocondrial o nuclear, tienen consecuencias graves en múltiples órganos. Cómo la terapia génica aborda las enfermedades mitocondriales se centra en técnicas como la edición genómica (CRISPR), trasplante de genes sanos y terapia de reemplazo mitocondrial, buscando corregir o compensar los defectos genéticos subyacentes.
1. Fundamentos de las enfermedades mitocondriales
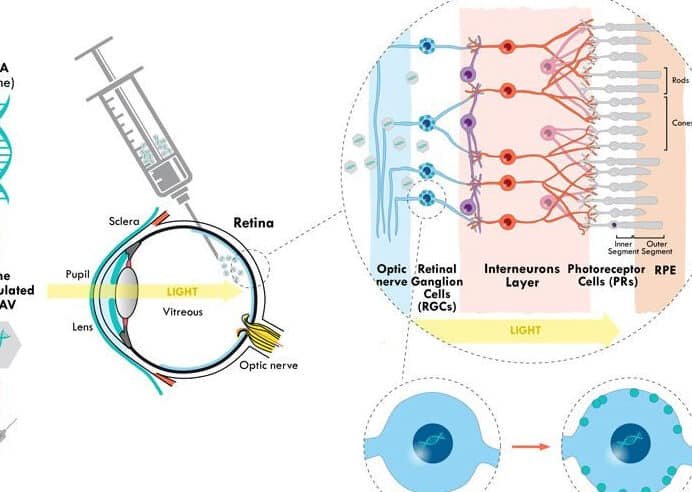
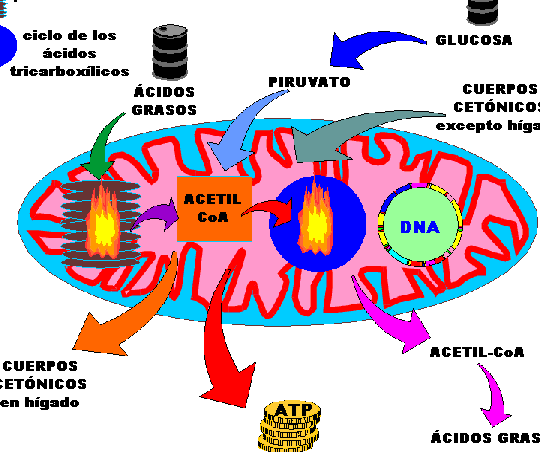
Las enfermedades mitocondriales surgen por fallos en los genes que controlan la función mitocondrial, esencial para la producción de ATP. Estas mutaciones pueden heredarse o aparecer de novo. Cómo la terapia génica aborda las enfermedades mitocondriales implica identificar los genes defectuosos y diseñar vectores (como virus adenoasociados) para introducir copias funcionales en las células afectadas.
2. Técnicas de edición genética aplicadas
Herramientas como CRISPR-Cas9 permiten modificar secuencias defectuosas en el ADN mitocondrial o nuclear. Esta técnica, combinada con sistemas de entrega específicos, facilita la corrección de mutaciones sin afectar el genoma circundante, una piedra angular en cómo la terapia génica aborda las enfermedades mitocondriales.
3. Terapia de reemplazo mitocondrial
Este enfoque implica transferir el núcleo celular de un paciente a un ovocito sano con mitocondrias funcionales, evitando la transmisión de mutaciones. Aunque experimental, representa una aplicación directa de cómo la terapia génica aborda las enfermedades mitocondriales, especialmente en prevención prenatal.
4. Desafíos en la entrega de genes
La barrera de la membrana mitocondrial y el riesgo de efectos off-target son obstáculos críticos. Avances en nanotecnología y vectores virales modificados buscan optimizar la precisión en cómo la terapia génica aborda las enfermedades mitocondriales.
5. Casos de éxito y ensayos clínicos
Ensayos recientes han demostrado mejoras en modelos de síndrome de Leigh y MELAS. Estas investigaciones validan el potencial de cómo la terapia génica aborda las enfermedades mitocondriales, aunque persisten retos regulatorios y de seguridad.
| Técnica | Aplicación | Estado actual |
| CRISPR-Cas9 | Edición de ADN mitocondrial | Fase preclínica |
| Terapia de reemplazo | Prevención de transmisión | Aprobada en algunos países |
| Vectores AAV | Entrega de genes terapéuticos | Ensayos clínicos fase I/II |
Guía detallada: cómo la terapia génica aborda las enfermedades mitocondriales
¿Cómo actúa la terapia génica a nivel molecular para corregir defectos en el ADN mitocondrial?
La terapia génica para corregir defectos en el ADN mitocondrial actúa introduciendo material genético sano o herramientas de edición génica, como nucleasas específicas o vectores virales, directamente en las mitocondrias o el núcleo celular. A nivel molecular, se emplean técnicas como la transferencia de genes nucleares (allotópica) para expresar proteínas mitocondriales funcionales desde el núcleo, o la edición directa del ADN mitocondrial mediante sistemas como CRISPR-Cas9 o TALENs, que cortan y reparan secuencias mutadas. Cómo la terapia génica aborda las enfermedades mitocondriales depende de la estrategia utilizada, ya sea reemplazando, silenciando o corrigiendo el gen defectuoso para restaurar la función energética celular.
Mecanismos de transferencia génica en mitocondrias
La transferencia génica en mitocondrias se realiza mediante vectores virales modificados, como adenovirus o lentivirus, que transportan ADN mitocondrial sano hasta las células afectadas. Alternativamente, se usan nanopartículas lipídicas para entregar moléculas de ARN o ADN sin desencadenar una respuesta inmune. Una vez dentro, el material genético se integra o recombina con el genoma mitocondrial defectuoso, restaurando la producción de ATP y reduciendo el estrés oxidativo.
Técnicas de edición génica aplicadas al ADN mitocondrial
Las técnicas de edición génica, como CRISPR-Cas9 y TALENs, permiten corregir mutaciones específicas en el ADN mitocondrial mediante cortes precisos en la secuencia defectuosa. Estas herramientas se combinan con sistemas de reparación homóloga o no homóloga para insertar copias correctas del gen. Aunque el uso de CRISPR en mitocondrias es complejo debido a la falta de enzimas reparadoras naturales, avances recientes han logrado modular su eficacia mediante vectores mitocondriales especializados.
| Técnica | Objetivo | Ventaja |
|---|---|---|
| CRISPR-Cas9 | Corregir mutaciones puntuales | Alta precisión |
| TALENs | Editar genes largos | Menos efectos off-target |
| Transferencia allotópica | Expresar genes mitocondriales desde el núcleo | Evita la edición directa del ADNmt |
Estrategias para superar las barreras de la terapia génica en mitocondrias
Las barreras principales incluyen la doble membrana mitocondrial y la falta de sistemas de reparación eficientes. Para superarlas, se han desarrollado péptidos de targeting mitocondrial que guían las herramientas génicas hasta su destino, junto con enzimas protectoras que mejoran la estabilidad del ADN reparado. Además, la terapia de reemplazo mitocondrial (MRT) combina citoplasma de donantes sanos con el núcleo del paciente, evitando mutaciones hereditarias. Cómo la terapia génica aborda las enfermedades mitocondriales implica optimizar estos métodos para garantizar seguridad y eficacia a largo plazo.
¿Qué características definen a las enfermedades mitocondriales y por qué representan un desafío para la medicina tradicional?
Las enfermedades mitocondriales son un grupo de trastornos genéticos caracterizados por disfunciones en las mitocondrias, orgánulos responsables de la producción de energía celular. Estas enfermedades presentan una amplia variabilidad clínica, afectando múltiples órganos, especialmente aquellos con alta demanda energética como el cerebro, músculos y corazón. Su heterogeneidad genética y la presencia de ADN mitocondrial (ADNmt) independiente del ADN nuclear complican el diagnóstico y tratamiento, desafiando a la medicina tradicional debido a la falta de terapias curativas y la dificultad para abordar mutaciones en ambos genomas. Cómo la terapia génica aborda las enfermedades mitocondriales es un enfoque prometedor, pero aún en desarrollo, para corregir defectos genéticos subyacentes.
Manifestaciones clínicas de las enfermedades mitocondriales
Las enfermedades mitocondriales pueden manifestarse con síntomas neurológicos, musculares, cardíacos y metabólicos, como debilidad muscular, epilepsia, cardiomiopatías o acidosis láctica. La gravedad varía desde formas leves hasta trastornos multisistémicos fatales en lactantes. La falta de marcadores específicos y la superposición con otras patologías dificultan su identificación, requiriendo pruebas genéticas y bioquímicas especializadas. Cómo la terapia génica aborda las enfermedades mitocondriales podría ofrecer soluciones personalizadas en el futuro.
Desafíos en el diagnóstico y tratamiento
El diagnóstico de las enfermedades mitocondriales es complejo debido a su diversidad genética y fenotípica. Las pruebas tradicionales, como biopsias musculares o estudios enzymáticos, no siempre son concluyentes. Además, las terapias actuales se limitan a manejar síntomas, sin abordar la causa raíz. La medicina tradicional enfrenta limitaciones en la entrega de fármacos a las mitocondrias y en la corrección de mutaciones en el ADNmt.
| Característica | Desafío |
|---|---|
| Heterogeneidad genética | Dificultad para identificar mutaciones específicas |
| Variabilidad fenotípica | Diagnóstico diferencial complejo |
| Doble origen genético (ADNmt y nuclear) | Limitaciones en terapias convencionales |
Avances en investigación y terapias emergentes
La investigación en enfermedades mitocondriales ha avanzado en técnicas de edición genética, como CRISPR/Cas9, y en el desarrollo de terapias de reemplazo mitocondrial. Estos enfoques buscan corregir o compensar las mutaciones defectuosas. Cómo la terapia génica aborda las enfermedades mitocondriales representa una vía innovadora, aunque persisten retos como la entrega eficiente de vectores y la seguridad a largo plazo.
¿En qué casos la terapia génica se aplica específicamente contra la encefalopatía mitocondrial y qué resultados se han observado?
La terapia génica se aplica específicamente en encefalopatías mitocondriales causadas por mutaciones en el ADN mitocondrial (ADNmt) o nuclear, enfocándose en corregir o reemplazar genes defectuosos para restaurar la función mitocondrial. Los resultados observados incluyen mejoras en síntomas neurológicos, reducción de la progresión de la enfermedad y, en algunos casos, aumento de la supervivencia, aunque los avances aún son preliminares y requieren más investigación para garantizar su eficacia y seguridad a largo plazo. Cómo la terapia génica aborda las enfermedades mitocondriales se centra en técnicas como la edición génica CRISPR-Cas9, la transferencia de genes sanos y el uso de vectores virales para entregar material genético funcional.
Mecanismos de acción de la terapia génica en encefalopatías mitocondriales
La terapia génica actúa mediante la corrección directa de mutaciones en el ADNmt o nuclear, utilizando herramientas como CRISPR-Cas9 o enzimas de restricción mitocondriales. También se emplean vectores virales, como adenovirus o lentivirus, para introducir genes funcionales en células afectadas. Estos enfoques buscan restaurar la producción de proteínas esenciales para la cadena respiratoria mitocondrial, mejorando la producción de energía celular y reduciendo el estrés oxidativo.
Resultados clínicos observados en ensayos con terapia génica
En ensayos preclínicos y algunos estudios en humanos, la terapia génica ha demostrado mejoras significativas en parámetros como la función motora, la cognición y la estabilidad metabólica. Por ejemplo, en modelos animales con síndrome de Leigh, se observó una reducción en la neurodegeneración y un aumento de la supervivencia. Sin embargo, los resultados varían según la técnica utilizada y el tipo de mutación, destacando la necesidad de más estudios para consolidar estos hallazgos.
Técnicas avanzadas en terapia génica para enfermedades mitocondriales
Entre las técnicas más prometedoras se encuentran la transferencia de genes mitocondriales sanos (allotopic expression), la edición basada en nucleasas y el uso de vectores AAV para targeting específico. A continuación, se presenta una comparación de estas técnicas:
| Técnica | Ventajas | Desafíos |
|---|---|---|
| Allotopic expression | Reemplazo directo de genes defectuosos | Baja eficiencia de entrega |
| CRISPR-Cas9 | Precisión en la edición génica | Riesgo de off-target effects |
| Vectores AAV | Seguridad y especificidad tisular | Limitación en tamaño del gen |
¿Cómo funciona la terapia de reemplazo mitocondrial y en qué tipo de pacientes con enfermedades mitocondriales está indicada?
La terapia de reemplazo mitocondrial (TRM) es una técnica de reproducción asistida que busca prevenir la transmisión de enfermedades mitocondriales hereditarias al reemplazar las mitocondrias defectuosas del óvulo o embrión de la madre por mitocondrias sanas de una donante. Este enfoque está indicado en pacientes con mutaciones patogénicas en el ADN mitocondrial (ADNmt), especialmente en mujeres portadoras de enfermedades graves como el síndrome de Leigh, la neuropatía óptica hereditaria de Leber (LHON) o la epilepsia mioclónica con fibras rojas rasgadas (MERRF). La TRM incluye métodos como la transferencia pronuclear o la transferencia de huso materno, y se aplica principalmente en casos donde existe un alto riesgo de transmitir trastornos mitocondriales incapacitantes o mortales a la descendencia. Cómo la terapia génica aborda las enfermedades mitocondriales también es un área de investigación prometedora, aunque la TRM sigue siendo la opción más avanzada para evitar la herencia de estas condiciones.
Métodos utilizados en la terapia de reemplazo mitocondrial
Los dos métodos principales en la terapia de reemplazo mitocondrial son la transferencia pronuclear y la transferencia de huso materno. En la primera, se fertilizan tanto el óvulo de la madre como el de la donante, y los pronúcleos (que contienen el ADN nuclear) del embrión afectado se transfieren al embrión de la donante, cuyo núcleo ha sido removido. En el segundo método, el huso mitótico (que contiene los cromosomas) del óvulo de la madre se transfiere a un óvulo de donante sin huso, preservando así el ADN nuclear materno mientras se reemplazan las mitocondrias defectuosas. Ambos métodos requieren técnicas de fecundación in vitro (FIV) y están sujetos a rigurosos protocolos éticos y legales.
Enfermedades mitocondriales tratables con TRM
La terapia de reemplazo mitocondrial está indicada para enfermedades causadas por mutaciones en el ADNmt, como el síndrome de Leigh, la encefalomiopatía mitocondrial (MELAS), y la neuropatía óptica hereditaria de Leber (LHON). Estas condiciones afectan principalmente órganos con alta demanda energética, como el cerebro, los músculos y el corazón, y suelen ser progresivas y debilitantes. La TRM ofrece una solución preventiva para parejas con riesgo de transmitir estas enfermedades, aunque no es aplicable en pacientes ya afectados, ya que solo actúa a nivel embrionario.
| Enfermedad | Síntomas principales | Gen afectado |
|---|---|---|
| Síndrome de Leigh | Degeneración neurológica, retraso psicomotor | MT-ATP6, entre otros |
| MELAS | Accidentes cerebrovasculares, convulsiones, miopatía | MT-TL1 |
| LHON | Pérdida bilateral de visión | MT-ND4, MT-ND6 |
Consideraciones éticas y legales de la TRM
La terapia de reemplazo mitocondrial plantea desafíos éticos y legales, como la modificación genética de la línea germinal y los derechos de la donante mitocondrial. En algunos países, como el Reino Unido, la TRM está legalmente permitida bajo estrictas regulaciones, mientras que en otros está prohibida debido a preocupaciones sobre la manipulación genética. Además, existen debates sobre el estatus jurídico de los niños nacidos mediante TRM, ya que tienen material genético de tres individuos: los padres nucleares y la donante mitocondrial. Cómo la terapia génica aborda las enfermedades mitocondriales podría ofrecer alternativas menos controvertidas en el futuro.
Preguntas Frecuentes
¿Qué es la terapia génica y cómo puede tratar enfermedades mitocondrialess?
La terapia génica es una técnica innovadora que busca corregir o reemplazar genes defectuosos causantes de enfermedades. En el caso de las enfermedades mitocondriales, esta terapia puede dirigirse a modificar el ADN mitocondrial o nuclear para restaurar la función energética de las células afectadas.
¿Cuáles son los principales enfoques de la terapia génica para enfermedades mitocondriales?
Los enfoques incluyen la edición genética con herramientas como CRISPR, la transferencia de genes sanos para compensar los defectuosos y la eliminación selectiva de ADN mitocondrial dañado. Estas estrategias buscan mejorar la producción de energía celular y reducir los síntomas.
¿Qué desafíos presenta la terapia génica en enfermedades mitocondriales?
Entre los principales desafíos están la barrera de la membrana mitocondrial, que dificulta la entrega de terapias, la posibilidad de efectos off-target en la edición genética y la necesidad de técnicas más precisas para modificar el ADN mitocondrial sin afectar el nuclear.
¿Existen ya terapias génicas aprobadas para enfermedades mitocondriales?
Actualmente, no hay terapias génicas aprobadas específicamente para enfermedades mitocondriales, pero varias están en ensayos clínicos. La investigación avanza rápidamente, centrándose en enfoques como la sustitución mitocondrial y la terapia de ARN de transferencia (ARNt).