ha revolucionado el campo de la medicina regenerativa y la investigación biomédica. Estas células, generadas mediante la reprogramación de células adultas, poseen la capacidad de diferenciarse en cualquier tipo celular del organismo, ofreciendo oportunidades sin precedentes para el estudio de enfermedades, el desarrollo de terapias personalizadas y la regeneración de tejidos dañados. Su versatilidad y ética, al evitar el uso de embriones, las convierten en una herramienta prometedora para la ciencia. Este artículo explora los avances, desafíos y futuras aplicaciones de las células iPS, destacando su impacto transformador en la salud humana.
El potencial de las células iPS (Pluripotentes inducidas) en la medicina regenerativa
1. ¿Qué son las células iPS (Pluripotentes inducidas)?
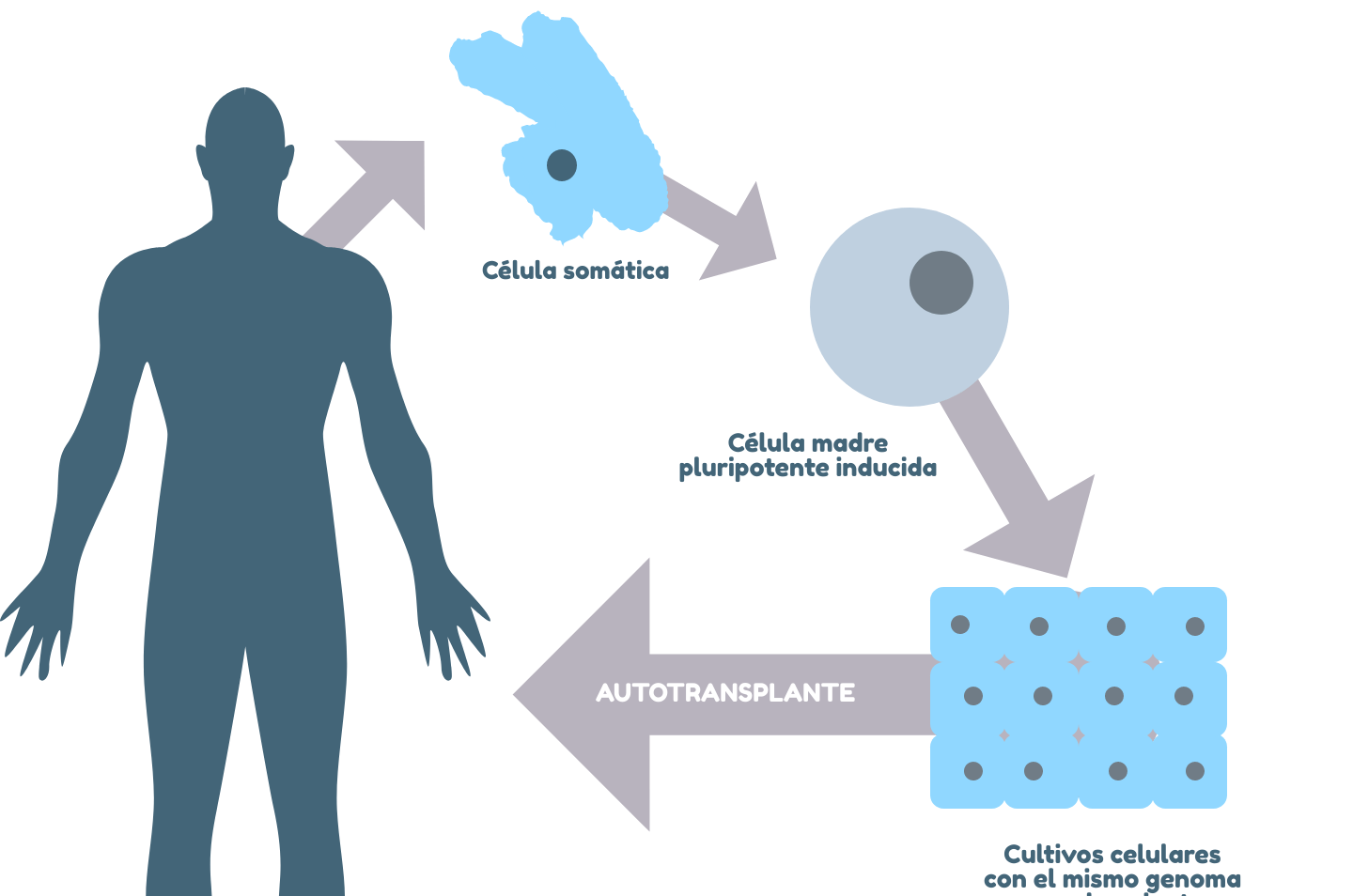
Las células iPS (Pluripotentes inducidas) son un tipo de célula madre creada mediante la reprogramación genética de células adultas, como las de la piel o la sangre, para que adquieran propiedades similares a las células madre embrionarias. Este proceso, descubierto por el científico Shinya Yamanaka en 2006, permite que estas células se diferencien en casi cualquier tipo de tejido del cuerpo humano. El potencial de las células iPS (Pluripotentes inducidas) radica en su capacidad para revolucionar terapias médicas sin los dilemas éticos asociados a las células embrionarias.
2. Aplicaciones terapéuticas de las células iPS
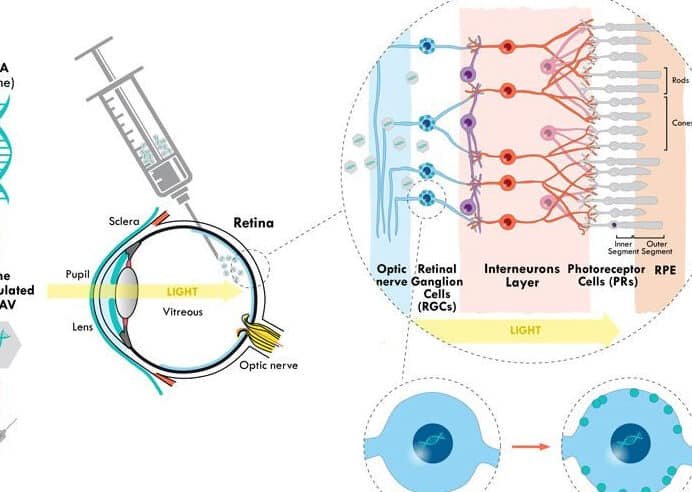
El potencial de las células iPS (Pluripotentes inducidas) se refleja en su amplio rango de aplicaciones. Estas células pueden utilizarse para regenerar tejidos dañados en enfermedades como Parkinson, diabetes o infartos. Además, permiten el desarrollo de modelos de enfermedades in vitro para probar fármacos de manera más precisa. Su uso en medicina personalizada también es destacable, ya que pueden generarse a partir del propio paciente, reduciendo el riesgo de rechazo en trasplantes.
3. Ventajas frente a otras células madre
A diferencia de las células madre embrionarias, las células iPS (Pluripotentes inducidas) no requieren la destrucción de embriones, evitando controversias éticas. También superan a las células madre adultas en versatilidad, ya que pueden convertirse en cualquier tipo celular. El potencial de las células iPS (Pluripotentes inducidas) incluye su capacidad de ser producidas a partir del paciente, minimizando problemas de compatibilidad inmunológica.
4. Desafíos y limitaciones actuales
A pesar de el potencial de las células iPS (Pluripotentes inducidas), existen desafíos técnicos y de seguridad que deben superarse. La reprogramación celular puede generar mutaciones no deseadas, y existe el riesgo de formación de tumores si las células no se diferencian correctamente. Además, los costos y el tiempo requerido para su producción siguen siendo altos, limitando su aplicación clínica masiva.
5. Futuro de la investigación con células iPS
La investigación en células iPS (Pluripotentes inducidas) avanza hacia métodos más seguros y eficientes de reprogramación celular. Se exploran técnicas para mejorar la pureza y estabilidad de estas células, así como su aplicación en bioimpresión 3D de órganos. El potencial de las células iPS (Pluripotentes inducidas) podría transformar la medicina en las próximas décadas, ofreciendo soluciones a enfermedades actualmente incurables.
| Aspecto | Descripción |
|---|---|
| Origen | Células adultas reprogramadas |
| Potencial | Diferenciación en múltiples tipos celulares |
| Aplicaciones | Medicina regenerativa, farmacología, investigación |
| Ventaja principal | Sin controversias éticas como las células embrionarias |
| Retos | Seguridad, eficiencia de producción, costos |
Preguntas Frecuentes
¿Qué son las células iPS y por qué son importantes?
Las células iPS (pluripotentes inducidas) son células adultas reprogramadas para adquirir propiedades similares a las células madre embrionarias, lo que les permite diferenciarse en cualquier tipo de tejido. Su importancia radica en su potencial para la medicina regenerativa, modelos de enfermedades y terapias personalizadas sin los dilemas éticos asociados a las células embrionarias.
¿Cómo se generan las células iPS?
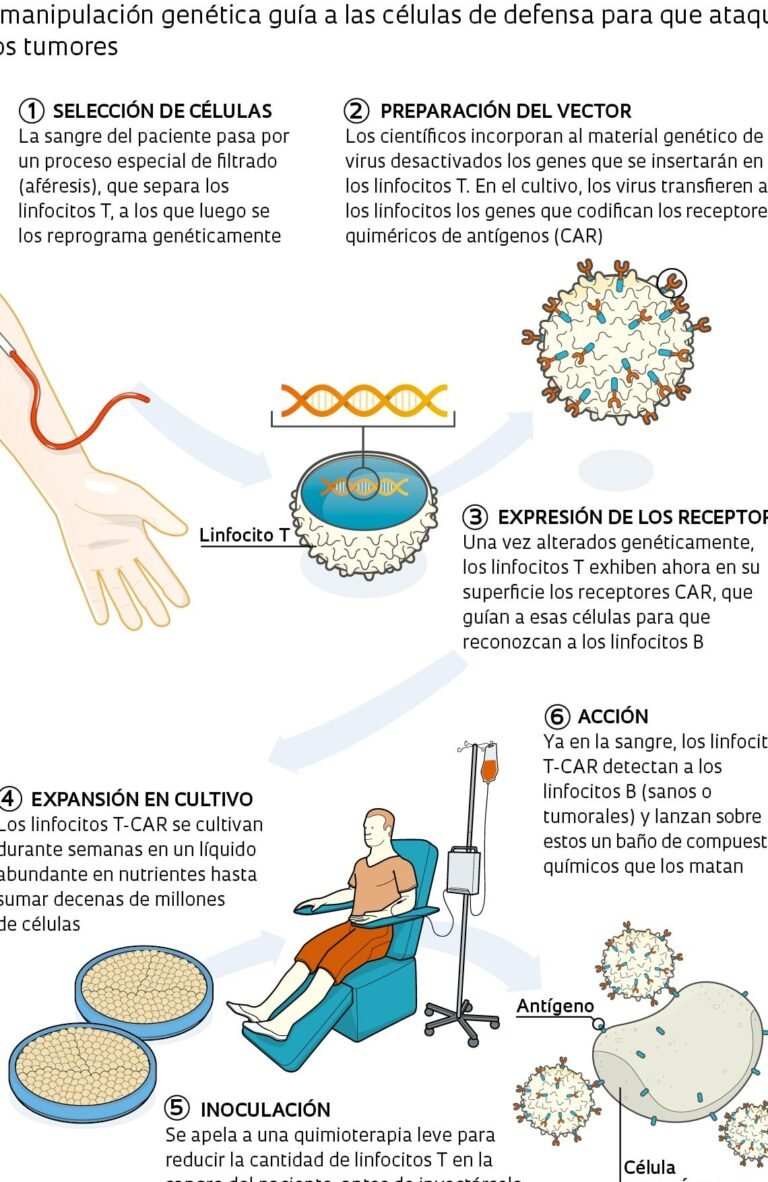
Las células iPS se producen introduciendo genes específicos (como Oct4, Sox2, Klf4 y c-Myc) en células somáticas adultas, mediante vectores virales o métodos no virales, que las reprograman a un estado pluripotente. Este proceso elimina la necesidad de usar embriones, aunque aún presenta desafíos técnicos y de seguridad.
¿Cuáles son las aplicaciones médicas de las células iPS?
Las aplicaciones incluyen regeneración de tejidos (como corazón, hígado o neuronas), farmacología personalizada y modelado de enfermedades para probar fármacos. También se investiga su uso en terapias para patologías como Parkinson, diabetes o lesiones medulares, aunque su implementación clínica aún está en etapas experimentales.
¿Qué desafíos enfrentan las células iPS en la investigación actual?
Los principales retos son garantizar su seguridad (evitando mutaciones o formación de tumores), mejorar la eficiencia de reprogramación y escalar su producción para uso clínico. Además, se buscan métodos alternativos para reducir costos y simplificar los protocolos de diferenciación celular.