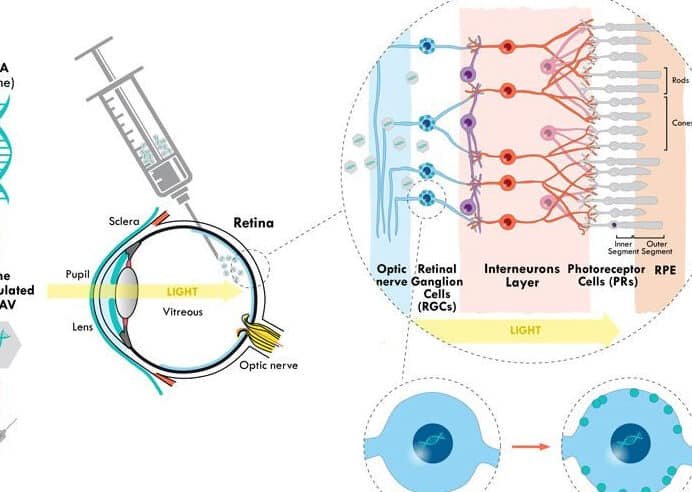
representa uno de los mayores desafíos en la medicina moderna. La complejidad de la barrera hematoencefálica, junto con la delicada estructura neuronal, dificulta la administración eficiente y segura de terapias génicas. A pesar de los avances en vectores virales y sistemas no virales, persisten obstáculos como la especificidad celular, la respuesta inmune y la durabilidad del efecto terapéutico. Este artículo explora las estrategias innovadoras en desarrollo, desde nanopartículas hasta técnicas quirúrgicas avanzadas, que buscan superar estas limitaciones y abrir nuevas puertas para el tratamiento de enfermedades neurológicas mediante la modificación genética.
El reto de la entrega de genes en el cerebro humano: Barreras y avances
La terapia génica aplicada al cerebro humano enfrenta desafíos únicos debido a la complejidad del sistema nervioso central y las barreras protectoras naturales, como la barrera hematoencefálica. El reto de la entrega de genes en el cerebro humano radica en superar estos obstáculos para garantizar la eficacia y seguridad de los tratamientos. A continuación, se exploran los aspectos clave de este reto científico.
1. La barrera hematoencefálica como obstáculo principal
La barrera hematoencefálica (BHE) es una capa de células endoteliales altamente especializadas que protege al cerebro de toxinas y patógenos, pero también dificulta la administración de terapias génicas. Superar esta barrera requiere métodos innovadores, como vectores virales modificados o sistemas de administración nanotecnológicos, para asegurar que los genes terapéuticos alcancen su objetivo.
2. Vectores virales y no virales en la entrega génica
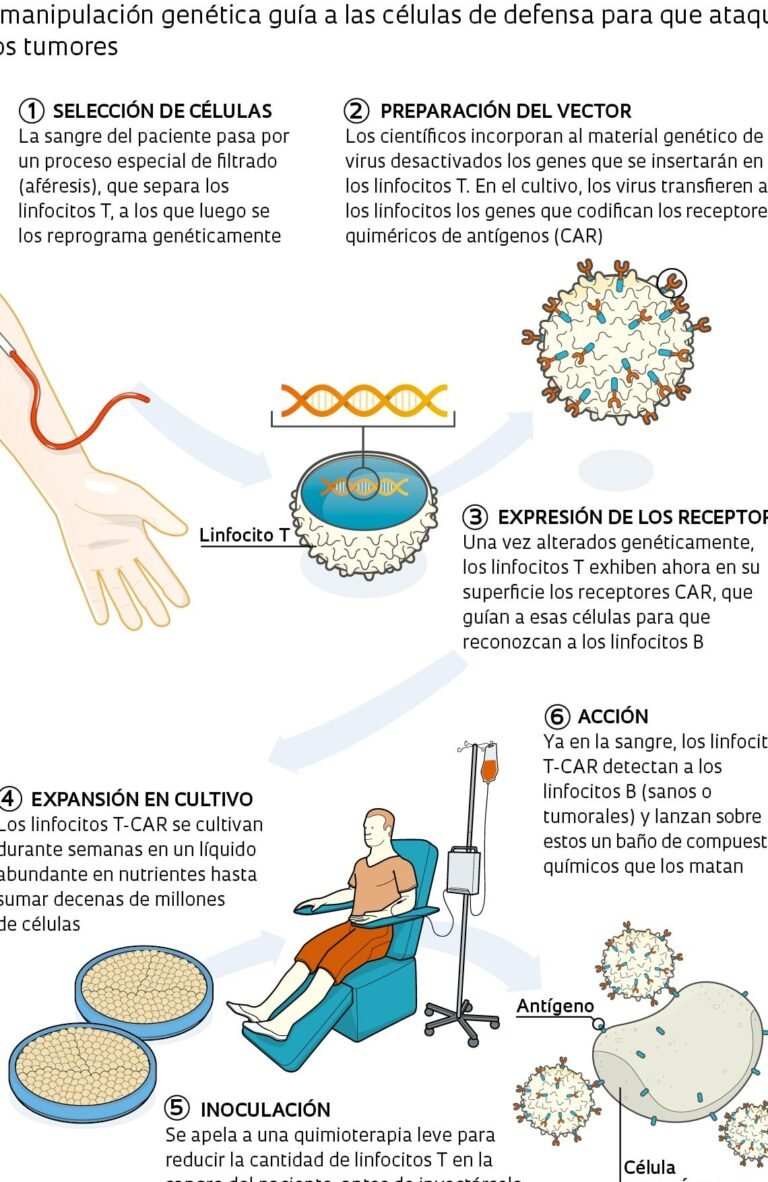
Para abordar el reto de la entrega de genes en el cerebro humano, se emplean tanto vectores virales (por ejemplo, adenovirus o lentivirus) como no virales (como liposomas o polímeros). Cada enfoque tiene ventajas y limitaciones en términos de eficiencia, especificidad y posibles respuestas inmunitarias. La elección del vector depende del tipo de terapia y del área cerebral a tratar.
3. Seguridad y efectos adversos potenciales
La seguridad es un aspecto crítico al tratar el cerebro humano. Insercciones génicas incorrectas o respuestas inmunitarias pueden provocar inflamación o efectos neurológicos no deseados. Por ello, las investigaciones actuales se centran en mejorar la precisión de los vectores y reducir riesgos asociados con el reto de la entrega de genes en el cerebro humano.
4. Avances en técnicas de administración dirigida
Métodos como la administración intracerebral directa o el uso de nanopartículas funcionalizadas han demostrado avances prometedores. Estas tecnologías permiten una liberación controlada y localizada de material génico, minimizando daños a tejidos circundantes y aumentando la eficacia del tratamiento.
5. Perspectivas futuras y ensayos clínicos
Los ensayos clínicos en fase experimental están evaluando terapias génicas para enfermedades neurodegenerativas, como el Parkinson y el Alzheimer. Aunque persiste el reto de la entrega de genes en el cerebro humano, los resultados preliminares ofrecen esperanza para tratamientos revolucionarios en la próxima década.
| Aspecto clave | Desafío asociado | Tecnología emergente |
|---|---|---|
| Barrera hematoencefálica | Limitación en la permeabilidad | Nanopartículas con ligandos específicos |
| Especificidad celular | Daño a células no objetivo | Vectores con promotores tejido-específicos |
| Respuesta inmunitaria | Inactivación de vectores | Modificación de cápsides virales |
Preguntas Frecuentes
¿Cuáles son los principales obstáculos para la entrega de genes en el cerebro humano?
Los principales obstáculos incluyen la barrera hematoencefálica, que dificulta el paso de vectores génicos, la especificidad celular requerida para evitar efectos off-target, y la respuesta inmune que puede neutralizar los vectores antes de alcanzar su destino.
¿Qué métodos se utilizan actualmente para superar la barrera hematoencefálica en la terapia génica?
Se emplean técnicas como inyección intracerebral directa, el uso de vectores virales modificados (ej.: AAV) con tropismo neuronal, y métodos físicos como ultrasonido focalizado para abrir temporalmente la barrera.
¿Qué tipos de vectores génicos son más prometedores para el cerebro humano?
Los vectores virales adenoasociados (AAV) destacan por su seguridad y capacidad de transducir neuronas, aunque se investigan alternativas como nanopartículas lipídicas para mejorar la capacidad de carga y reducir la inmunogenicidad.
¿Cómo se evalúa la eficacia y seguridad de las terapias génicas en el cerebro?
Mediante ensayos clínicos en fases que miden la expresión génica, efectos adversos y mejoras funcionales, apoyados por técnicas de imagen cerebral y biomarcadores específicos para monitorizar el impacto terapéutico.