ha revolucionado la investigación biomédica en los últimos años. Estas células, generadas mediante la reprogramación de células adultas a un estado pluripotente, ofrecen un potencial sin precedentes para estudiar mecanismos patológicos y desarrollar tratamientos personalizados. Al permitir la creación de modelos celulares específicos de pacientes, las células iPS facilitan el análisis de enfermedades complejas y la prueba de fármacos in vitro. Además, su aplicación en terapias regenerativas abre nuevas esperanzas para abordar patologías hasta ahora incurables. Este artículo explora los avances, desafíos y perspectivas futuras de el uso de células iPS para modelos de enfermedades y terapia en la medicina contemporánea.
El uso de células iPS para modelos de enfermedades y terapia: Avances y aplicaciones
El uso de células iPS para modelos de enfermedades y terapia ha revolucionado la investigación biomédica al permitir la generación de células pluripotentes inducidas (iPS) a partir de células adultas, como fibroblastos o células sanguíneas. Estas células pueden diferenciarse en cualquier tipo celular del cuerpo humano, lo que facilita el estudio de enfermedades complejas, el desarrollo de fármacos y la terapia celular personalizada.
1. ¿Qué son las células iPS y cómo se generan?
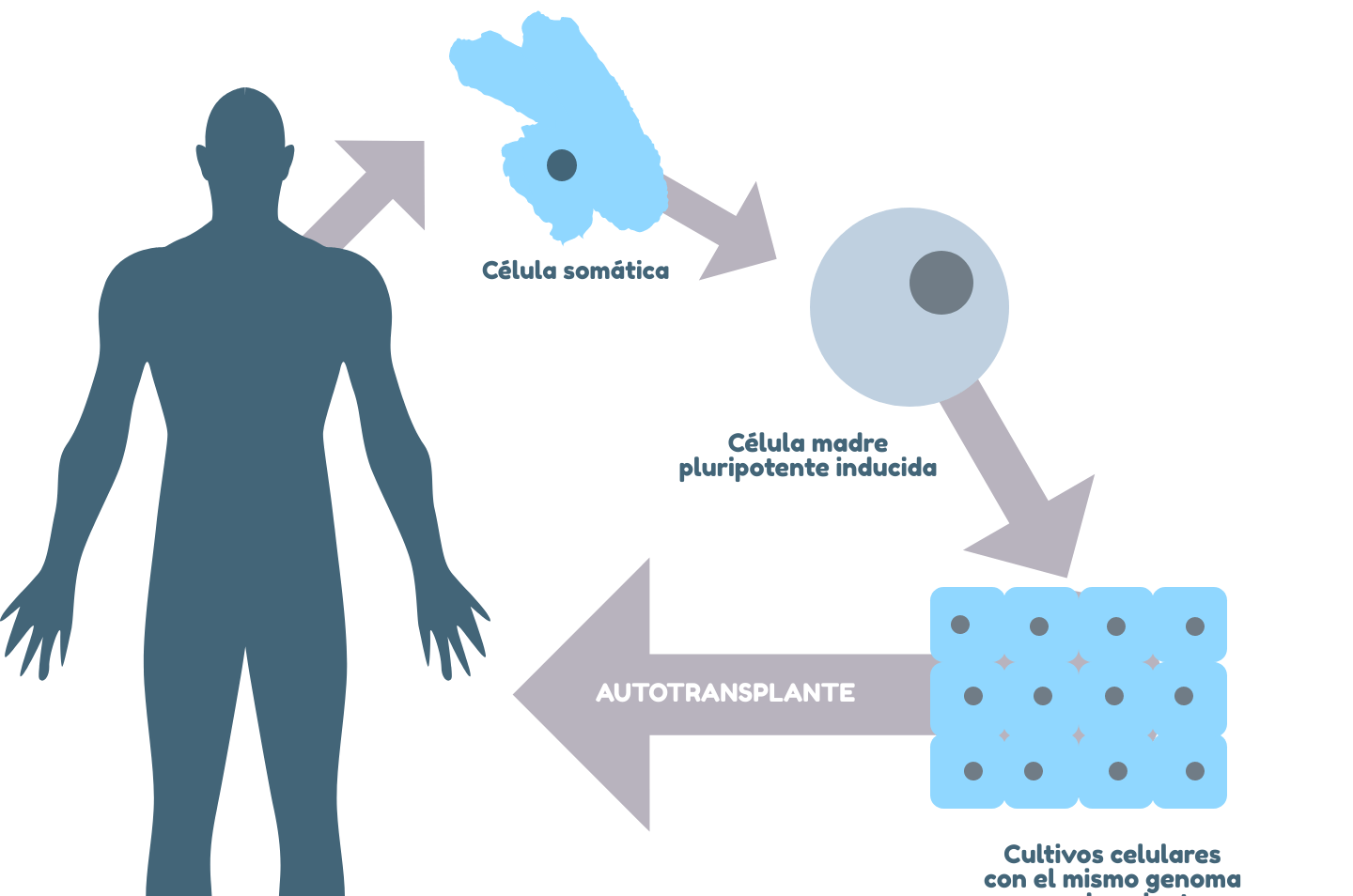
Las células iPS (células pluripotentes inducidas) son células adultas reprogramadas para adquirir propiedades similares a las células madre embrionarias. Mediante la de factores de transcripción específicos (como Oct4, Sox2, Klf4 y c-Myc), se logra revertir su estado maduro a un estado pluripotente. Este proceso permite el uso de células iPS para modelos de enfermedades y terapia al proporcionar una fuente ilimitada de células específicas del paciente.
2. Aplicaciones en modelado de enfermedades
El uso de células iPS para modelos de enfermedades y terapia incluye la creación de modelos in vitro de patologías como Parkinson, Alzheimer o diabetes. Estas células pueden diferenciarse en neuronas, cardiomiocitos u otros tejidos afectados, replicando las características moleculares y fisiológicas de la enfermedad. Esto facilita el estudio de mecanismos patogénicos y la identificación de posibles dianas terapéuticas.
3. Terapia celular y medicina regenerativa
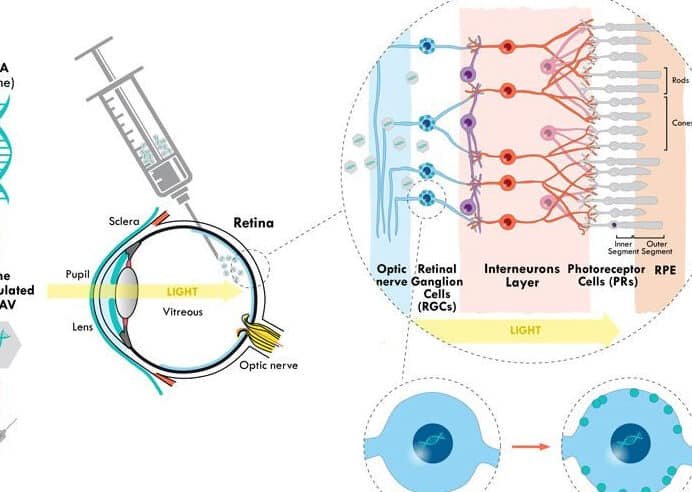
En el ámbito terapéutico, el uso de células iPS para modelos de enfermedades y terapia promueve enfoques innovadores, como la regeneración de tejidos dañados. Por ejemplo, se han realizado ensayos clínicos para trasplantes de retina derivada de iPS en pacientes con degeneración macular, mostrando resultados prometedores en la recuperación de la visión.
4. Retos y limitaciones actuales
A pesar de su potencial, el uso de células iPS para modelos de enfermedades y terapia enfrenta desafíos, como el riesgo de formación de tumores debido a la reprogramación incompleta, la variabilidad en la calidad de las líneas celulares y los altos costos de producción. Además, se requiere optimizar protocolos de diferenciación para garantizar seguridad y eficacia en aplicaciones clínicas.
5. Futuras direcciones en investigación
El futuro del uso de células iPS para modelos de enfermedades y terapia se centra en mejorar las técnicas de edición genética (como CRISPR/Cas9) para corregir mutaciones, desarrollar bancos de líneas iPS compatibles con diferentes genotipos y optimizar protocolos de producción a gran escala. Estas innovaciones podrían acelerar su implementación en terapias personalizadas.
| Aplicación | Ventaja | Ejemplo |
| Modelado de enfermedades | Estudio de mecanismos sin necesidad de biopsias invasivas | Neuronas derivadas de iPS para Parkinson |
| Terapia celular | Personalización y reducción de rechazo inmunológico | Trasplante de retinocitos en degeneración macular |
| Desarrollo de fármacos | Pruebas de toxicidad y eficacia en células humanas | Cardiomiocitos para evaluar cardiotoxicidad |
Preguntas Frecuentes
¿Qué son las células iPS y cómo se utilizan en modelos de enfermedades?
Las células iPS (células madre pluripotentes inducidas) son células adultas reprogramadas para adquirir propiedades similares a las células madre embrionarias. En los modelos de enfermedades, permiten estudiar mecanismos patológicos, probar fármacos y personalizar terapias al derivarlas de pacientes con condiciones específicas.
¿Qué ventajas ofrecen las células iPS frente a otros modelos de investigación?
Las células iPS superan limitaciones éticas y técnicas de otros modelos, como el uso de embriones o animales, ya que pueden generarse directamente de tejidos humanos. Además, permiten recrear enfermedades complejas en laboratorio, manteniendo la carga genética del paciente para mayor precisión.
¿Cómo contribuyen las células iPS al desarrollo de terapias personalizadas?
Al generarse a partir de células del propio paciente, las células iPS facilitan el diseño de terapias personalizadas, evitando rechazo inmunológico. Se usan para probar fármacos in vitro, corregir mutaciones con edición génica (como CRISPR) y generar tejidos compatibles para trasplantes.
¿Cuáles son los principales desafíos en el uso de células iPS para terapias?
Los retos incluyen garantizar su seguridad (evitar mutaciones durante la reprogramación), escalar su producción para aplicaciones clínicas y reducir costos. Además, se requiere validar su eficacia en ensayos clínicos antes de su implementación masiva en medicina regenerativa.