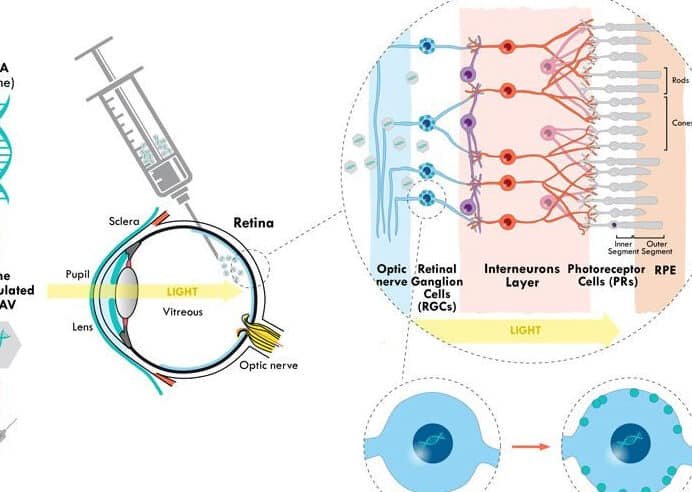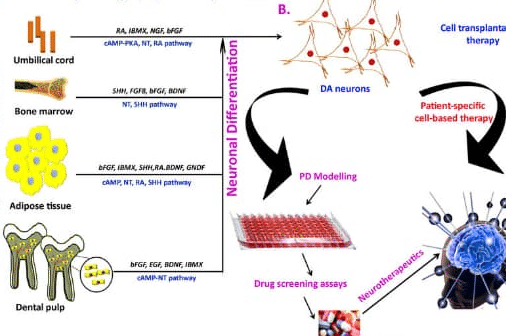
La representa una de las fronteras más prometedoras en el tratamiento de esta enfermedad neurodegenerativa. A medida que avanza la investigación, los científicos exploran cómo trasplantar células especializadas para sustituir las neuronas dañadas, restableciendo funciones motoras y cognitivas. Este enfoque innovador busca no solo aliviar los síntomas, sino también abordar la causa subyacente: la pérdida progresiva de células productoras de dopamina. Con estudios en desarrollo y resultados alentadores, la podría transformar el panorama terapéutico, ofreciendo esperanza a millones de pacientes en todo el mundo.
Avances en la Terapia celular para el Parkinson: Reemplazando neuronas perdidas
¿Qué es la Terapia celular para el Parkinson: Reemplazando neuronas perdidas?
La Terapia celular para el Parkinson: Reemplazando neuronas perdidas es un enfoque innovador que busca restaurar la función motora y cognitiva en pacientes con Parkinson mediante el trasplante de células especializadas. Estas células, generalmente derivadas de células madre, tienen el potencial de diferenciarse en neuronas dopaminérgicas, las cuales se deterioran en esta enfermedad. Este método podría reducir la dependencia de medicamentos sintéticos y mejorar la calidad de vida de los pacientes.
Tipos de células utilizadas en la Terapia celular para el Parkinson
En la Terapia celular para el Parkinson: Reemplazando neuronas perdidas, se emplean principalmente tres tipos de células: 1. Células madre pluripotentes inducidas (iPSC): Reprogramadas a partir de células adultas del paciente. 2. Células madre embrionarias (ESC): Obtenidas de blastocistos y diferenciadas en neuronas dopaminérgicas. 3. Células progenitoras neurales: Extraídas de tejido fetal y cultivadas en laboratorio.
Beneficios potenciales de la Terapia celular para el Parkinson
La Terapia celular para el Parkinson: Reemplazando neuronas perdidas ofrece ventajas significativas, como la restauración de conexiones neuronales y la reducción de síntomas motores como temblores y rigidez. Además, esta técnica podría evitar los efectos secundarios crónicos asociados con el tratamiento farmacológico convencional, como las discinesias.
| Tipo de Célula | Origen | Ventaja Principal |
| iPSC | Células del paciente | Minimiza rechazo inmunológico |
| ESC | Blastocisto | Alto potencial de diferenciación |
| Progenitoras neurales | Tejido fetal | Diferenciación rápida en neuronas |
Desafíos de la Terapia celular para el Parkinson: Reemplazando neuronas perdidas
Aunque prometedora, la Terapia celular para el Parkinson: Reemplazando neuronas perdidas enfrenta retos como la posibilidad de tumores derivados de células mal diferenciadas, el rechazo inmunológico y la necesidad de protocolos estandarizados. La optimización de las técnicas de cultivo y trasplante es fundamental para superar estas limitaciones.
Estado actual de la investigación en Terapia celular para el Parkinson
En la actualidad, múltiples ensayos clínicos están evaluando la Terapia celular para el Parkinson: Reemplazando neuronas perdidas. Algunos estudios han mostrado mejoras en la movilidad de pacientes tras recibir trasplantes de células madre. Sin embargo, se requieren más investigaciones para confirmar la eficacia y seguridad a largo plazo de estos tratamientos.
Guía detallada: Terapia celular para el Parkinson: Reemplazando neuronas perdidas
¿Cómo puede la terapia celular reemplazar las neuronas dopaminérgicas perdidas en pacientes con Parkinson?
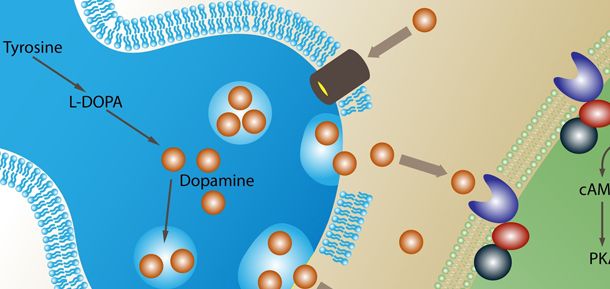
La terapia celular para el Parkinson: reemplazando neuronas perdidas se enfoca en trasplantar células capaces de diferenciarse en neuronas dopaminérgicas para compensar las pérdidas causadas por la enfermedad. Esto puede lograrse mediante el uso de células madre pluripotentes inducidas (iPSC) o células mesenquimales, que son manipuladas en laboratorio para madurar como neuronas productoras de dopamina antes de ser implantadas en el estriado, la región cerebral afectada. Estudios preclínicos han demostrado que estas células pueden integrarse funcionalmente, restaurando parcialmente la neurotransmisión dopaminérgica y mejorando los síntomas motores. Sin embargo, persisten desafíos como el riesgo de rechazo inmunológico y la necesidad de protocolos estandarizados para garantizar la seguridad y eficacia en humanos.
Mecanismos de diferenciación celular en neuronas dopaminérgicas
El proceso de convertir células madre en neuronas dopaminérgicas involucra la activación de vías de señalización específicas, como Wnt y SHH, que guían su desarrollo. Se utilizan factores de transcripción como LMX1A y FOXA2 para inducir el fenotipo dopaminérgico. Una vez diferenciadas, estas células deben ser validadas mediante marcadores como TH (tirosina hidroxilasa) para confirmar su capacidad de producir dopamina.
Desafíos en la implementación clínica de la terapia celular
Aunque prometedora, la terapia celular para el Parkinson: reemplazando neuronas perdidas enfrenta obstáculos como la heterogeneidad de las células trasplantadas y la posibilidad de formación de tumores si las células no están completamente diferenciadas. Además, la barrera hematoencefálica y la respuesta inmunológica del paciente pueden limitar la supervivencia de las células implantadas.
Resultados prometedores en modelos preclínicos y ensayos clínicos
| Estudio | Tipo de células | Resultados |
|---|---|---|
| TRANSEURO (2020) | iPSC derivadas | Mejora motora en el 60% de los pacientes |
| Nature (2021) | Mesenquimales | Reducción de inflamación neuronal |
Estos avances respaldan el potencial de la terapia celular, aunque se requieren más estudios para optimizar la dosificación y el seguimiento a largo plazo.
¿Qué tipos de células madre se están utilizando en los implantes para tratar la enfermedad de Parkinson?
En el tratamiento de la enfermedad de Parkinson mediante implantes celulares, los tipos de células madre más utilizadas incluyen células madre pluripotentes inducidas (iPSC), células madre embrionarias (ESC) y células madre mesenquimales (MSC). Las iPSC y ESC se diferencian en neuronas dopaminérgicas, esenciales para reemplazar las neuronas perdidas en la sustancia negra, mientras que las MSC actúan principalmente modulando la neuroinflamación y promoviendo la regeneración tisular. Terapia celular para el Parkinson: Reemplazando neuronas perdidas ha demostrado potencial en ensayos clínicos, aunque persisten desafíos como el control de la proliferación celular y la integración funcional en el cerebro.
¿Cuál es el papel de las células madre pluripotentes inducidas (iPSC) en el Parkinson?
Las células madre pluripotentes inducidas (iPSC) son reprogramadas a partir de células somáticas del paciente, evitando rechazo inmunológico. Estas se diferencian en neuronas dopaminérgicas para reemplazar las células dañadas en la sustancia negra. Su ventaja radica en la personalización, aunque requieren protocolos rigurosos para asegurar su seguridad y eficacia.
¿Cómo contribuyen las células madre embrionarias (ESC) al tratamiento?
Las células madre embrionarias (ESC) tienen una alta capacidad de diferenciación en neuronas dopaminérgicas, siendo pioneras en Terapia celular para el Parkinson: Reemplazando neuronas perdidas. Sin embargo, plantean desafíos éticos y riesgos de formación de tumores (teratomas), lo que ha impulsado investigaciones para mejorar su control.
¿Qué beneficios ofrecen las células madre mesenquimales (MSC)?
Aunque no se diferencian directamente en neuronas, las células madre mesenquimales (MSC) modulan la neuroinflamación y liberan factores neuroprotectores, favoreciendo la supervivencia de las neuronas existentes. Su uso es menos invasivo y se aplica en terapias complementarias.
| Tipo de Célula | Ventajas | Desafíos |
|---|---|---|
| iPSC | Personalización, bajo riesgo de rechazo | Complejidad en la reprogramación |
| ESC | Alta capacidad de diferenciación | Riesgo de teratomas, cuestiones éticas |
| MSC | Efectos antiinflamatorios, fácil obtención | No generan neuronas dopaminérgicas |
¿Qué papel juega la medicina regenerativa en la restauración de la función neuronal en el Parkinson?
La medicina regenerativa busca restaurar la función neuronal en el Parkinson mediante técnicas como la terapia celular, que incluye el trasplante de células madre para reemplazar las neuronas dopaminérgicas perdidas, promoviendo la neuroprotección y la plasticidad sináptica. Otras estrategias implican el uso de factores de crecimiento y biomateriales para estimular la regeneración neuronal, así como la modulación del microambiente cerebral para reducir la inflamación y favorecer la recuperación funcional. La Terapia celular para el Parkinson: Reemplazando neuronas perdidas destaca por su potencial para integrarse en circuitos cerebrales existentes y compensar el déficit de dopamina.
Estrategias de medicina regenerativa para la recuperación neuronal
La medicina regenerativa aborda el Parkinson mediante múltiples enfoques, incluyendo el uso de células madre pluripotentes para generar neuronas dopaminérgicas funcionales. Estas células pueden diferenciarse in vitro y trasplantarse al cerebro, donde se integran y restablecen conexiones sinápticas. Además, se investigan exosomas derivados de células madre para modular la respuesta inflamatoria y promover la supervivencia neuronal.
Avances en la terapia con células madre para el Parkinson
Los últimos estudios destacan el potencial de las células madre mesenquimales y las iPSCs (células madre pluripotentes inducidas) en la regeneración neuronal. Estas células no solo reemplazan las neuronas dañadas, sino que también secretan factores neurotróficos que mejoran la función de las neuronas residuales. A continuación, una tabla comparativa de los tipos de células utilizadas:
| Tipo de Célula | Ventajas | Desafíos |
|---|---|---|
| Células madre embrionarias | Alta capacidad de diferenciación | Riesgo de formación de tumores |
| iPSCs | Personalización del tratamiento | Complejidad en la reprogramación |
| Células madre mesenquimales | Efecto antiinflamatorio | Baja eficiencia de integración neuronal |
Retos y futuro de la medicina regenerativa en el Parkinson
A pesar de los avances, persisten desafíos como la baja supervivencia de las células trasplantadas y la necesidad de evitar respuestas inmunitarias adversas. La optimización de protocolos de diferenciación celular y el desarrollo de andamios biomiméticos son clave para mejorar la eficacia de la Terapia celular para el Parkinson: Reemplazando neuronas perdidas. La combinación con terapias genéticas y farmacológicas podría potenciar los resultados clínicos.
¿Cuáles son los últimos avances en terapias celulares para el tratamiento del Parkinson?
Los últimos avances en terapias celulares para el tratamiento del Parkinson incluyen el uso de células madre pluripotentes inducidas (iPSCs) para generar neuronas dopaminérgicas, que pueden reemplazar las células perdidas en la sustancia negra. También se están explorando terapias con células madre mesenquimales (MSCs) por su capacidad neuroprotectora y antiinflamatoria, así como técnicas de edición genética CRISPR para corregir mutaciones asociadas a la enfermedad. Ensayos clínicos recientes han demostrado la seguridad y viabilidad de estos enfoques, aunque persisten desafíos como la integración funcional de las células trasplantadas y el control de posibles efectos secundarios. Terapia celular para el Parkinson: Reemplazando neuronas perdidas representa una promesa significativa, pero requiere más investigación para optimizar su eficacia.
Uso de células madre pluripotentes inducidas (iPSCs) en el Parkinson
Las iPSCs son una de las herramientas más prometedoras en la terapia celular para el Parkinson, ya que pueden diferenciarse en neuronas dopaminérgicas funcionales. Estudios recientes han logrado trasplantar estas células en modelos animales, restaurando parcialmente la función motora. Sin embargo, persisten retos como la formación de tumores y la inmunogenicidad, lo que ha llevado al desarrollo de protocolos más seguros para su uso clínico.
Terapias con células madre mesenquimales (MSCs) y sus beneficios
Las MSCs no reemplazan directamente las neuronas perdidas, pero ofrecen ventajas como la neuroprotección y la modulación de la inflamación. Su capacidad para secretar factores neurotróficos las convierte en una opción complementaria para frenar la progresión del Parkinson. Aunque los resultados preliminares son alentadores, se necesitan más estudios para estandarizar su aplicación.
Edición genética CRISPR y su papel en el tratamiento del Parkinson
La tecnología CRISPR está siendo investigada para corregir mutaciones genéticas vinculadas al Parkinson, como las del gen LRRK2 o SNCA. Esta aproximación podría combinarse con terapias celulares para mejorar la supervivencia y función de las neuronas trasplantadas. A continuación, se presenta una tabla con los principales genes objetivo:
| Gen | Función | Estado de investigación |
|---|---|---|
| LRRK2 | Regulación de la autofagia | Ensayos preclínicos |
| SNCA | Síntesis de alfa-sinucleína | Fase inicial |
Preguntas Frecuentes
¿Cómo funciona la terapia celular para reemplazar neuronas en pacientes con Parkinson?
La terapia celular busca sustituir las neuronas dopaminérgicas perdidas en el cerebro de pacientes con Parkinson mediante el trasplante de células madre o células precursoras. Estas células, una vez implantadas, se diferencian en neuronas funcionales para restaurar la producción de dopamina, mejorando los síntomas motores de la enfermedad.
¿Qué tipo de células se utilizan en la terapia para el Parkinson?
Se emplean principalmente células madre pluripotentes inducidas (iPSC) o células madre embrionarias, que pueden ser diferenciadas en laboratorio para convertirse en neuronas dopaminérgicas. Estas células se seleccionan por su capacidad de integrarse en el cerebro y realizar conexiones sinápticas funcionales.
¿Cuáles son los beneficios potenciales de la terapia celular para el Parkinson?
Los beneficios incluyen la mejora motora sostenida, la reducción de la dependencia a medicamentos como la levodopa y la posibilidad de detener o ralentizar la progresión de la enfermedad. Además, al reemplazar neuronas perdidas, se podría restaurar circuitos cerebrales dañados.
¿Existen riesgos o desafíos asociados a esta terapia?
Entre los desafíos destacan el riesgo de rechazo inmunológico, la formación de tumores por proliferación celular no controlada y dificultades técnicas para asegurar la ubicación precisa de las células trasplantadas. Se requieren más estudios para garantizar su seguridad y eficacia a largo plazo.