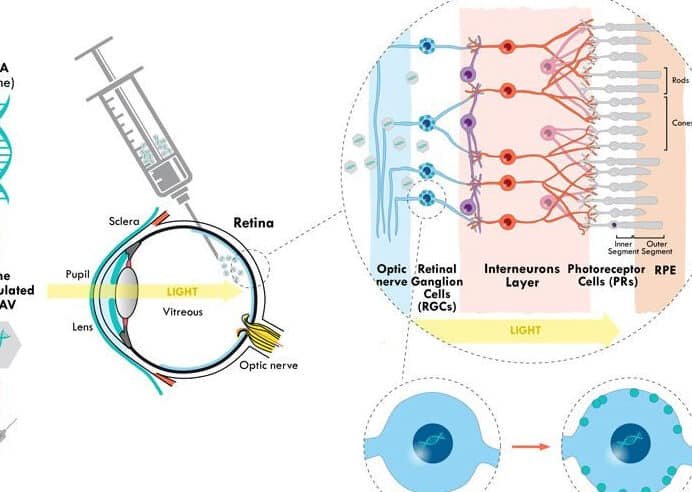
Las terapias de silenciamiento génico para la amiloidosis representan un avance revolucionario en el tratamiento de estas enfermedades, caracterizadas por la acumulación anormal de proteínas amiloides en tejidos y órganos. Estas terapias actúan bloqueando la producción de proteínas defectuosas en su origen, mediante el uso de moléculas como ARN pequeños de interferencia (siRNA) o oligonucleótidos antisentido (ASO). Al reducir la síntesis de las proteínas responsables de la formación de amiloides, se previene el daño progresivo a los órganos afectados. Este enfoque promete transformar el manejo de la amiloidosis, ofreciendo una alternativa precisa y efectiva frente a tratamientos convencionales.
Terapias de silenciamiento génico para la amiloidosis: avances y perspectivas
¿Qué son las Terapias de silenciamiento génico para la amiloidosis?
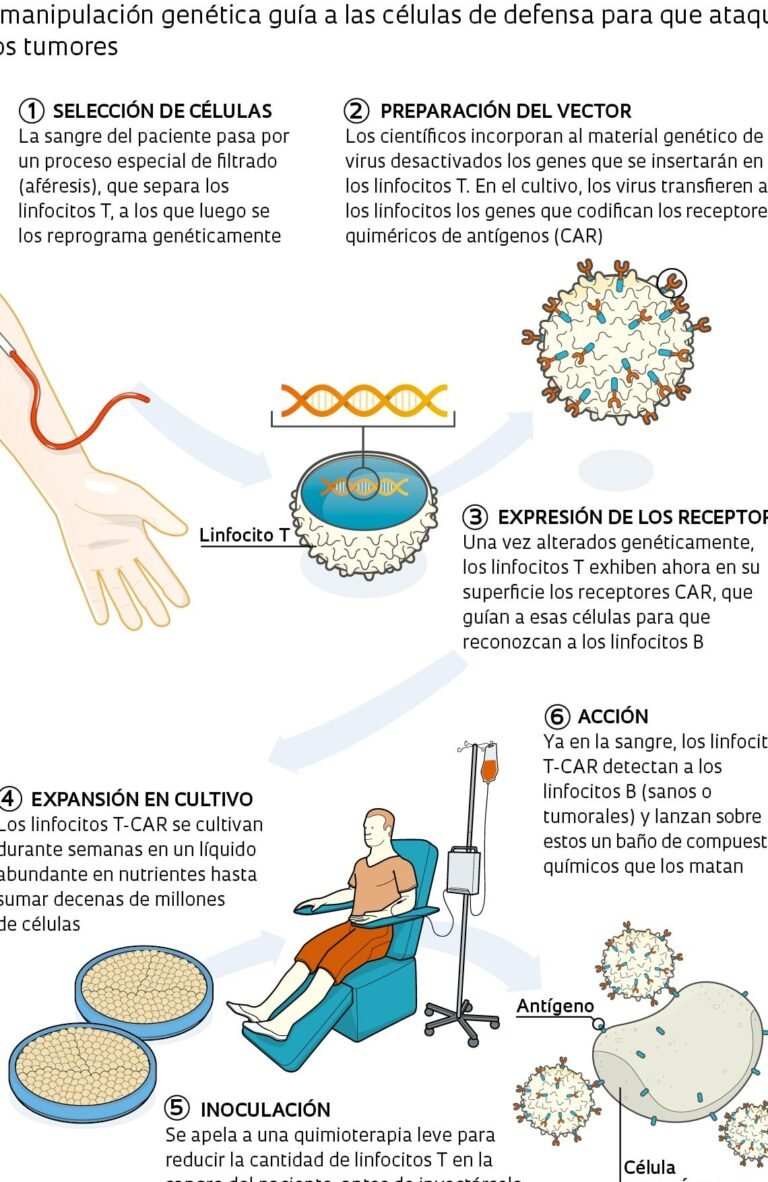
Las Terapias de silenciamiento génico para la amiloidosis son enfoques innovadores que utilizan moléculas como ARN de interferencia (ARNi) o oligonucleótidos antisentido (ASO) para suprimir la expresión de genes responsables de la producción de proteínas amiloidogénicas. Estas terapias actúan a nivel molecular, evitando la acumulación de depósitos de amiloide en órganos y tejidos, lo que puede retrasar o detener la progresión de la enfermedad.
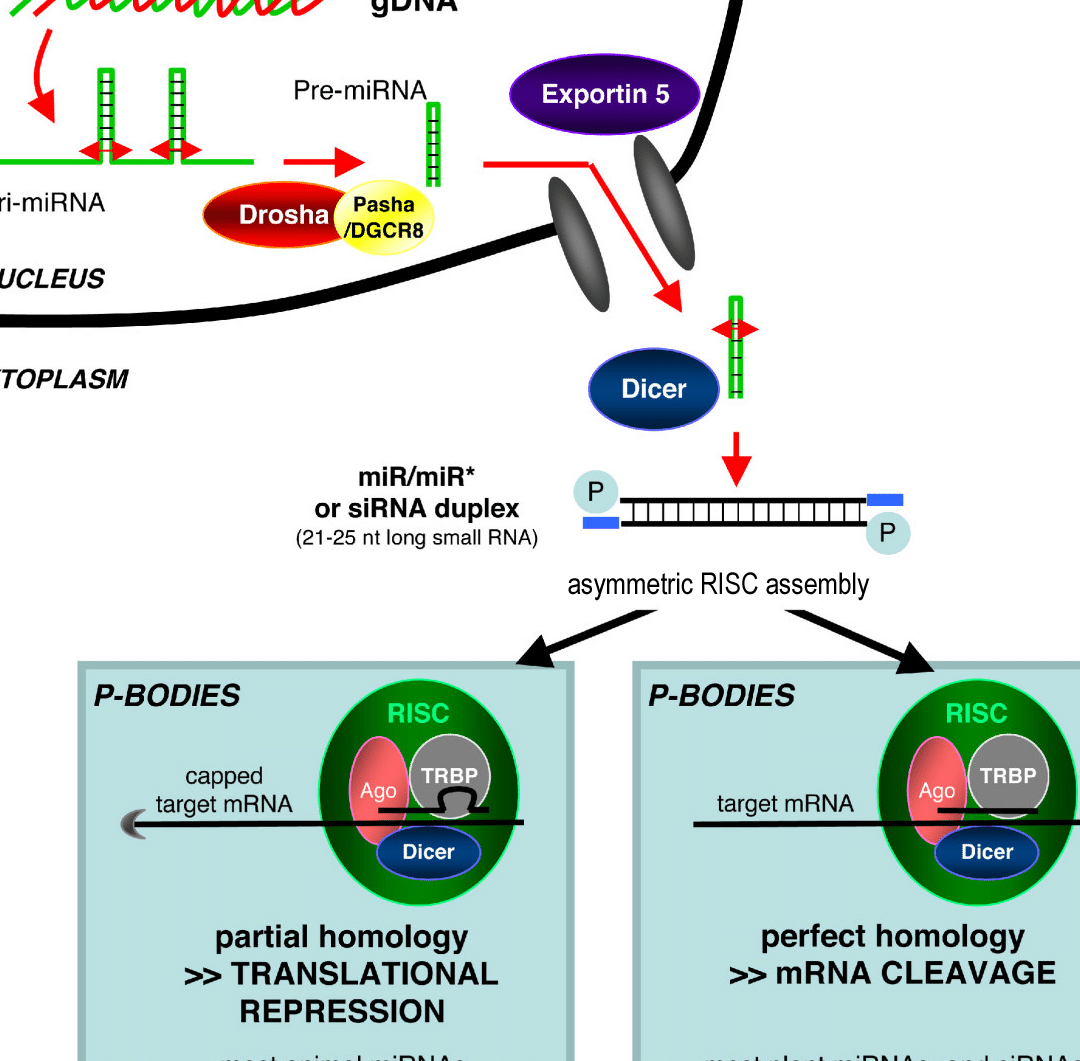
Mecanismos de acción de las Terapias de silenciamiento génico
Estas terapias emplean dos mecanismos principales: ARNi degrada el ARN mensajero (ARNm) específico, mientras que los ASO bloquean su traducción o facilitan su degradación. En la amiloidosis, el objetivo suele ser el gen TTR (transtiretina), cuya mutación provoca una forma hereditaria de la enfermedad. Al silenciar este gen, se reduce la producción de proteínas defectuosas que forman depósitos tóxicos.
Aplicaciones clínicas actuales
Actualmente, las Terapias de silenciamiento génico para la amiloidosis han sido aprobadas para pacientes con amiloidosis hereditaria por transtiretina (hATTR). Medicamentos como patisirán (ARNi) e inotersen (ASO) han demostrado eficacia en ensayos clínicos, mejorando síntomas neurológicos y cardíacos. Su administración es periódica, mediante infusiones o inyecciones subcutáneas.
Ventajas y desafíos de estas terapias
Una ventaja clave es su especificidad, al actuar solo sobre genes diana. Sin embargo, desafíos incluyen la administración repetitiva, posibles efectos secundarios (trombocitopenia con inotersen) y el alto costo. Además, requieren seguimiento continuo para ajustar dosis y evaluar respuestas a largo plazo.
Futuro de las Terapias de silenciamiento génico en amiloidosis
Se investigan mejoras como sistemas de entrega dirigida a órganos afectados (ej. hígado) y terapias combinadas. También se exploran aplicaciones en otras formas de amiloidosis, como la AL (cadena ligera), ampliando el impacto potencial de estas intervenciones.
| Tipo de Terapia | Molécula Utilizada | Gen Objetivo | Ejemplo de Fármaco |
|---|---|---|---|
| ARN de interferencia (ARNi) | siRNA | TTR | Patisirán |
| Oligonucleótidos antisentido (ASO) | ASO | TTR | Inotersen |
Preguntas Frecuentes
¿Qué es la terapia de silenciamiento génico para la amiloidosis?
La terapia de silenciamiento génico es un enfoque innovador que busca reducir o eliminar la producción de proteínas anormales responsables de la amiloidosis. Utiliza moléculas como ARN de interferencia o oligonucleótidos antisentido para bloquear la expresión de genes defectuosos, evitando así la acumulación de amiloide en tejidos y órganos.
¿Cuáles son los beneficios de esta terapia frente a tratamientos convencionales?
Esta terapia ofrece ventajas como una mayor precisión al actuar directamente sobre el gen causante, menos efectos secundarios sistémicos en comparación con quimioterapias, y la potencial capacidad de ralentizar o detener la progresión de la enfermedad, mejorando la calidad de vida del paciente.
¿Qué tipos de amiloidosis pueden tratarse con silenciamiento génico?
Actualmente, el enfoque se centra en formas hereditarias como la amiloidosis por transtiretina (ATTR), donde mutaciones genéticas provocan depósitos dañinos. También se investiga su aplicación en otras variantes, como la amiloidosis AL, aunque su uso en estas aún está en fase experimental.
¿Cuáles son los posibles riesgos o limitaciones de esta terapia?
Aunque prometedora, la terapia puede presentar desafíos como respuestas inmunitarias no deseadas, dificultad para administrarse en órganos específicos, o costes elevados. Además, su efectividad a largo plazo sigue bajo estudio, requiriendo seguimiento continuo en ensayos clínicos.